名校
解题方法
1 . Tapentadol是一种新型止痛药物,合成其中间体ⅷ的路线如下:
(1)化合物ⅰ的分子式为______ ,含有的官能团名称为______ 。
(2)根据化合物iii的结构特征,分析预测其可能的化学性质,完成下表。
(3)反应⑤的方程式可表示为ⅲ+ⅳ→ⅶ+y,化合物y的化学式为______ 。
(4)关于反应⑥的说法中,正确的有______。
(5)化合物x是ⅱ的同分异构体,满足下列条件的同分异构体有______ 种。
a.含有苯环,且苯环上有两个侧链
b.与 溶液反应显紫色
溶液反应显紫色
c.1 mol x与足量Na反应,生成1 mol
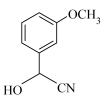
(6)以 和NaCN为含碳原料,合成化合物
和NaCN为含碳原料,合成化合物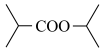 。
。
基于你设计的合成路线,回答下列问题:
①相关步骤涉及到卤代烃制醇反应,其化学方程式为____________ 。
②最后一步反应中,能与 反应产生
反应产生 的有机反应物为
的有机反应物为______ (写结构简式)。
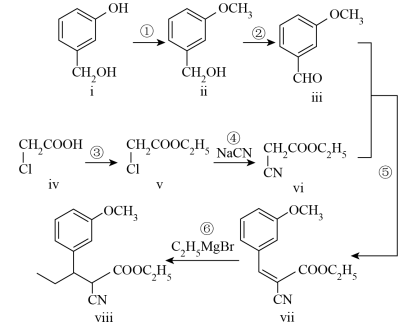
(1)化合物ⅰ的分子式为
(2)根据化合物iii的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂、条件 | 反应形成的新物质 | 反应类型 |
| a | 新制 、加热 、加热 | ||
| b |
|
(3)反应⑤的方程式可表示为ⅲ+ⅳ→ⅶ+y,化合物y的化学式为
(4)关于反应⑥的说法中,正确的有______。
| A.反应过程中,有π键发生断裂 | B.化合物ⅶ的 杂化的原子只有C 杂化的原子只有C |
| C.化合物ⅶ所有碳原子一定处于同一平面上 | D.化合物ⅷ只有1个手性碳原子 |
(5)化合物x是ⅱ的同分异构体,满足下列条件的同分异构体有
a.含有苯环,且苯环上有两个侧链
b.与
 溶液反应显紫色
溶液反应显紫色c.1 mol x与足量Na反应,生成1 mol

(6)以
 和NaCN为含碳原料,合成化合物
和NaCN为含碳原料,合成化合物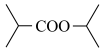 。
。基于你设计的合成路线,回答下列问题:
①相关步骤涉及到卤代烃制醇反应,其化学方程式为
②最后一步反应中,能与
 反应产生
反应产生 的有机反应物为
的有机反应物为
您最近一年使用:0次
2024-03-22更新
|
1333次组卷
|
4卷引用:2024届宁夏银川市唐徕中学高三下学期四模理科综合试题-高中化学
2024届宁夏银川市唐徕中学高三下学期四模理科综合试题-高中化学广东省佛山市2024届高三教学质量检测(一)化学试题(已下线)题型12 有机推断题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)压轴题14?有机合成与推断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)-2024年高考化学压轴题专项训练(新高考通用)
2 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。
(1)以生物材质(以 计)与水蒸气反应制取
计)与水蒸气反应制取 是一种低耗能,高效率的制
是一种低耗能,高效率的制 方法。该方法由气化炉制造
方法。该方法由气化炉制造 和燃烧炉再生
和燃烧炉再生 两步构成,气化炉中涉及到的反应如下:
两步构成,气化炉中涉及到的反应如下:
I.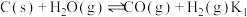
Ⅱ.
Ⅲ.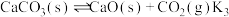
Ⅳ.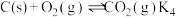
①该工艺制 总反应可表示为
总反应可表示为 ,该反应的平衡常数
,该反应的平衡常数
___________ (用 等的代数式表示)。
等的代数式表示)。
②绝热条件下,将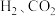 以体积比
以体积比 充入恒容密闭容器中,若只发生反应Ⅱ,下列可作为反应Ⅱ达到平衡的判据是
充入恒容密闭容器中,若只发生反应Ⅱ,下列可作为反应Ⅱ达到平衡的判据是___________ 。
A. 与
与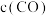 比值不变 B.容器内气体密度不变
比值不变 B.容器内气体密度不变
C.容器内气体压强不变 D.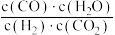 不变
不变
(2) 的速率方程为
的速率方程为 ,
,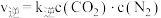 (
( 、
、 为速率常数,与温度、催化剂、接触面积有关,与浓度无关)。
为速率常数,与温度、催化剂、接触面积有关,与浓度无关)。
净反应速率 等于正、逆反应速率之差,平衡时,
等于正、逆反应速率之差,平衡时,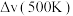
___________ (填“>”、“<”或“=”) 。
。
(3)一定条件下, 与
与 反应可合成
反应可合成 ,
, ,该反应分两步进行:
,该反应分两步进行:
ⅰ.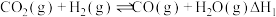
ⅱ.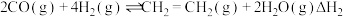
 ,压强恒定为
,压强恒定为 时,将
时,将 的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
 的平衡转化率为
的平衡转化率为___________ ,反应ⅰ的平衡常数
___________ ( 是以分压表示的平衡常数,分压
是以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(4)利用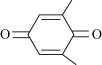 (Q)与
(Q)与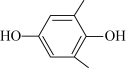 (QH2)电解转化法从烟气中分离
(QH2)电解转化法从烟气中分离 的原理如图,已知气体可选择性通过膜电极,溶液不能通过
的原理如图,已知气体可选择性通过膜电极,溶液不能通过
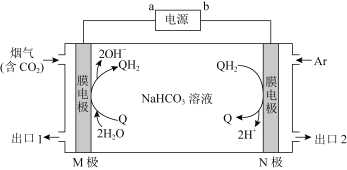
①(填“a”或“b”)___________ 为电源负极。
② 从出口
从出口___________ (填“1”或“2”)排出, 在
在 极上发生的反应为
极上发生的反应为___________ 。
(1)以生物材质(以
 计)与水蒸气反应制取
计)与水蒸气反应制取 是一种低耗能,高效率的制
是一种低耗能,高效率的制 方法。该方法由气化炉制造
方法。该方法由气化炉制造 和燃烧炉再生
和燃烧炉再生 两步构成,气化炉中涉及到的反应如下:
两步构成,气化炉中涉及到的反应如下:I.
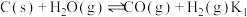
Ⅱ.

Ⅲ.
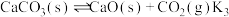
Ⅳ.
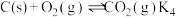
①该工艺制
 总反应可表示为
总反应可表示为 ,该反应的平衡常数
,该反应的平衡常数
 等的代数式表示)。
等的代数式表示)。②绝热条件下,将
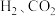 以体积比
以体积比 充入恒容密闭容器中,若只发生反应Ⅱ,下列可作为反应Ⅱ达到平衡的判据是
充入恒容密闭容器中,若只发生反应Ⅱ,下列可作为反应Ⅱ达到平衡的判据是A.
 与
与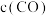 比值不变 B.容器内气体密度不变
比值不变 B.容器内气体密度不变C.容器内气体压强不变 D.
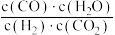 不变
不变(2)
 的速率方程为
的速率方程为 ,
,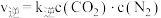 (
( 、
、 为速率常数,与温度、催化剂、接触面积有关,与浓度无关)。
为速率常数,与温度、催化剂、接触面积有关,与浓度无关)。净反应速率
 等于正、逆反应速率之差,平衡时,
等于正、逆反应速率之差,平衡时,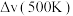
 。
。(3)一定条件下,
 与
与 反应可合成
反应可合成 ,
, ,该反应分两步进行:
,该反应分两步进行:ⅰ.
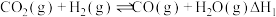
ⅱ.
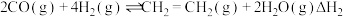
 ,压强恒定为
,压强恒定为 时,将
时,将 的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:| 组分 |  |  |  |
| 物质的量分数(%) | 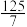 | 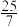 | 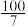 |
 的平衡转化率为
的平衡转化率为
 是以分压表示的平衡常数,分压
是以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。(4)利用
 (Q)与
(Q)与 (QH2)电解转化法从烟气中分离
(QH2)电解转化法从烟气中分离 的原理如图,已知气体可选择性通过膜电极,溶液不能通过
的原理如图,已知气体可选择性通过膜电极,溶液不能通过
①(填“a”或“b”)
②
 从出口
从出口 在
在 极上发生的反应为
极上发生的反应为
您最近一年使用:0次
名校
解题方法
3 . 标况下, 的溶解度约为
的溶解度约为 ,
, ;室温下
;室温下 溶液中各含碳粒子的物质的量分数与
溶液中各含碳粒子的物质的量分数与 的关系如图1所示,向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中
的关系如图1所示,向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中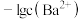 与
与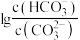 的关系如图2所示,下列说法正确的是
的关系如图2所示,下列说法正确的是
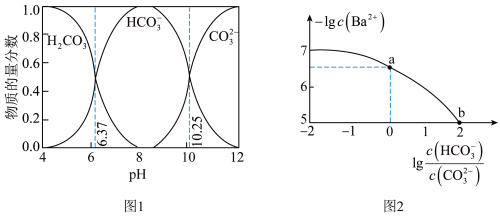
 的溶解度约为
的溶解度约为 ,
, ;室温下
;室温下 溶液中各含碳粒子的物质的量分数与
溶液中各含碳粒子的物质的量分数与 的关系如图1所示,向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中
的关系如图1所示,向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中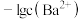 与
与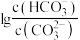 的关系如图2所示,下列说法正确的是
的关系如图2所示,下列说法正确的是
A.饱和碳酸的浓度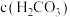 约为 约为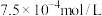 |
B. 对应的溶液中存在: 对应的溶液中存在: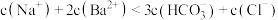 |
C. 的过程中,溶液中 的过程中,溶液中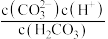 逐渐减小 逐渐减小 |
D. 点对应溶液的 点对应溶液的 为9.25 为9.25 |
您最近一年使用:0次
名校
4 . 化合物G是用于治疗慢性便秘药品普卡必利的中间体,其合成路线如下:
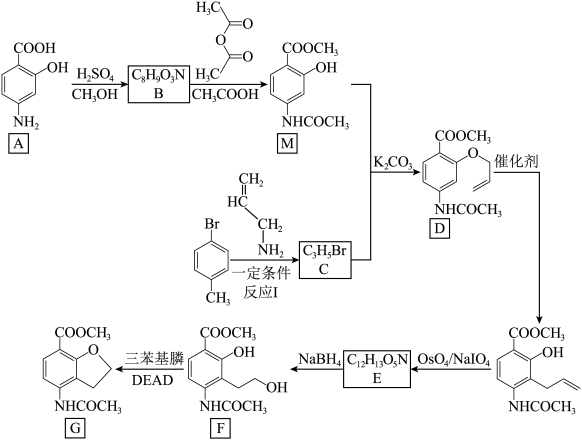
已知: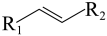
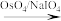
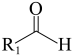 +
+
回答下列问题。
(1)有机物A中的官能团为羟基、羧基和_______ 。
(2)反应A→B的化学方程式为_______ 。
(3)M+C→D为可逆反应,推测 的作用:
的作用:_______ 。
(4)E的结构简式为_______ 。
(5)写出符合下列条件的B的一种同分异构体的结构简式_______ 。
①属于 -氨基酸(氨基连接在与羧基相连的碳原子上)
-氨基酸(氨基连接在与羧基相连的碳原子上)
②遇 溶液显紫色
溶液显紫色
(6)请根据流程中的信息,设计以苯酚和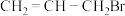 为原料合成
为原料合成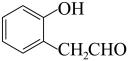 的合成路线
的合成路线_______ 。

已知:

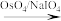
 +
+
回答下列问题。
(1)有机物A中的官能团为羟基、羧基和
(2)反应A→B的化学方程式为
(3)M+C→D为可逆反应,推测
 的作用:
的作用:(4)E的结构简式为
(5)写出符合下列条件的B的一种同分异构体的结构简式
①属于
 -氨基酸(氨基连接在与羧基相连的碳原子上)
-氨基酸(氨基连接在与羧基相连的碳原子上)②遇
 溶液显紫色
溶液显紫色(6)请根据流程中的信息,设计以苯酚和
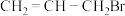 为原料合成
为原料合成 的合成路线
的合成路线
您最近一年使用:0次
名校
解题方法
5 . 下列表格中各项分类都正确 的一组是
类别 选项 | 离子化合物 | 电解质 | 酸性氧化物 | 碱性氧化物 | 强酸 |
| A | AlCl3 | 熔融态KNO3 | NO2 | Na2O2 | H2SO3 |
| B | NH3·H2O | 铁 | ClO2 | Fe3O4 | NaHSO4 |
| C | K2S | 胆矾 | SO3 | MgO | HClO4 |
| D | CH3COONH4 | 盐酸 | CO2 | Al2O3 | HI |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 中医药作为中国优秀传统文化的典范,凝聚着祖先的智慧和经验的结晶。矿物药的成分主要为金属﹑金属氧化物﹑盐等。
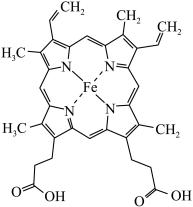
(1)铁华粉常用来治疗血虚萎黄,其成分为醋酸亚铁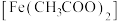 ,其形成的血红素分子结构如图所示。铁位于周期表的
,其形成的血红素分子结构如图所示。铁位于周期表的___________ 区,铁华粉中基态亚铁离子的未成对电子数与其电子总数之比为___________ ,铁华粉中组成元素的电负性由大到小的顺序为___________ (填元素符号),血红素分子中铁(Ⅱ)的配位数为___________ 。
(2)生石灰可用于止血,轻质氧化镁可用于治疗便秘。请比较CaO、MgO的熔点大小,并请解释原因:___________ 。
(3)多原子分子中各原子若在同一平面,且有相互平行的 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,如
键”,如 分子中存在“离域
分子中存在“离域 键”,可表示成
键”,可表示成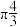 ,则
,则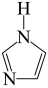 (咪唑)中的“离域
(咪唑)中的“离域 键”可表示为
键”可表示为___________ 。
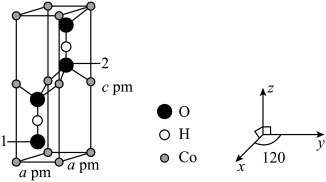
(4)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号 原子的坐标为
原子的坐标为 ,则2号
,则2号 原子的坐标为
原子的坐标为___________ 。设 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  (用代数式表示)。
(用代数式表示)。
(1)铁华粉常用来治疗血虚萎黄,其成分为醋酸亚铁
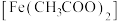 ,其形成的血红素分子结构如图所示。铁位于周期表的
,其形成的血红素分子结构如图所示。铁位于周期表的
(2)生石灰可用于止血,轻质氧化镁可用于治疗便秘。请比较CaO、MgO的熔点大小,并请解释原因:
(3)多原子分子中各原子若在同一平面,且有相互平行的
 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,如
键”,如 分子中存在“离域
分子中存在“离域 键”,可表示成
键”,可表示成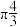 ,则
,则 (咪唑)中的“离域
(咪唑)中的“离域 键”可表示为
键”可表示为(4)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号
 原子的坐标为
原子的坐标为 ,则2号
,则2号 原子的坐标为
原子的坐标为 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
7 . I.金属镁性质活泼,能与许多物质反应,某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2中燃烧,可能产物为MgO、N2和Mg3N2.通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO2气体能被NaOH溶液吸收,Mg3N2极易与水反应。___________ (填字母);装置B的作用是___________ 。
(2)用来检验N2的实验装置为___________ (填字母)。
(3)设计实验证明产物中存在Mg3N2:___________ 。
Ⅱ.二氧化氯(ClO2)是一种黄绿色气体,沸点为11℃,不稳定,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。ClO2易溶于水但不与水反应,其水溶液在温度过高时有可能爆炸。某小组按照如图实验装置制备ClO2并验证其某些性质。回答下列问题:___________ 。
(5)通入氮气的主要作用有两个,一是可以起到搅拌作用,二是___________ 。
(6)B装置的作用是________ 。C装置用来吸收ClO2,则C中液体宜选用_________ (填序号)。
①热水②冰水③饱和食盐水
(7)D装置中ClO2与NaOH溶液反应可生成等物质的量的两种钠盐,其中一种为NaClO2,D装置中生成这两种钠盐的化学方程式为___________ ;饱和NaClO2溶液在温度低于38℃时析出晶体NaClO2·3H2O,在温度高于38℃时析出晶体NaClO2.请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:a.___________ ;b.___________ ;c.洗涤;d.干燥。
(8)设计一个简易实验证明二氧化氯具有永久的漂白性:___________ 。
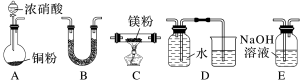
(2)用来检验N2的实验装置为
(3)设计实验证明产物中存在Mg3N2:
Ⅱ.二氧化氯(ClO2)是一种黄绿色气体,沸点为11℃,不稳定,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。ClO2易溶于水但不与水反应,其水溶液在温度过高时有可能爆炸。某小组按照如图实验装置制备ClO2并验证其某些性质。回答下列问题:
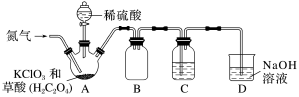
(5)通入氮气的主要作用有两个,一是可以起到搅拌作用,二是
(6)B装置的作用是
①热水②冰水③饱和食盐水
(7)D装置中ClO2与NaOH溶液反应可生成等物质的量的两种钠盐,其中一种为NaClO2,D装置中生成这两种钠盐的化学方程式为
(8)设计一个简易实验证明二氧化氯具有永久的漂白性:
您最近一年使用:0次
2024-02-14更新
|
86次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题
8 . 化石燃料的燃烧、汽车尾气的排放和硝酸工业尾气中普遍含有的NOx是污染大气的主要成分之一,需要回收处理并加以利用。
(1)为减轻汽车尾气中NO和CO对环境的污染,可在汽车排气管上安装催化转化器,主要发生的反应是:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH。
N2(g)+2CO2(g) ΔH。
已知断裂1mol相应化学键需要的能量如表:
则ΔH为___________ 。
(2)已知:CH4(g)+4NO2(g)=CO2(g)+2H2O(l)+4NO(g) ΔH=-654kJ·mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(l)+2N2(g) ΔH=-1240kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
CH4将NO2还原为N2并生成水蒸气的热化学方程式为___________ 。
(3)燃煤烟气脱硝的反应之一为 2NO2(g) + 4CO(g) N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
0~2 min内该反应的平均速率为v(N2)=___________ , 8分钟时反应达到平衡,则NO2的平衡转化率=___________ ;n值可能为___________ (填字母)。
A.3.2 B.3.36 C.3.3 D.3.1
(4)NH3催化还原氮氧化物技术(SCR)是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示:
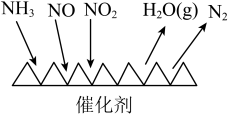
用Fe作催化剂时,在氨气足量的情况下,当c(NO2):c(NO)=1:1时,脱氮率最佳,按最佳脱氮率,每生成2mol N2,转移电子数目为___________ 。
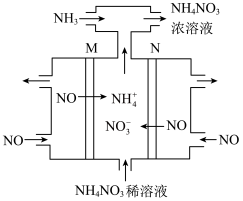
(5)除上述方法外,还可用电解法将NO转变为NH4NO3,其工作原理如下图,N极的电极反应式为___________ ,通入NH3的主要原因是___________ 。
(1)为减轻汽车尾气中NO和CO对环境的污染,可在汽车排气管上安装催化转化器,主要发生的反应是:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH。
N2(g)+2CO2(g) ΔH。已知断裂1mol相应化学键需要的能量如表:
| 化学键 | C≡O | N≡O | N≡N | C=O |
| 键能/(kJ·mol-1) | 1072 | 630 | 946 | 799 |
(2)已知:CH4(g)+4NO2(g)=CO2(g)+2H2O(l)+4NO(g) ΔH=-654kJ·mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(l)+2N2(g) ΔH=-1240kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
CH4将NO2还原为N2并生成水蒸气的热化学方程式为
(3)燃煤烟气脱硝的反应之一为 2NO2(g) + 4CO(g)
 N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:| 时间 | 0 min | 2 min | 4 min | 6 min | 8min | 10 min |
| n(NO2)/mol | 4.0 | 3.6 | n | 3.1 | 3.0 | 3.0 |
A.3.2 B.3.36 C.3.3 D.3.1
(4)NH3催化还原氮氧化物技术(SCR)是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示:

用Fe作催化剂时,在氨气足量的情况下,当c(NO2):c(NO)=1:1时,脱氮率最佳,按最佳脱氮率,每生成2mol N2,转移电子数目为
(5)除上述方法外,还可用电解法将NO转变为NH4NO3,其工作原理如下图,N极的电极反应式为

您最近一年使用:0次
2024-02-13更新
|
101次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题
9 . 甲烷是天然气的主要成分,是一种重要的清洁能源和化工原料。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知: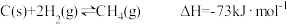
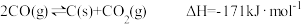
CO(g)+3H2(g) CH4(g)+H2O(g)ΔH=-203kJ·mol-1
CH4(g)+H2O(g)ΔH=-203kJ·mol-1
写出CO与H2O(g)反应生成H2和CO2的热化学方程式___________ 。
(2)工业上常用 与水蒸气在一定条件下来制取H2,其原理为:
与水蒸气在一定条件下来制取H2,其原理为: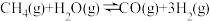 。
。
①一定温度时,在一个体积为2L的恒容密闭容器中,加入1molCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为___________ ,此反应的平衡常数为___________  (结果保留到小数点后三位)。
(结果保留到小数点后三位)。
②下列说法中能说明此反应达到平衡状态的是___________ 。
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.体系的平均相对分子质量不再发生变化
D.体系的密度不再发生变化
E.反应速率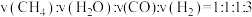
(3)一定温度下,向某密闭容器中充入适量CH3CHO(g),发生反应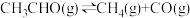 ,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
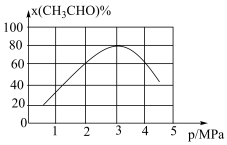
①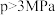 时,增大压强,CH3CHO的转化率降低,其原因是
时,增大压强,CH3CHO的转化率降低,其原因是___________ 。
②当压强为4MPa时,该反应的平衡常数Kp=___________ MPa(用各物质分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
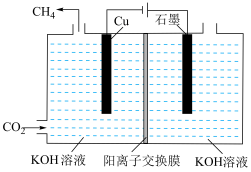
(4) 电化学制
电化学制 。下图表示以KOH溶液作电解质溶液进行电解的示意图,
。下图表示以KOH溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为___________ 。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知:
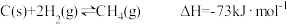
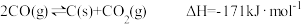
CO(g)+3H2(g)
 CH4(g)+H2O(g)ΔH=-203kJ·mol-1
CH4(g)+H2O(g)ΔH=-203kJ·mol-1写出CO与H2O(g)反应生成H2和CO2的热化学方程式
(2)工业上常用
 与水蒸气在一定条件下来制取H2,其原理为:
与水蒸气在一定条件下来制取H2,其原理为: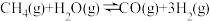 。
。①一定温度时,在一个体积为2L的恒容密闭容器中,加入1molCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为
 (结果保留到小数点后三位)。
(结果保留到小数点后三位)。②下列说法中能说明此反应达到平衡状态的是
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.体系的平均相对分子质量不再发生变化
D.体系的密度不再发生变化
E.反应速率
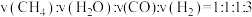
(3)一定温度下,向某密闭容器中充入适量CH3CHO(g),发生反应
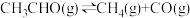 ,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
①
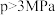 时,增大压强,CH3CHO的转化率降低,其原因是
时,增大压强,CH3CHO的转化率降低,其原因是②当压强为4MPa时,该反应的平衡常数Kp=
(4)
 电化学制
电化学制 。下图表示以KOH溶液作电解质溶液进行电解的示意图,
。下图表示以KOH溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为
您最近一年使用:0次
名校
解题方法
10 . “天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一、回答:
(1)镍基态原子有___________ 种不同空间运动状态的电子,第四周期与基态镍原子单电子数相同的元素有___________ 种(不含镍元素)。
(2)Ni2+与丁二酮肟可形成鲜红色的二丁二酮肟合镍(M= 289 g·mol-1),结构如下图所示。0.2mol二丁二酮肟合镍分子内含有σ键___________ mol,碳碳键是由___________ 轨道重叠形成的。

a.sp3和sp2 b.sp2和 sp2 c.sp2和p d.sp3和p
(3) 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键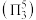 。
。 键角
键角___________  键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因___________ 。
(4)人类合成的第一个稀有气体化合物是XeF+PtF ,PtF
,PtF 中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在氧原子围成的___________ (填“四面体”“立方体"或“八面体”)空隙中,该晶胞的空间利用率为___________ (铼的原子半径为rRepm,氧原子半径为rOpm,列出计算式)。
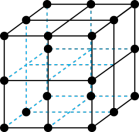
(6)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
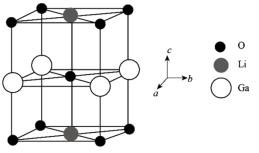
①上述晶胞沿着a轴的投影图为___________ (填字母)。
A. B.
B.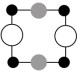 C.
C.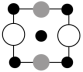
②用 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为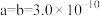 m,
m,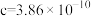 m,则其密度为
m,则其密度为___________  (列出计算式即可)。
(列出计算式即可)。
(1)镍基态原子有
(2)Ni2+与丁二酮肟可形成鲜红色的二丁二酮肟合镍(M= 289 g·mol-1),结构如下图所示。0.2mol二丁二酮肟合镍分子内含有σ键

a.sp3和sp2 b.sp2和 sp2 c.sp2和p d.sp3和p
(3)
 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键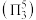 。
。 键角
键角 键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因(4)人类合成的第一个稀有气体化合物是XeF+PtF
 ,PtF
,PtF 中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。| A.熔化状态下不能导电 |
| B.XeF+中所有原子都满足8电子稳定结构 |
| C.用两个Cl替换F后,所得PtF4Cl2有两种结构 |
| D.含有离子键、极性键、非极性键和配位键 |
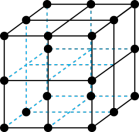
(6)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:

①上述晶胞沿着a轴的投影图为
A.
 B.
B. C.
C.
②用
 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为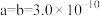 m,
m,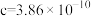 m,则其密度为
m,则其密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次