名校
解题方法
1 . 资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)CO2的捕集:
①CO2属于___________ 分子(填“极性”或“非极性”),其晶体(干冰)属于__________ 晶体。
②用饱和 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)=_______ ;(室温下, 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式_____ 。
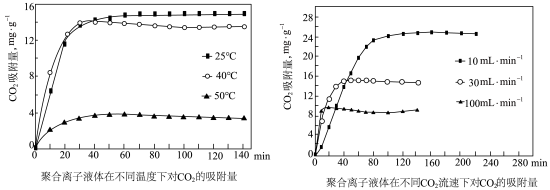
③聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是____________ 。
(2)生产尿素:工业上以CO2、 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步: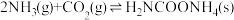
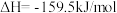
第二步:
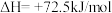
写出上述合成尿素的热化学方程式_______ 。
(3)合成乙酸:中国科学家首次以 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
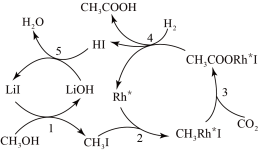
①原料中的 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:____________ 。
②根据图示 ,写出总反应的化学方程式:_______ 。
(1)CO2的捕集:
①CO2属于
②用饱和
 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)= 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式③聚合离子液体是目前广泛研究的CO2吸附剂。

(2)生产尿素:工业上以CO2、
 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:第一步:
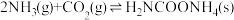
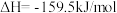
第二步:

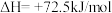
写出上述合成尿素的热化学方程式
(3)合成乙酸:中国科学家首次以
 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
①原料中的
 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:②
您最近一年使用:0次
2024-04-04更新
|
362次组卷
|
3卷引用:天津市南开中学2020届高三一模化学试卷
2 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
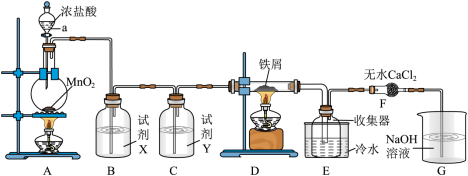
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
名校
3 . 下列实验操作能达到其对应目的的是
| 实验目的 | 操作 | |
| A | 欲证明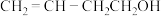 中含有碳碳双键 中含有碳碳双键 | 取该物质适量于试管,滴入酸性 溶液 溶液 |
| B | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,生成三溴苯酚白色沉淀,过滤 |
| C | 欲检验乙醇的消去反应产物 | 将乙醇与浓硫酸混合,迅速加热到170℃(务必迅速加热到170℃,140℃会有乙醚生成),将气体产物通过导气管直接通入酸性高锰酸钾 |
| D | 欲证明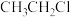 中含有氯原子 中含有氯原子 | 取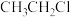 在碱性条件下的水解液适量于试管,加足量硝酸酸化,再加入 在碱性条件下的水解液适量于试管,加足量硝酸酸化,再加入 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-08更新
|
733次组卷
|
3卷引用:天津市双菱中学2023-2024学年高二下学期期中质量检测化学试卷
解题方法
4 . 常温下,二元弱酸 在溶液中各组分百分含量
在溶液中各组分百分含量 随溶液pH的变化如图所示。下列说法错误的是
随溶液pH的变化如图所示。下列说法错误的是
 在溶液中各组分百分含量
在溶液中各组分百分含量 随溶液pH的变化如图所示。下列说法错误的是
随溶液pH的变化如图所示。下列说法错误的是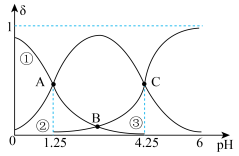
A.曲线②表示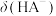 随溶液pH的变化 随溶液pH的变化 |
B. 的一级电离常数 的一级电离常数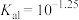 |
C.NaHA溶液中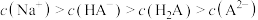 |
D.常温下,若向 溶液中滴加 溶液中滴加 溶液使溶液pH=7,则一定存在: 溶液使溶液pH=7,则一定存在: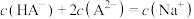 |
您最近一年使用:0次
2024-02-25更新
|
728次组卷
|
7卷引用:天津市红桥区2024届高三下学期二模化学试题
天津市红桥区2024届高三下学期二模化学试题2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学甘肃省白银市名校2023-2024学年高三下学期联合调研化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)甘肃省天水市麦积区2024届高三下学期2月第二次模拟检测化学试题2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学四川省成都市崇州市怀远中学2023-2024学年高三上学期期末理综试题-高中化学
5 . 锰和硫能形成多种重要的化合物,在工业生产中有广泛应用。回答下列问题:
(1)烟气中的SO2可与CO进行综合处理。
已知:Ⅰ.S(g)+O2(g)=SO2(g) ΔH=-297.3kJ·mol-1
Ⅱ.CO的燃烧热283kJ·mol-1
Ⅲ.相关化学键的键能数据如表所示:
①表中x=___________ 。
②写出CO的燃烧热的热化学方程式:___________ 。
③以物质的量之比为1﹕2的SO2和CO充入密闭容器中发生反应SO2(g)+2CO(g) S(g)+2CO2(g) ΔH,SO2(g)和S(g)平衡时的体积分数(φ)与温度(T)的关系如图所示,图中表示SO2(g)平衡时的体积分数与温度关系的曲线为
S(g)+2CO2(g) ΔH,SO2(g)和S(g)平衡时的体积分数(φ)与温度(T)的关系如图所示,图中表示SO2(g)平衡时的体积分数与温度关系的曲线为___________ (填“L1”或“L2”),T0℃时该反应的平衡常数K=___________ 。

(2)Na2S2O8具有强氧化性,其中的S元素为+6价,Na2S2O8用于检验水相中的Mn2+时,生成SO 且溶液变为紫红色,1molNa2S2O8中过氧键的数目为
且溶液变为紫红色,1molNa2S2O8中过氧键的数目为___________ ;检验Mn2+的反应中氧化剂和还原剂的物质的量之比为___________ 。
(3)MnO2可用如图装置电解方法制备,电解池中间是质子交换膜,分隔开的两室溶液分别为足量的硫酸钠溶液和足量的硫酸锰溶液,则阴极室中的溶液为___________ ;电解产生的MnO2沉积在电极上,若一段时间后该电极所在的溶液质量减轻了4.45g,则电路中转移电子的物质的量为___________ mol。

(1)烟气中的SO2可与CO进行综合处理。
已知:Ⅰ.S(g)+O2(g)=SO2(g) ΔH=-297.3kJ·mol-1
Ⅱ.CO的燃烧热283kJ·mol-1
Ⅲ.相关化学键的键能数据如表所示:
| 化学键 | C O O | C=O | O=O |
| 键能(E)/kJ·mol-1 | 1076 | x | 498 |
②写出CO的燃烧热的热化学方程式:
③以物质的量之比为1﹕2的SO2和CO充入密闭容器中发生反应SO2(g)+2CO(g)
 S(g)+2CO2(g) ΔH,SO2(g)和S(g)平衡时的体积分数(φ)与温度(T)的关系如图所示,图中表示SO2(g)平衡时的体积分数与温度关系的曲线为
S(g)+2CO2(g) ΔH,SO2(g)和S(g)平衡时的体积分数(φ)与温度(T)的关系如图所示,图中表示SO2(g)平衡时的体积分数与温度关系的曲线为
(2)Na2S2O8具有强氧化性,其中的S元素为+6价,Na2S2O8用于检验水相中的Mn2+时,生成SO
 且溶液变为紫红色,1molNa2S2O8中过氧键的数目为
且溶液变为紫红色,1molNa2S2O8中过氧键的数目为(3)MnO2可用如图装置电解方法制备,电解池中间是质子交换膜,分隔开的两室溶液分别为足量的硫酸钠溶液和足量的硫酸锰溶液,则阴极室中的溶液为

您最近一年使用:0次
名校
解题方法
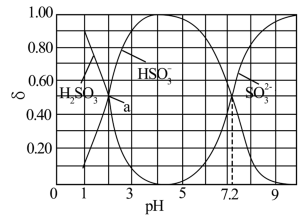
6 . 边搅拌边向 溶液中通入
溶液中通入 制备
制备 溶液,水溶液中
溶液,水溶液中 、
、 、
、 的分布系数δ随pH的变化关系如图所示。[比如
的分布系数δ随pH的变化关系如图所示。[比如 的分布系数:
的分布系数: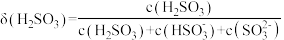 ]下列有关叙述错误的是
]下列有关叙述错误的是
 溶液中通入
溶液中通入 制备
制备 溶液,水溶液中
溶液,水溶液中 、
、 、
、 的分布系数δ随pH的变化关系如图所示。[比如
的分布系数δ随pH的变化关系如图所示。[比如 的分布系数:
的分布系数: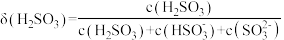 ]下列有关叙述错误的是
]下列有关叙述错误的是
| A.当溶液pH范围为4~5时,停止通入SO2 |
B.根据曲线数据计算可知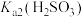 的数量级为 的数量级为 |
C.a点的溶液中 |
D. 的溶液中, 的溶液中,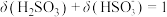 |
您最近一年使用:0次
名校
7 . 如图所示与对应叙述相符的是
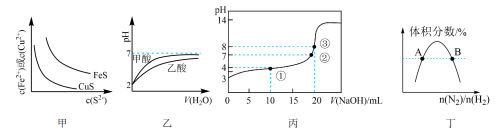

A.图甲:一定温度 、 、 沉淀溶解平衡曲线,则 沉淀溶解平衡曲线,则 |
B.图乙:等体积 的甲酸与乙酸稀释的 的甲酸与乙酸稀释的 曲线,则酸性:甲酸 曲线,则酸性:甲酸 乙酸 乙酸 |
C.图丙:某温度下向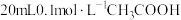 溶液中逐滴加入 溶液中逐滴加入 溶液, 溶液, 变化曲线如图丙所示(忽略温度变化),则①点 变化曲线如图丙所示(忽略温度变化),则①点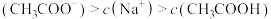 |
D.图丁: 平衡时 平衡时 体积分数随起始 体积分数随起始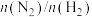 变化曲线,则转化率: 变化曲线,则转化率: |
您最近一年使用:0次
名校
8 . 完成下列小题
(1)现有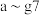 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
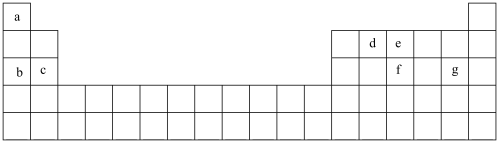
①元素 和f在周期表中的位置
和f在周期表中的位置_____ ,_____ 。
②用电子式表示由 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:_____ 。
③元素的原子间反应最容易形成离子键的是_____ 。
A.c和f B.b和g C.d和g D.b和
④ 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子_____ (填“是”或“不是”)都满足最外层为8电子结构
(2) 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中, 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:
①下列元素的符号:
_____ 、
_____ 、
_____ 。
② 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为 。写出该化合物的化学式
。写出该化合物的化学式_____ 。
(1)现有
 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
①元素
 和f在周期表中的位置
和f在周期表中的位置②用电子式表示由
 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:③元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和

④
 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子(2)
 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,
 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:①下列元素的符号:



②
 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为 。写出该化合物的化学式
。写出该化合物的化学式
您最近一年使用:0次
名校
解题方法
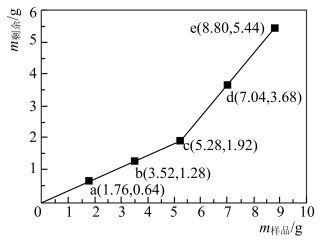
9 . 为确定 和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入
和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入 某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
 和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入
和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入 某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
A.稀硫酸中溶质的浓度为 |
B.该混合物中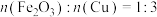 |
C.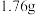 样品充分反应后,溶液中一定存在 样品充分反应后,溶液中一定存在 和 和 ,一定不存在 ,一定不存在 |
D.各组样品均发生反应: 、 、 |
您最近一年使用:0次
2024-02-14更新
|
269次组卷
|
2卷引用:天津市第一中学2023-2024学年高一上学期期末考试化学试卷
名校
10 . 化合物G是一种治疗中度高血压药物的中间体,其一种合成路线如图所示(部分反应条件已略去):
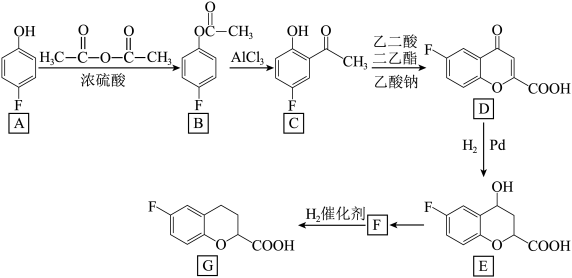
(1)A的名称为___________ ,由A生成B的反应类型为___________ 。
(2)C中含氧官能团的名称为___________ ,写出乙二酸二乙酯的结构简式:___________ 。
(3)B分子中共面原子数最多为___________ 个。
(4)由E生成F反应化学方程式为___________ 。
(5)能与NaHCO3溶液反应生成CO2,且属于芳香化合物的C的同分异构体有___________ 种
(不含立体异构),其中核磁共振氢谱中只有4组峰的结构简式为___________ 。
(6)参照上述合成路线,写出以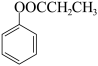 为原料制备
为原料制备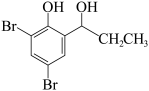 的合成路线:
的合成路线:________ (其他无机试剂任选)。

(1)A的名称为
(2)C中含氧官能团的名称为
(3)B分子中共面原子数最多为
(4)由E生成F反应化学方程式为
(5)能与NaHCO3溶液反应生成CO2,且属于芳香化合物的C的同分异构体有
(不含立体异构),其中核磁共振氢谱中只有4组峰的结构简式为
(6)参照上述合成路线,写出以
 为原料制备
为原料制备 的合成路线:
的合成路线:
您最近一年使用:0次



