1 . 丙烯是一种重要的化工原料。可在一固定容积的密闭容器中由丙烷催化脱氢制备。
(1)已知: ①C3H8(g)=C3H6(g)+H2(g) _______。
_______。
②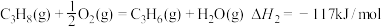
③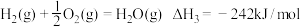
反应①的
___________ 。
(2)欲提高①反应中 的平衡转化率,可采取的措施有___________(填标号)。
的平衡转化率,可采取的措施有___________(填标号)。
(3)能表明该反应①达到平衡状态的是___________(填字母)。
(4)某温度下,在体积不变的密闭容器内发生反应①,起始总压强为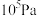 ,平衡时总压增加了20%。则达到平衡时,
,平衡时总压增加了20%。则达到平衡时, 的转化率为
的转化率为___________ 。该反应的平衡常数
___________ Pa.(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。写出该反应的化学平衡常数表达式:K=___________ ;保持恒温恒容,将反应的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡___________ (填“正向”逆向”或“不”)移动,平衡常数K___________ (填“变大”变小”或“不变”)。
(1)已知: ①C3H8(g)=C3H6(g)+H2(g)
 _______。
_______。②
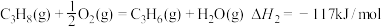
③
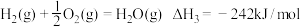
反应①的

(2)欲提高①反应中
 的平衡转化率,可采取的措施有___________(填标号)。
的平衡转化率,可采取的措施有___________(填标号)。A.增大 的浓度 的浓度 | B.提高温度 | C.恒容下通入惰性气体 | D.使用高效催化剂 |
| A.C3H8的转化率等于H2的产率 | B.混合气体的平均相对分子质量不变 |
C.v(C3H8)与 的比值不变 的比值不变 | D.混合气体的密度不变 |
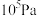 ,平衡时总压增加了20%。则达到平衡时,
,平衡时总压增加了20%。则达到平衡时, 的转化率为
的转化率为
(5)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。写出该反应的化学平衡常数表达式:K=
您最近一年使用:0次
解题方法
2 . 下列根据实验操作和现象所得出的结论正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 向酸性KMnO4溶液中通入SO2 | 溶液紫红色褪去 | SO2具有漂白性 |
| B | 在镁、铝为电极,氢氧化钠为电解质的原电池装置 | 镁表面有气泡 | 金属活动性:Al>Mg |
| C | 测定等物质的量浓度的NaCl与Na2CO3溶液的pH | 后者较大 | 非金属性:Cl>C |
| D | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-06-01更新
|
781次组卷
|
3卷引用:广西防城港市防城中学2020届高三上学期10月月考化学试题
名校
3 . 反应物和生成物均为气态的平衡体系,平衡常数表达式为:K= 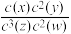 ,有关该平衡体系说法
,有关该平衡体系说法不正确 的是
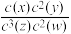 ,有关该平衡体系说法
,有关该平衡体系说法| A.升温温度,该反应平衡常数K一定发生改变 |
| B.增大压强,w的质量分数减小 |
C.该反应的化学方程式为:3z(g)+2w(g)  x(g)+2y(g) x(g)+2y(g) |
| D.增大x气体浓度平衡向正反应方向移动 |
您最近一年使用:0次
2017-10-17更新
|
379次组卷
|
3卷引用:广西防城港市实验高级中学2023-2024学年高二上学期期中考试化学试题
4 . 选择下列实验方法分离物质,将分离方法的字母序号填在横线上。
A过滤法 B分液法 C蒸馏法 D结晶法 E萃取法 F 蒸发
(1)___________ 分离水和豆油的混合物;
(2)___________ 从含有硝酸钾和少量氯化钾的混合溶液中获得硝酸钾;
(3)___________ 分离饱和食盐水和沙子的混合物;
(4)____________ 分离酒精和水的混合物。
A过滤法 B分液法 C蒸馏法 D结晶法 E萃取法 F 蒸发
(1)
(2)
(3)
(4)
您最近一年使用:0次
2016-12-09更新
|
226次组卷
|
2卷引用:广西防城港市2020—2021学年高一上学期期中测试化学试题



