名校
1 . 二甲醚( )是一种洁净液体燃料,工业上以CO和
)是一种洁净液体燃料,工业上以CO和 为原料生产
为原料生产 。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
进行下列反应:
反应ⅰ:
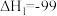 kJ⋅mol
kJ⋅mol
反应ⅱ:
 kJ⋅mol
kJ⋅mol
反应ⅲ:
 kJ⋅mol
kJ⋅mol
(1)在该条件下,若反应i的起始浓度分别为 mol⋅L
mol⋅L ,
, mol⋅L
mol⋅L ,8 min后达到化学平衡状态,CO的转化率为50%,则8 min内CO的平均反应速率为
,8 min后达到化学平衡状态,CO的转化率为50%,则8 min内CO的平均反应速率为_______
(2)在t℃时。反应ⅱ的平衡常数为400,此温度下,在1 L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
此时
_______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(3)催化总反应为: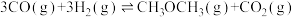

①
_______ kJ⋅mol
②CO的平衡转化率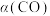 与温度、压强的关系如图所示。图中X代表
与温度、压强的关系如图所示。图中X代表_______ (填“温度”或“压强”)。 。回答下列问题:
。回答下列问题:
①用各物质的平衡浓度表示该反应的平衡常数表达式
_______ 。
②下列有关上述可逆反应的说法正确的是_______ 。
A.断裂 个
个 同时断裂
同时断裂 个
个 键,说明该可逆反应达到平衡
键,说明该可逆反应达到平衡
B.混合气体的平均密度不再改变,说明该可逆反应达到平衡
C.在该容器中充入一定量的氢气,平衡不移动
D.在该容器中充入 ,平衡常数K增大
,平衡常数K增大
E.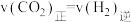 ,说明该可逆反应达到平衡
,说明该可逆反应达到平衡
F.该反应在低温下能自发进行
 )是一种洁净液体燃料,工业上以CO和
)是一种洁净液体燃料,工业上以CO和 为原料生产
为原料生产 。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)进行下列反应:
反应ⅰ:

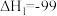 kJ⋅mol
kJ⋅mol
反应ⅱ:

 kJ⋅mol
kJ⋅mol
反应ⅲ:

 kJ⋅mol
kJ⋅mol
(1)在该条件下,若反应i的起始浓度分别为
 mol⋅L
mol⋅L ,
, mol⋅L
mol⋅L ,8 min后达到化学平衡状态,CO的转化率为50%,则8 min内CO的平均反应速率为
,8 min后达到化学平衡状态,CO的转化率为50%,则8 min内CO的平均反应速率为(2)在t℃时。反应ⅱ的平衡常数为400,此温度下,在1 L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 |  |  |  |
c/(mol·L ) ) | 0.05 | 2.0 | 2.0 |

 (填“>”“<”或“=”)
(填“>”“<”或“=”)(3)催化总反应为:
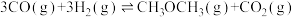

①


②CO的平衡转化率
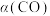 与温度、压强的关系如图所示。图中X代表
与温度、压强的关系如图所示。图中X代表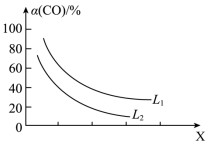
 。回答下列问题:
。回答下列问题:①用各物质的平衡浓度表示该反应的平衡常数表达式

②下列有关上述可逆反应的说法正确的是
A.断裂
 个
个 同时断裂
同时断裂 个
个 键,说明该可逆反应达到平衡
键,说明该可逆反应达到平衡B.混合气体的平均密度不再改变,说明该可逆反应达到平衡
C.在该容器中充入一定量的氢气,平衡不移动
D.在该容器中充入
 ,平衡常数K增大
,平衡常数K增大E.
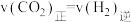 ,说明该可逆反应达到平衡
,说明该可逆反应达到平衡F.该反应在低温下能自发进行
您最近一年使用:0次
名校
解题方法
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.含有7.8 g 的溶液中: 的溶液中: 的数目为 的数目为 |
B.1 L 1 mol⋅L 溴化铵水溶液中 溴化铵水溶液中 与 与 离子数之和大于 离子数之和大于 |
C.标准状况下,11.2 L  含有 含有 键的数目为 键的数目为 |
D.常温下,1 L  的 的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近一年使用:0次
2024-05-02更新
|
67次组卷
|
2卷引用:广西防城港市实验高级中学2023-2024学年高二下学期期中考试化学试题
名校
3 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”,根据图示回答下列问题:___________ 。
(2)足量B通入品红溶液中,溶液褪色,体现了B的___________ 性;足量B通入溴水,溶液褪色,体现了B的___________ 性;足量B通入氢硫酸溶液,有淡黄色的固体生成,体现了B的___________ 性。
(3)气体A和B,不能用D的浓溶液干燥的气体是___________ (填A或B化学式),它与D的浓溶液反应有淡黄色的固体生成,请写出该反应的化学方程式___________ 。
(4)要实现 的转化,可选用下列试剂中的___________(填字母)。
的转化,可选用下列试剂中的___________(填字母)。
(5) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的方法
溶液是否变质的方法___________ 。

(2)足量B通入品红溶液中,溶液褪色,体现了B的
(3)气体A和B,不能用D的浓溶液干燥的气体是
(4)要实现
 的转化,可选用下列试剂中的___________(填字母)。
的转化,可选用下列试剂中的___________(填字母)。A. | B. | C. | D. |
(5)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的方法
溶液是否变质的方法
您最近一年使用:0次
名校
解题方法
4 . 请完成下列问题:
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是___________ (填序号)。
①碳酸钙高温分解 ②生石灰和水的反应 ③ 在
在 中燃烧
中燃烧
(2)如图是原电池的装置图。请回答下列问题:___________ (填“正极”或“负极”),发生___________ 反应(填“氧化”或“还原”);电子由___________ 片通过导线流向___________ 片。(均填化学式)
②溶液中的 向
向___________ 片移动。(填化学式)
③Cu片上发生反应的电极反应式为___________ 。
④若Fe电极消耗5.6g,则外电路转移___________  。
。
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是
①碳酸钙高温分解 ②生石灰和水的反应 ③
 在
在 中燃烧
中燃烧(2)如图是原电池的装置图。请回答下列问题:
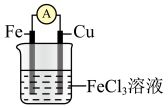
②溶液中的
 向
向③Cu片上发生反应的电极反应式为
④若Fe电极消耗5.6g,则外电路转移
 。
。
您最近一年使用:0次
名校
5 . 氮是自然界中生物体生命活动不可缺少的重要元素,其化合物种类丰富。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题: 的电子式为
的电子式为___________ 。
(2)试管内发生反应的化学方程式为___________ 。
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是___________ 。
②一段时间后, 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为___________ 。
③为提高乙装置中实验的成功率,将盛放有___________ 的干燥管连接在甲、乙装置之间。
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。___________ (填“ⅰ”“ⅱ”或“ⅲ”)。
(5)写出“氧化炉”中反应的化学方程式___________ 。
(6)“吸收塔”排出的尾气中会含有NO、 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整:______ 。
 ___________
___________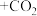 。
。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题:
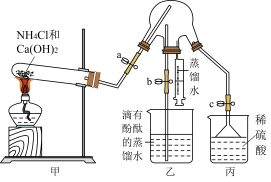
 的电子式为
的电子式为(2)试管内发生反应的化学方程式为
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是
②一段时间后,
 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为③为提高乙装置中实验的成功率,将盛放有
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。
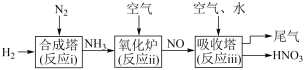
(5)写出“氧化炉”中反应的化学方程式
(6)“吸收塔”排出的尾气中会含有NO、
 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整: ___________
___________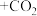 。
。
您最近一年使用:0次
6 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________ 、___________ 和玻璃。
(2)光导纤维的主要成分是 。
。 为
为___________ (“酸性”、“碱性”或“两性”)氧化物,写出 与烧碱反应的化学方程式
与烧碱反应的化学方程式___________ 。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:___________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式___________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是___________ 。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)光导纤维的主要成分是
 。
。 为
为 与烧碱反应的化学方程式
与烧碱反应的化学方程式(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成
 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是
您最近一年使用:0次
名校
7 . 已知化学反应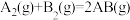 的能量变化如图所示,判断下列叙述中正确的是
的能量变化如图所示,判断下列叙述中正确的是
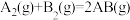 的能量变化如图所示,判断下列叙述中正确的是
的能量变化如图所示,判断下列叙述中正确的是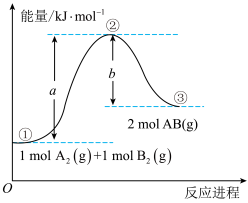
A.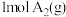 和 和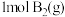 反应生成 反应生成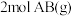 吸收的热量为(a-b)kJ 吸收的热量为(a-b)kJ |
| B.①→②→③的过程中有非极性键的断裂和形成 |
| C.该反应是放热反应 |
| D.该反应中反应物的总能量高于生成物的总能量 |
您最近一年使用:0次
名校
8 . 短周期主族元素W、X、Y和Z的原子序数依次增大,W原子是半径最小的原子,X原子的最外层电子数是内层电子数的3倍,元素Y是应用广泛的半导体材料,元素Z与X同主族。下列说法正确的是
| A.X、Y两种元素形成的化合物一定是共价化合物 |
| B.原子半径:Z>Y>X>W |
| C.最高价氧化物对应的水化物酸性:Y>Z |
| D.氢化物稳定性:X<Z |
您最近一年使用:0次
名校
解题方法
9 . 对下列现象或事实的解释正确的是
| 选项 | 实验现象或化学事实 | 解释 |
| A | 向某溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中一定含有 |
| B | 常温下,Fe、Al放入浓 或浓 或浓 中无明显现象 中无明显现象 | 常温下Fe、Al与浓 或浓 或浓 不反应 不反应 |
| C | 蔗糖中加入浓硫酸,蔗糖逐渐变黑并有刺激性气味的气体产生 | 浓硫酸具有脱水性和氧化性 |
| D |  通入 通入 溶液中,再滴入 溶液中,再滴入 溶液产生白色沉淀 溶液产生白色沉淀 | 白色沉淀为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列离子方程式书写正确的是
A.锌与稀硝酸反应: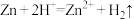 |
B. 溶液与 溶液与 溶液混合加热: 溶液混合加热: |
C.向 溶液中滴加氨水: 溶液中滴加氨水: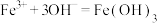 |
D.过量 气体通入氢氧化钠溶液中: 气体通入氢氧化钠溶液中: |
您最近一年使用:0次



