名校
解题方法
1 . 请完成下列问题:
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是___________ (填序号)。
①碳酸钙高温分解 ②生石灰和水的反应 ③ 在
在 中燃烧
中燃烧
(2)如图是原电池的装置图。请回答下列问题:___________ (填“正极”或“负极”),发生___________ 反应(填“氧化”或“还原”);电子由___________ 片通过导线流向___________ 片。(均填化学式)
②溶液中的 向
向___________ 片移动。(填化学式)
③Cu片上发生反应的电极反应式为___________ 。
④若Fe电极消耗5.6g,则外电路转移___________  。
。
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是
①碳酸钙高温分解 ②生石灰和水的反应 ③
 在
在 中燃烧
中燃烧(2)如图是原电池的装置图。请回答下列问题:
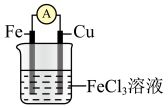
②溶液中的
 向
向③Cu片上发生反应的电极反应式为
④若Fe电极消耗5.6g,则外电路转移
 。
。
您最近一年使用:0次
2 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________ 、___________ 和玻璃。
(2)光导纤维的主要成分是 。
。 为
为___________ (“酸性”、“碱性”或“两性”)氧化物,写出 与烧碱反应的化学方程式
与烧碱反应的化学方程式___________ 。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:___________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式___________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是___________ 。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)光导纤维的主要成分是
 。
。 为
为 与烧碱反应的化学方程式
与烧碱反应的化学方程式(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是______(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成
 、
、 和一种气体单质,写出发生反应的化学方程式
和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是
您最近一年使用:0次
名校
解题方法
3 . 材料与生活、生产息息相关,目前使用的材料主要有:金属材料、传统无机非金属材料、新型无机非金属材料、高分子材料、复合材料等。
(1)硅酸盐材料是重要的传统无机非金属材料,也是日常生活、交通工具、建筑行业等不可缺少的材料之一、下列不属于传统硅酸盐产品的是___________ (填写序号)。
①光导纤维 ②水泥 ③玻璃 ④陶瓷
(2)玻璃是重要的建筑和装饰材料,玻璃属于___________ (填“纯净物”或“混合物”)。雕花玻璃的花纹是利用氢氟酸对普通玻璃中的二氧化硅的腐蚀作用而制成的,写出该反应的化学方程式___________ 。
(3)氮化硅是一种高温陶瓷材料,它的硬度大、熔点高,化学性质稳定。工业上普遍采用高纯硅与纯氮在1300℃反应获得氮化硅,该反应属于化学反应基本类型中的___________ 反应;已知氮化硅中硅元素的化合价为+4价,则氮化硅的化学式为___________ 。
(1)硅酸盐材料是重要的传统无机非金属材料,也是日常生活、交通工具、建筑行业等不可缺少的材料之一、下列不属于传统硅酸盐产品的是
①光导纤维 ②水泥 ③玻璃 ④陶瓷
(2)玻璃是重要的建筑和装饰材料,玻璃属于
(3)氮化硅是一种高温陶瓷材料,它的硬度大、熔点高,化学性质稳定。工业上普遍采用高纯硅与纯氮在1300℃反应获得氮化硅,该反应属于化学反应基本类型中的
您最近一年使用:0次
名校
解题方法
4 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)锌铜原电池装置示意图如图1,Zn片作___________ (填“正极”或“负极”)。
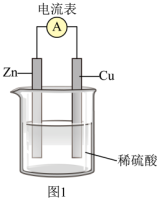
(2)Cu片上发生反应的电极反应式为___________ ,Zn片上的电极反应式为___________
(3)电流表指针偏转,说明该装置实现了化学能向___________ 的转化。
(4)某锂-空气电池的总反应为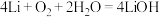 ,其工作原理示意图如图2。
,其工作原理示意图如图2。
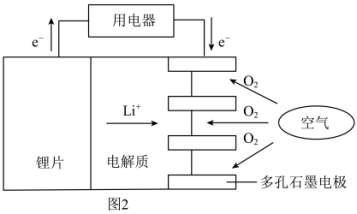
下列说法正确的是___________ (填字母)。
a.锂片作负极 b. 发生还原反应
发生还原反应
(1)锌铜原电池装置示意图如图1,Zn片作

(2)Cu片上发生反应的电极反应式为
(3)电流表指针偏转,说明该装置实现了化学能向
(4)某锂-空气电池的总反应为
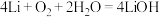 ,其工作原理示意图如图2。
,其工作原理示意图如图2。
下列说法正确的是
a.锂片作负极 b.
 发生还原反应
发生还原反应
您最近一年使用:0次
2023-04-29更新
|
145次组卷
|
2卷引用:广西防城港市实验高级中学2022-2023学年高一下学期期中考试化学试题
解题方法
5 . t℃时,将3molA和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g)⇌xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余0.8molB,并测得C的浓度为0.4mol·L-1,请填写下列空白:
(1)从开始反应至达到平衡状态,B的平均反应速率为_______ ,A的平衡浓度为_______ mol/L。
(2)x=_______ ,平衡常数K=_______ 。(列出计算式不用计算出结果)
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)_______ 。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(1)从开始反应至达到平衡状态,B的平均反应速率为
(2)x=
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
您最近一年使用:0次
解题方法
6 . 写出下列燃烧热的热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式______ 。
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式___________ 。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式
您最近一年使用:0次
解题方法
7 . 根据事实,写出下列反应的热化学方程式。
(1)28gN2(g)与适量的O2(g)反应,生成NO2(g),吸收68kJ热量________ 。
(2)2molAl(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8kJ热量__________ 。
(1)28gN2(g)与适量的O2(g)反应,生成NO2(g),吸收68kJ热量
(2)2molAl(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8kJ热量
您最近一年使用:0次
8 . 某实验小组同学进行如图1实验,以检验化学反应中的能量变化。
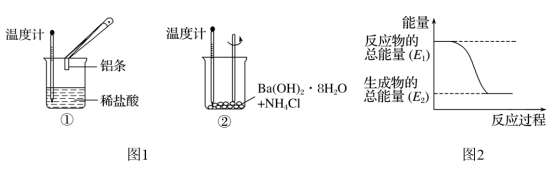
请回答下列问题:
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是__ 热反应,Ba(OH)2·8H2O与NH4Cl的反应是_ 热反应。反应过程_ (填“①”或“②”)的能量变化可用图2表示。
(2)一定量的氢气在氧气中充分燃烧并放出热量。若生成气态水放出的热量为Q1;生成液态水放出的热量为Q2,那么Q1_______ Q2(填“大于”“小于”或“等于”)。

请回答下列问题:
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
(2)一定量的氢气在氧气中充分燃烧并放出热量。若生成气态水放出的热量为Q1;生成液态水放出的热量为Q2,那么Q1
您最近一年使用:0次
9 . 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示装置。
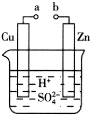
(1)a和b不连接时,烧杯中现象是_______ 。
(2)a和b用导线连接,Cu极为原电池___ (“正”或“负”)极,电极反应式为___ ;溶液中H+移向__ (填“Cu”或“Zn”)极。
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为_____ 。

(1)a和b不连接时,烧杯中现象是
(2)a和b用导线连接,Cu极为原电池
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为
您最近一年使用:0次
解题方法
10 . 某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图。依图回答:
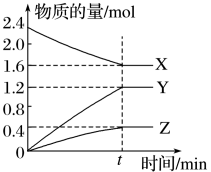
(1)该反应的化学方程式可表示为_______ 。
(2)反应起始至tmin(设t=5),Y的平均反应速率是_______ 。
(3)在tmin时,该反应达到了_______ 状态,下列可判断反应已达到该状态的是_______ (填字母)。
A. X、Y、Z的反应速率相等
B. X、Y的反应速率比为2:3
C. 混合气体的密度不变
D. 生成1molZ的同时生成2molX
E. X、Y、Z物质的量之比等于系数比
F. 混合气体的总压强不再发生改变

(1)该反应的化学方程式可表示为
(2)反应起始至tmin(设t=5),Y的平均反应速率是
(3)在tmin时,该反应达到了
A. X、Y、Z的反应速率相等
B. X、Y的反应速率比为2:3
C. 混合气体的密度不变
D. 生成1molZ的同时生成2molX
E. X、Y、Z物质的量之比等于系数比
F. 混合气体的总压强不再发生改变
您最近一年使用:0次



