1 . 某学校兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
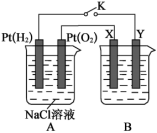
(1)通 的
的 电极为
电极为___________ 极(填电极名称),其电极反应式为___________ 。
(2)若B电池为电镀池,X、Y为质量相同的不含杂质的两电极,电解质溶液为 溶液,目的是在某铁镀件上镀一层铜,则X电极材料为
溶液,目的是在某铁镀件上镀一层铜,则X电极材料为___________ ,Y电极的反应式为___________ 。若A池中消耗准状况下 的
的 ,则B池中两电极的质量相差
,则B池中两电极的质量相差___________ g。
(3)若B电池为精炼铜,且粗铜中含有 、
、 、
、 、
、 等杂质,在
等杂质,在___________ 。电极(填“X”或“Y”)周围有固体沉积。
(4)若X、Y均为 电池的电解质溶液为
电池的电解质溶液为 的
的 溶液,当电池工作一段时间后,B电池溶液的
溶液,当电池工作一段时间后,B电池溶液的 将
将___________ (填“增大”“减小”或“不变”),要使该溶液恢复到原来的状态,需加入___________ 。
(5)若X、Y均是铜,电解质溶液为 溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是
溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是 ,试写出该电极发生的电极反应式为
,试写出该电极发生的电极反应式为___________ 。

(1)通
 的
的 电极为
电极为(2)若B电池为电镀池,X、Y为质量相同的不含杂质的两电极,电解质溶液为
 溶液,目的是在某铁镀件上镀一层铜,则X电极材料为
溶液,目的是在某铁镀件上镀一层铜,则X电极材料为 的
的 ,则B池中两电极的质量相差
,则B池中两电极的质量相差(3)若B电池为精炼铜,且粗铜中含有
 、
、 、
、 、
、 等杂质,在
等杂质,在(4)若X、Y均为
 电池的电解质溶液为
电池的电解质溶液为 的
的 溶液,当电池工作一段时间后,B电池溶液的
溶液,当电池工作一段时间后,B电池溶液的 将
将(5)若X、Y均是铜,电解质溶液为
 溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是
溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是 ,试写出该电极发生的电极反应式为
,试写出该电极发生的电极反应式为
您最近一年使用:0次
2 . 已知:①

②
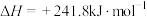
③
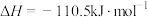
④
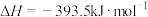
回答下列问题:
(1)上述变化中属于吸热反应的是___________ (填序号)。
(2)写出 燃烧的热化学方程式:
燃烧的热化学方程式:___________ 。
(3)反应 的
的
___________  。
。
(4)相同压强下,质量相等且起始温度相同的两份 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量___________ (填“>”“<”或“=”)反应Ⅱ放出的热量。
(5)在一定条件下,将 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
___________  。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:___________ 。
(6)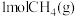 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:________ 。



②

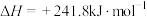
③

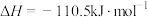
④

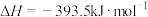
回答下列问题:
(1)上述变化中属于吸热反应的是
(2)写出
 燃烧的热化学方程式:
燃烧的热化学方程式:(3)反应
 的
的
 。
。(4)相同压强下,质量相等且起始温度相同的两份
 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量(5)在一定条件下,将
 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
 。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:(6)
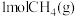 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:
您最近一年使用:0次
名校
3 . 学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: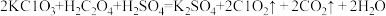 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
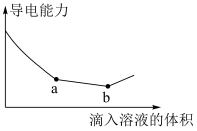
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
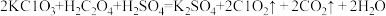 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
您最近一年使用:0次
2024-01-28更新
|
111次组卷
|
4卷引用:广西北海市2023-2024学年高一上学期期末考试化学试题
4 . 根据所学习的元素周期表的相关知识,回答下列问题:
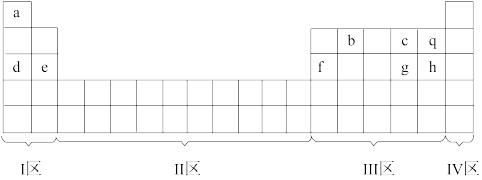
(1)在上面元素周期表中,全部是金属元素的区域为___________(填字母)。
(2)写出a~h中,金属性最强的元素的原子结构示意图:___________ 。
(3)已知某粒子的结构示意图为 ,试回答:
,试回答:
当 ,
, 时,该粒子为
时,该粒子为___________ (填“原子”“阳离子”或“阴离子”),该元素为周期表中的___________ (填上面表格中标注的字母)。
(4)d元素与c元素形成的化合物中可用作呼吸面具内的供氧剂的是___________ (填化学式),它与 反应的化学方程式是
反应的化学方程式是___________ 。
(5)q、h元素对应单质与氢气反应的剧烈程度:___________ >___________ (写出元素对应单质的化学式)。

(1)在上面元素周期表中,全部是金属元素的区域为___________(填字母)。
| A.Ⅰ区 | B.Ⅱ区 | C.Ⅲ区 | D.Ⅳ区 |
(3)已知某粒子的结构示意图为
 ,试回答:
,试回答:当
 ,
, 时,该粒子为
时,该粒子为(4)d元素与c元素形成的化合物中可用作呼吸面具内的供氧剂的是
 反应的化学方程式是
反应的化学方程式是(5)q、h元素对应单质与氢气反应的剧烈程度:
您最近一年使用:0次
5 . 现有以下物质:① 溶液;②熔融
溶液;②熔融 ;③氯化氢;④熔融
;③氯化氢;④熔融 ;⑤
;⑤ 固体;⑥
固体;⑥ ;⑦
;⑦ (胶体);⑧饱和
(胶体);⑧饱和 溶液;⑨乙醇;⑩
溶液;⑨乙醇;⑩ 。
。
回答下列问题:
(1)属于非电解质的是___________ (填序号,下同),能导电的电解质是___________ 。
(2)写出④的电离方程式:___________ 。
(3)写出 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(4)向盐酸中逐滴滴加等浓度的氢氧化钠溶液,溶液的导电能力变化情况为___________ 。
(5)写出用 溶液作为“腐蚀液”腐蚀⑩的离子方程式:
溶液作为“腐蚀液”腐蚀⑩的离子方程式:___________ 。
 溶液;②熔融
溶液;②熔融 ;③氯化氢;④熔融
;③氯化氢;④熔融 ;⑤
;⑤ 固体;⑥
固体;⑥ ;⑦
;⑦ (胶体);⑧饱和
(胶体);⑧饱和 溶液;⑨乙醇;⑩
溶液;⑨乙醇;⑩ 。
。回答下列问题:
(1)属于非电解质的是
(2)写出④的电离方程式:
(3)写出
 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:(4)向盐酸中逐滴滴加等浓度的氢氧化钠溶液,溶液的导电能力变化情况为
(5)写出用
 溶液作为“腐蚀液”腐蚀⑩的离子方程式:
溶液作为“腐蚀液”腐蚀⑩的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 铁及其化合物与生产、生活息息相关。回答下列问题:
(1) 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是_______ 。
(2)印刷电路板的制作原理是用足量的 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:_______ 。
(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用 将其还原的化学方程式为
将其还原的化学方程式为_______ 。
(4)某废料铁泥的主要成分为 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:

①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、_______ 、_______ 。
②能检验溶液A中含有 的试剂是
的试剂是_______ (填字母)。
A.铁粉 B.酸性 溶液 C.KSCN溶液
溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为_______ 。
④若最终获得 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为_______ 。
(1)
 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是(2)印刷电路板的制作原理是用足量的
 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用
 将其还原的化学方程式为
将其还原的化学方程式为(4)某废料铁泥的主要成分为
 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、
②能检验溶液A中含有
 的试剂是
的试剂是A.铁粉 B.酸性
 溶液 C.KSCN溶液
溶液 C.KSCN溶液③步骤Ⅱ中发生反应的离子方程式为
④若最终获得
 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次
2023-01-20更新
|
525次组卷
|
7卷引用:广西北海市2023-2024学年高一上学期期末考试化学试题
名校
解题方法
7 . 我国提出争取在2030年前实现碳达峰、2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。回答下列问题:
Ⅰ.如图所示电解装置可将CO2转化为乙烯(C2H4),该装置中的电解质溶液为稀硫酸,电极材料均为惰性电极。

(1)电极b是_______ (填“阴极”或“阳极”),电极a上发生的电极反应式是_______ 。
(2)电解过程中H+运动方向为_______ (填“由a到b”或“由b到a”)。电解后,溶液中n(H+)_______ (填“增大”“减小”或“不变”)。
Ⅱ.实验室用CH4燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。

(3)甲装置中,负极的电极反应式为_______ 。
(4)乙装置中,石墨(C)极的电极反应式为_______ 。
(5)若在标准状况下,有1.12L氧气参加反应,则理论上通过乙装置中X交换膜的电量为_______ C(已知:法拉第常数代表每摩尔电子所携带的电荷,数值F=9.65×104C·mol−1)。一段时间后,丙装置中c(Cu2+)_______ (填“增大”“减小”或“不变”)。
(6)若以该CH4燃料电池为电源,用石墨作电极电解200mL0.5mol·L-1的CuSO4溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是_______ 。
Ⅰ.如图所示电解装置可将CO2转化为乙烯(C2H4),该装置中的电解质溶液为稀硫酸,电极材料均为惰性电极。

(1)电极b是
(2)电解过程中H+运动方向为
Ⅱ.实验室用CH4燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。

(3)甲装置中,负极的电极反应式为
(4)乙装置中,石墨(C)极的电极反应式为
(5)若在标准状况下,有1.12L氧气参加反应,则理论上通过乙装置中X交换膜的电量为
(6)若以该CH4燃料电池为电源,用石墨作电极电解200mL0.5mol·L-1的CuSO4溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是
您最近一年使用:0次
2022-12-13更新
|
214次组卷
|
2卷引用:广西北海市2022-2023学年高二上学期期末考试化学试题
解题方法
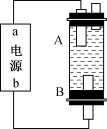
8 . 某兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜的精炼原理,如图所示,其中乙装置中 为阳离子交换膜。请按要求回答相关问题:
为阳离子交换膜。请按要求回答相关问题:

(1)甲中通入氧气的电极是___________ 极(填“正”或“负”),通甲烷气体的电极反应式是___________ 。
(2)乙装置中电解的总离子方程式为___________ ,阴极产物为___________ 。
(3)若在标准状况下,有 氧气参加反应,则丙装置中阴极析出铜的质量为
氧气参加反应,则丙装置中阴极析出铜的质量为___________  。
。
(4)某同学利用铅蓄电池设计电解法制取漂白液的实验装置如图所示,a为电池的___________ 极。写出 与
与 反应生成漂白液的离子方程式:
反应生成漂白液的离子方程式:___________ 。
 为阳离子交换膜。请按要求回答相关问题:
为阳离子交换膜。请按要求回答相关问题:
(1)甲中通入氧气的电极是
(2)乙装置中电解的总离子方程式为
(3)若在标准状况下,有
 氧气参加反应,则丙装置中阴极析出铜的质量为
氧气参加反应,则丙装置中阴极析出铜的质量为 。
。(4)某同学利用铅蓄电池设计电解法制取漂白液的实验装置如图所示,a为电池的
 与
与 反应生成漂白液的离子方程式:
反应生成漂白液的离子方程式:
您最近一年使用:0次
解题方法
9 . 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)下列变化过程,属于放热反应的是___________ (填序号)。
① 水解反应 ②酸碱中和反应 ③
水解反应 ②酸碱中和反应 ③ 在
在 中燃烧 ④固体
中燃烧 ④固体 溶于水 ⑤液态水变成水蒸气 ⑥碳高温条件下还原
溶于水 ⑤液态水变成水蒸气 ⑥碳高温条件下还原 ⑦浓硫酸稀释
⑦浓硫酸稀释
(2)实验测得,标准状况下 甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出
甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出 的热量,试写出表示甲烷燃烧热的热化学方程式:
的热量,试写出表示甲烷燃烧热的热化学方程式:___________ 。
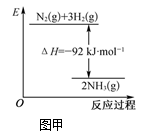
(3)已知反应 ,该反应过程中的能量变化如图甲,化学键键能如下表所示,通过计算可得
,该反应过程中的能量变化如图甲,化学键键能如下表所示,通过计算可得
___________ 。
(4)锂催化非水相氮还原合成氨的反应机理如图乙所示,各步 如下表所示:
如下表所示:
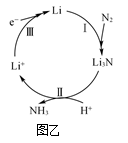
①反应机理图可知,反应中第___________ (填“I”“II”或“III”)步完成后,能自发完成后续反应。
②第II步反应的离子方程式为___________ 。
(1)下列变化过程,属于放热反应的是
①
 水解反应 ②酸碱中和反应 ③
水解反应 ②酸碱中和反应 ③ 在
在 中燃烧 ④固体
中燃烧 ④固体 溶于水 ⑤液态水变成水蒸气 ⑥碳高温条件下还原
溶于水 ⑤液态水变成水蒸气 ⑥碳高温条件下还原 ⑦浓硫酸稀释
⑦浓硫酸稀释(2)实验测得,标准状况下
 甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出
甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出 的热量,试写出表示甲烷燃烧热的热化学方程式:
的热量,试写出表示甲烷燃烧热的热化学方程式:(3)已知反应
 ,该反应过程中的能量变化如图甲,化学键键能如下表所示,通过计算可得
,该反应过程中的能量变化如图甲,化学键键能如下表所示,通过计算可得

| 化学键 |  |  |  |
键能/ |  | 391 | 436 |
(4)锂催化非水相氮还原合成氨的反应机理如图乙所示,各步
 如下表所示:
如下表所示:
| 步骤 | I | II | III |
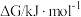 | 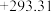 | 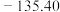 |  |
①反应机理图可知,反应中第
②第II步反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 原电池是化学对人类的一项重大贡献。如图为原电池装置示意图。
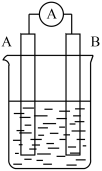
(1)若A为铜,B为锌,电解质溶液为稀硫酸。A和B不连接时,装置中发生反应的离子方程式是_______ 。
(2)若A为铝,B为铜,电解质溶液为 ,用导线相连,则负极为
,用导线相连,则负极为_______ (填“铝”或“铜”),若将装置中 溶液换为氢氧化钠溶液,请写出装置中负极的电极反应式:
溶液换为氢氧化钠溶液,请写出装置中负极的电极反应式:_______ 。
(3)若A为 ,B为
,B为 ,电解质溶液为稀硫酸,工作时的总反应为
,电解质溶液为稀硫酸,工作时的总反应为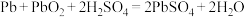 。写出B电极反应式:
。写出B电极反应式:_______ ;该电池在工作时,A电极的质量将_______ (填“增大”“减小”或“不变”)。

(1)若A为铜,B为锌,电解质溶液为稀硫酸。A和B不连接时,装置中发生反应的离子方程式是
(2)若A为铝,B为铜,电解质溶液为
 ,用导线相连,则负极为
,用导线相连,则负极为 溶液换为氢氧化钠溶液,请写出装置中负极的电极反应式:
溶液换为氢氧化钠溶液,请写出装置中负极的电极反应式:(3)若A为
 ,B为
,B为 ,电解质溶液为稀硫酸,工作时的总反应为
,电解质溶液为稀硫酸,工作时的总反应为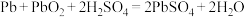 。写出B电极反应式:
。写出B电极反应式:
您最近一年使用:0次
2022-07-16更新
|
192次组卷
|
2卷引用:广西北海市2021-2022学年高一下学期期末检测化学试题



