名校
1 . 根据要求,回答下列问题:
(1)已知甲烷的燃烧热为 ,
,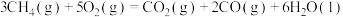
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式:_______ ,若 、
、 键的键能分别为
键的键能分别为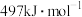 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是_______ ;1mol 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是_______ (保留1位小数)。
(2)煤的气化反应之一为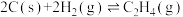

已知:①

②
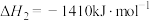
③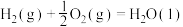

则上述煤的生成 的气化反应的
的气化反应的
_______ 。实际生产中该气化反应需要加入催化剂,其主要原因是_______ (填“速率问题”或“平衡问题”)。
(1)已知甲烷的燃烧热为
 ,
,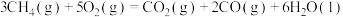
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式: 、
、 键的键能分别为
键的键能分别为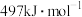 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是(2)煤的气化反应之一为
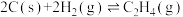

已知:①


②

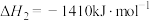
③
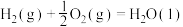

则上述煤的生成
 的气化反应的
的气化反应的
您最近一年使用:0次
2022-12-13更新
|
210次组卷
|
2卷引用:广西北海市2022-2023学年高二上学期期末考试化学试题
2 . 化学计量在化学中占有重要地位。回答下列问题:
(1)含有1 mol O的Fe3O4中,含有___________ mol Fe。
(2)溶质质量为29.4 g的硫酸溶液中含有___________ mol H+。
(3)标准状况下6. 72 L NH3分子中所含原子数与___________ g H2O所含原子数相等。
(4)0.5L1mol·L-1FeCl3溶液与0.2L1mol·L-1KCl溶液中的Cl-的数目之比为___________ 。
(5)在过氧化钠与水的反应中,每生成0.1 mol 氧气,转移电子的数目约为___________ 。
(6)用MnO2和浓盐酸制取氯气,当4 mol 氯化氢被氧化时,生成的氯气的体积(标况)是___________ 。
(1)含有1 mol O的Fe3O4中,含有
(2)溶质质量为29.4 g的硫酸溶液中含有
(3)标准状况下6. 72 L NH3分子中所含原子数与
(4)0.5L1mol·L-1FeCl3溶液与0.2L1mol·L-1KCl溶液中的Cl-的数目之比为
(5)在过氧化钠与水的反应中,每生成0.1 mol 氧气,转移电子的数目约为
(6)用MnO2和浓盐酸制取氯气,当4 mol 氯化氢被氧化时,生成的氯气的体积(标况)是
您最近一年使用:0次
名校
3 . 化学科学家采用丙烯歧化法制取乙烯和丁烯的反应原理为2C3H6(g) C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:
(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
①a=_______ ,p初始:p5min=_______ 。
②其他条件不变,若缩小反应器的体积,则C3H6转化率_______ (填“增大”“减小”或“不变”)。
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:
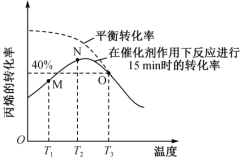
①N点_______ (填“有”或“没有”)达到平衡状态,原因是_______ 。
②M→N过程中C3H6转化率升高的原因是_______ 。
③T3时Kc=_______ ,若其他条件不变,往反应器中再加入2 mol C3H6,反应重新达到平衡时混合体系中乙烯的体积分数为_______ 。
 C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| C2H4的物质的量/mol | 0 | 0.8 | 1.2 | 1.5 | a | 1.5 |
①a=
②其他条件不变,若缩小反应器的体积,则C3H6转化率
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:

①N点
②M→N过程中C3H6转化率升高的原因是
③T3时Kc=
您最近一年使用:0次
2021-03-21更新
|
213次组卷
|
3卷引用:广西北海市2020-2021学年高二下学期期末教学质量检测化学试题
名校
4 . 根据所学知识回答下列问题:
(1)标准状况下,___ gCO和4.48LCO2所含的分子数目相同,两种气体的碳原子数之和为___ 。
(2)将标况下6.72LHCl气体溶于水,配成100mL溶液,得到物质的量浓度为___ 的盐酸溶液。
(3)已知8gA与32gB恰好完全反应,只生成0.5molC和18gD,则C的摩尔质量为___ 。
(1)标准状况下,
(2)将标况下6.72LHCl气体溶于水,配成100mL溶液,得到物质的量浓度为
(3)已知8gA与32gB恰好完全反应,只生成0.5molC和18gD,则C的摩尔质量为
您最近一年使用:0次
11-12高二上·广西北海·期中
5 . 将6 mol A、3 mol B充入容积为1 L的密闭容器中,进行如下反应:2A (g)+ B (g) 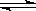 2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算:
2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算:
(1)用A表示的反应速率;___________
(2)B的转化率;__________
(3)平衡时C的物质的量浓度。______________
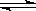 2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算:
2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算:(1)用A表示的反应速率;
(2)B的转化率;
(3)平衡时C的物质的量浓度。
您最近一年使用:0次
6 . 在一固定容积的密闭容器中,保持一定条件下进行以下反应:X(气)+2Y(气) 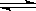 3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为 。
(2)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加入 mol Y,加入 mol Z,才能使平衡时Z为0.9 a mol。
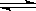 3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为 。
(2)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加入 mol Y,加入 mol Z,才能使平衡时Z为0.9 a mol。
您最近一年使用:0次
11-12高一上·广西北海·期末
7 . 向氢氧化钠溶液中慢慢地通入二氧化碳气体,反应生成正盐,当继续通入过量二氧化碳时,正盐便转化成酸式盐。
(1)写出上述反应的化学方程式
① 。
② 。
(2)标准状态下,向100 mL 2 mol·L-1 的NaOH溶液中通入3.36L二氧化碳气体,试求反应后所得溶质的物质的量为________________。
(1)写出上述反应的化学方程式
① 。
② 。
(2)标准状态下,向100 mL 2 mol·L-1 的NaOH溶液中通入3.36L二氧化碳气体,试求反应后所得溶质的物质的量为________________。
您最近一年使用:0次
11-12高二上·广西北海·期末
8 . 一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6升,再在此溶液中加入过量NaOH溶液,最终得到沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少?________
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积?________ 。
(1)Mg、Al的物质的量各为多少?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积?
您最近一年使用:0次



