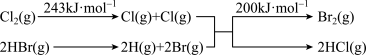已知:①

②
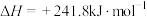
③
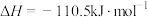
④
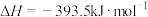
回答下列问题:
(1)上述变化中属于吸热反应的是___________ (填序号)。
(2)写出 燃烧的热化学方程式:
燃烧的热化学方程式:___________ 。
(3)反应 的
的
___________  。
。
(4)相同压强下,质量相等且起始温度相同的两份 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量___________ (填“>”“<”或“=”)反应Ⅱ放出的热量。
(5)在一定条件下,将 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
___________  。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:___________ 。
(6)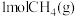 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:________ 。



②

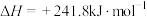
③

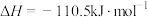
④

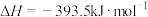
回答下列问题:
(1)上述变化中属于吸热反应的是
(2)写出
 燃烧的热化学方程式:
燃烧的热化学方程式:(3)反应
 的
的
 。
。(4)相同压强下,质量相等且起始温度相同的两份
 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量(5)在一定条件下,将
 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
 。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:(6)
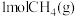 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:
更新时间:2024-02-19 15:15:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)已知2mol氢气燃烧生成液态水时放出572kJ热量,反应方程式是2H2(g)+O2(g)=2H2O(l)请回答下列问题:
①该反应的生成物能量总和_______ (填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,放出的热量_______ (填“>”、“<”或“=”)572kJ。
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点_______ 。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101kPa时:
2SO2(g)+O2(g)=2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是_______ 。
(3)已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为_______ 。
①该反应的生成物能量总和
②若2 mol氢气完全燃烧生成水蒸气,放出的热量
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101kPa时:
2SO2(g)+O2(g)=2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是
(3)已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氨(NH3)、肼(N2H4)是两种氮的氢化物。
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是___ 。
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?___ ,(若能,请说明理由),(若不能,请说明还需补充的数据)___ 。
途径Ⅰ.N2 NH3(ΔH1)
NH3(ΔH1)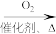 NO、H2O(l)(ΔH2)
NO、H2O(l)(ΔH2)
途径Ⅱ.N2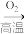 NO(ΔH)
NO(ΔH)
(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:___ 。
(4)在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
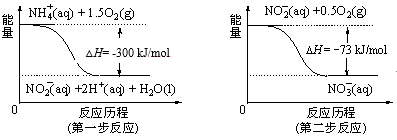
①第一步反应是___ (填“放热”或“吸热”)反应。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___ 。
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?
途径Ⅰ.N2
 NH3(ΔH1)
NH3(ΔH1)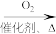 NO、H2O(l)(ΔH2)
NO、H2O(l)(ΔH2)途径Ⅱ.N2
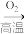 NO(ΔH)
NO(ΔH)(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
(4)在微生物的作用下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
【推荐3】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=________ kJ•mol-1。
(2)下列示意图中能体现上述反应能量变化的是________ 。判断的理由是________ 。
A.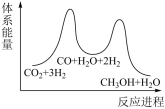 B.
B.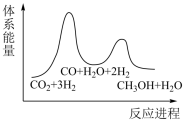 C.
C.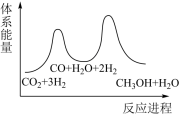
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=
(2)下列示意图中能体现上述反应能量变化的是
A.
 B.
B. C.
C.
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氨气具有还原性,例如,氨气能与卤素单质发生置换反应。已知几种化学键的键能数据如表所示。
请写出氨气与溴蒸气反应的热化学方程式:_______
| 化学键 | N-H | N≡N | Br-Br | H-Br |
| 键能/(kJ·mol-1) | 391 | 946 | 194 | 366 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】填空
(1)已知下列热化学方程式:
①H2O(1)=H2(g)+ O2(g) △H1=285.8 kJ∙mol−1
O2(g) △H1=285.8 kJ∙mol−1
②C(s)+ O2(g)=CO(g) △H2=−110.5 kJ∙mol−1
O2(g)=CO(g) △H2=−110.5 kJ∙mol−1
③H2O(g)=H2(g)+ O2(g) △H3=241.8 kJ∙mol−1
O2(g) △H3=241.8 kJ∙mol−1
上述反应中属于放热反应的是_____ 。
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为_____ 。
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么△H3将_____ (填“增大”“减小”或“不变”)
(4)反应C(s)+H2O(g)=CO(g)+H2(g)的△H=_____ kJ∙mol−1。
(5)0.1mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼(B2O3)和气态水,释放203.3kJ的热。
①写出反应的热化学方程式_____ 。
②H2O(1)=H2O(g) △H=_____ kJ∙mol−1。
③11.2L(标准状况)气态乙硼烷(B2H6)完全燃烧生成液态水生成的热_____ kJ。
(1)已知下列热化学方程式:
①H2O(1)=H2(g)+
 O2(g) △H1=285.8 kJ∙mol−1
O2(g) △H1=285.8 kJ∙mol−1②C(s)+
 O2(g)=CO(g) △H2=−110.5 kJ∙mol−1
O2(g)=CO(g) △H2=−110.5 kJ∙mol−1③H2O(g)=H2(g)+
 O2(g) △H3=241.8 kJ∙mol−1
O2(g) △H3=241.8 kJ∙mol−1上述反应中属于放热反应的是
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么△H3将
(4)反应C(s)+H2O(g)=CO(g)+H2(g)的△H=
(5)0.1mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼(B2O3)和气态水,释放203.3kJ的热。
①写出反应的热化学方程式
②H2O(1)=H2O(g) △H=
③11.2L(标准状况)气态乙硼烷(B2H6)完全燃烧生成液态水生成的热
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】CO2可用来合成低碳烯烃。
2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) ΔH=akJ·mol-1
CH2=CH2(g)+4H2O(g) ΔH=akJ·mol-1
已知:H2和CH2=CH2的燃烧热分别是285.8kJ·mol-1和1411.0kJ·mol-1,且H2O(g) H2O(l) ΔH=-44.0kJ·mol-1,则a=
H2O(l) ΔH=-44.0kJ·mol-1,则a=_____ 。
2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) ΔH=akJ·mol-1
CH2=CH2(g)+4H2O(g) ΔH=akJ·mol-1已知:H2和CH2=CH2的燃烧热分别是285.8kJ·mol-1和1411.0kJ·mol-1,且H2O(g)
 H2O(l) ΔH=-44.0kJ·mol-1,则a=
H2O(l) ΔH=-44.0kJ·mol-1,则a=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__ 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式___ 。
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:___ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–12NO(g)+O2(g)
 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】氮、碳氧化物的无害化处理是研究的热点。一定条件下 发生如下反应:
发生如下反应:
Ⅰ.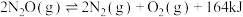
Ⅱ.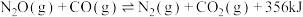
完成下列填空:
(1)反应Ⅰ平衡常数的表达式K=_______ 。
(2)某温度下,反应Ⅰ的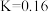 ,该温度下,测得容器中
,该温度下,测得容器中 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。_______
(3)甲为10L的恒温容器。盛有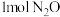 和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,
和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,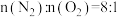 ,则
,则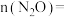
_______ mol;0~5min, 的平均反应速率
的平均反应速率
_______  。
。
(4)乙为10L的绝热容器。向其中充入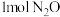 和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间
和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间_______ 甲;此时乙中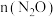 比甲中
比甲中_______ (以上两空选填“>”“<”或“=”),理由是:_______ 。
(5)不同压强的密闭容器中,分别充入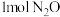 和1mol CO,发生反应Ⅰ和反应Ⅱ,测得
和1mol CO,发生反应Ⅰ和反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
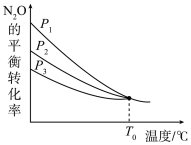
P1、P2、P3由小到大的顺序为_______ ;温度高于T0℃时,容器内发生的主要反应为_______ (填“Ⅰ”“Ⅱ”或“Ⅰ和Ⅱ”)。
 发生如下反应:
发生如下反应:Ⅰ.
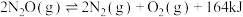
Ⅱ.
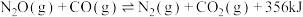
完成下列填空:
(1)反应Ⅰ平衡常数的表达式K=
(2)某温度下,反应Ⅰ的
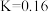 ,该温度下,测得容器中
,该温度下,测得容器中 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。(3)甲为10L的恒温容器。盛有
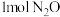 和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,
和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,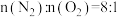 ,则
,则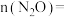
 的平均反应速率
的平均反应速率
 。
。(4)乙为10L的绝热容器。向其中充入
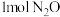 和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间
和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间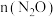 比甲中
比甲中(5)不同压强的密闭容器中,分别充入
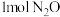 和1mol CO,发生反应Ⅰ和反应Ⅱ,测得
和1mol CO,发生反应Ⅰ和反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
P1、P2、P3由小到大的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在1L的密闭容器中,加入0.5molCaCO3,发生反应:CaCO3(s)⇌CaO(s)+CO2(g),图中A表示CO2的平衡浓度与温度的关系曲线。

(1)该反应正反应方向为_______ 热反应(填“吸”或“放”),温度为T5℃时,该反应的平衡常数 _______ 。
(2)达到平衡后,保持温度不变,再次通入1molCO2,平衡移动的方向_______ (填“正方向”、“逆方向”或“不”),再次平衡后容器内的压强 _______ (填“增大”、“减小”或“不变”)。
(3)加快该化学反应速率并能增加该反应进行程度的措施:_______ 。(写一种即可)

(1)该反应正反应方向为
(2)达到平衡后,保持温度不变,再次通入1molCO2,平衡移动的方向
(3)加快该化学反应速率并能增加该反应进行程度的措施:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知制备甲醇的有关化学反应及平衡常数如表所示:
(1)则反应
_______  ;
;
_______ (填数据)。
(2)850℃时,在密闭容器中进行反应①,开始时只加入 、
、 ,反应10
,反应10 后测得各组分的浓度如表:
后测得各组分的浓度如表:
(ⅰ)该时间段内反应速率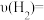
_______ 。
(ⅱ)比较此时正逆反应速率的大小υ正_______ (填“>““<”或“=”) υ逆。
(ⅲ)反应达到平衡后,保持其他条件不变,只把容器的体积缩小一半,平衡_______ (填“逆向”“正向”或“不”)移动,该反应的平衡常数_______ (填“增大”“减小”或“不变”)。
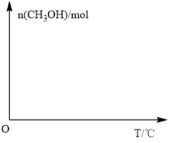
(3)反应①依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,甲醇物质的量变化的曲线示意图_________ 。
| 化学反应 | 反应热 | 平衡常数(850℃) |
①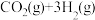 = =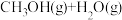 | 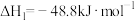 | 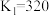 |
②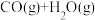 = = | 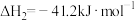 |  |
③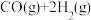 = = |  | 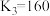 |
(1)则反应

 ;
;
(2)850℃时,在密闭容器中进行反应①,开始时只加入
 、
、 ,反应10
,反应10 后测得各组分的浓度如表:
后测得各组分的浓度如表:| 物质 |  |  |  |  |
浓度(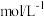 ) ) | 0.2 | 0.2 | 0.4 | 0.4 |
(ⅰ)该时间段内反应速率
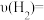
(ⅱ)比较此时正逆反应速率的大小υ正
(ⅲ)反应达到平衡后,保持其他条件不变,只把容器的体积缩小一半,平衡
(3)反应①依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,甲醇物质的量变化的曲线示意图

您最近一年使用:0次