依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__ 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式___ 。
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:___ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–12NO(g)+O2(g)
 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:
更新时间:2020-10-11 10:31:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】写出“0.5mol红热的炭和水蒸气充分反应,生成CO和氢气,吸收65.6KJ的热量”的热化学反应方程式。___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】写出下列反应的热化学方程式。
(1)已知断开1molH—H键、1molN—H键、1molN≡N键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______________________________
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,请写出该反应的热化学方程式:_______________________________________________

(1)已知断开1molH—H键、1molN—H键、1molN≡N键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,请写出该反应的热化学方程式:

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:____________ 。
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是_____________ (填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是____________ 。(填字母)
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
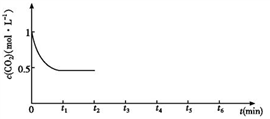
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。_____________
⑵改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)______ K(II)(填“﹥”“﹤”或“=”下同);平衡时CH3OH的浓度c(I)____ c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______ 。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”)。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡_____ 移动(填“正向”“逆向”或“不”)。
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:
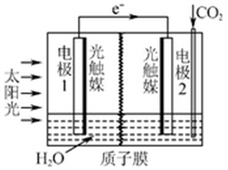
①电极2的电极反应式是____________ ;
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量_____ (填“增加”或“减少”______ g。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。

⑵改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:

①电极2的电极反应式是
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】以下几个热化学方程式中:
①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
②CO(g)+ O2(g)=CO2(g) ΔH=-283kJ·mol-1
O2(g)=CO2(g) ΔH=-283kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
④CaCO3=CaO+CO2 ΔH=+177.7kJ·mol-1
⑤C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ·mol-1
⑦ H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l) ΔH=-57.3kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3kJ·mol-1
不正确的有___ ;表示燃烧热的热化学方程式有___ ,表示中和热的热化学方程式有___ 。(填序号)
①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
②CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ·mol-1
O2(g)=CO2(g) ΔH=-283kJ·mol-1③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
④CaCO3=CaO+CO2 ΔH=+177.7kJ·mol-1
⑤C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ·mol-1
⑦
 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l) ΔH=-57.3kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3kJ·mol-1不正确的有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2, ΔH1_______ ΔH2(填“>”“<”或“=”,下同)。
(2)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1_______ ΔH2。
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2
(3)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量_______ 57.3 kJ。
(4)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t ℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式_______ 。
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2, ΔH1
(2)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2
(3)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
(4)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t ℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题
(1)下列反应中,属于放热反应的是__________ ,属于吸热反应的是________ 。
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有______________________ 。
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有____________ ;表示中和热的热化学方程式有_____________________ 。
(1)下列反应中,属于放热反应的是
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)已知:25 ℃、101 kPa时,Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ·mol-1;S(s)+O2(g)===SO2(g) ΔH=-297 kJ·mol-1;Mn(s)+S(s)+2O2(g)===MnSO4(s) ΔH=-1 065 kJ·mol-1 SO2与MnO2反应生成无水MnSO4的热化学方程式是___________________________ 。
(2)已知:温度过高时,WO2(s)转变为WO2(g):①WO2(s)+2H2(g) W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1②WO2(g)+2H2(g)
W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1②WO2(g)+2H2(g) W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1;则WO2(s)W
W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1;则WO2(s)W O2(g)的ΔH=
O2(g)的ΔH=______________
(2)已知:温度过高时,WO2(s)转变为WO2(g):①WO2(s)+2H2(g)
 W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1②WO2(g)+2H2(g)
W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1②WO2(g)+2H2(g) W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1;则WO2(s)W
W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1;则WO2(s)W O2(g)的ΔH=
O2(g)的ΔH=
您最近一年使用:0次
【推荐2】Ⅰ:载人航天器中,利用萨巴蒂尔反应将航天员呼出的 转化为
转化为 ,再通过电解
,再通过电解 获得
获得 ,实现
,实现 的再生。
的再生。
已知:①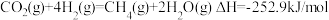
②
请回答:
(1)反应②属于_______ (填“吸热”或“放热”)反应。
(2)反应①消耗 时,反应
时,反应_______ (填“吸热”或“放热”)热量,其数值为_______ kJ。
(3)反应②热量变化为 时,生成
时,生成 的质量为
的质量为_______ 。
(4)反应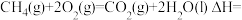
_______  。
。
Ⅱ: 资源化利用的方法之一是合成二甲醚
资源化利用的方法之一是合成二甲醚 。
。 催化加氢合成二甲醚的过程中主要发生下列反应:
催化加氢合成二甲醚的过程中主要发生下列反应:
反应Ⅰ:
反应Ⅱ:
(5)其中,反应Ⅱ:分以下①②两步完成,请写出反应①的热化学方程式。
①_______ 。
②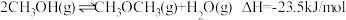
 转化为
转化为 ,再通过电解
,再通过电解 获得
获得 ,实现
,实现 的再生。
的再生。已知:①
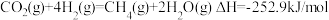
②

请回答:
(1)反应②属于
(2)反应①消耗
 时,反应
时,反应(3)反应②热量变化为
 时,生成
时,生成 的质量为
的质量为(4)反应
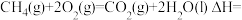
 。
。Ⅱ:
 资源化利用的方法之一是合成二甲醚
资源化利用的方法之一是合成二甲醚 。
。 催化加氢合成二甲醚的过程中主要发生下列反应:
催化加氢合成二甲醚的过程中主要发生下列反应:反应Ⅰ:

反应Ⅱ:

(5)其中,反应Ⅱ:分以下①②两步完成,请写出反应①的热化学方程式。
①
②
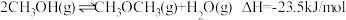
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
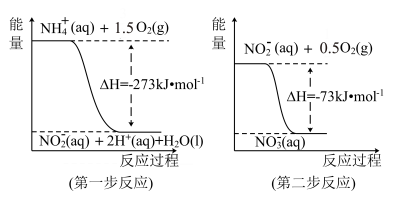
(1)第一步反应是________ (填“放热”或“吸热”)反应,判断依据是_________ 。
(2)1mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: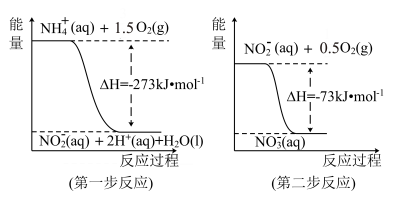
(1)第一步反应是
(2)1mol
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
【推荐2】甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
①CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1=260kJ•mol﹣1
2CO(g)+2H2(g) △H1=260kJ•mol﹣1
已知:②2CO(g)+O2(g) 2CO2(g) △H2=﹣566kJ•mol﹣1
2CO2(g) △H2=﹣566kJ•mol﹣1
则CH4与O2反应生成CO和H2的热化学方程式为_______________ 。
(2)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
①b处电极上发生的电极反应式:_______________________ ;
②电镀结束后,装置Ⅰ中KOH溶液的浓度______________ (填写“变大”、“变小”或“不变”),装置Ⅱ中Cu电极上发生的电极反应式:______________ 。
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷_____________ L(标准状况下)。

(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
①CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1=260kJ•mol﹣1
2CO(g)+2H2(g) △H1=260kJ•mol﹣1已知:②2CO(g)+O2(g)
 2CO2(g) △H2=﹣566kJ•mol﹣1
2CO2(g) △H2=﹣566kJ•mol﹣1则CH4与O2反应生成CO和H2的热化学方程式为
(2)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
①b处电极上发生的电极反应式:
②电镀结束后,装置Ⅰ中KOH溶液的浓度
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
(1)H2的燃烧热ΔH=_________ 。
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为_________ g。
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________ 。
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1(1)H2的燃烧热ΔH=
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次



