用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
(1)H2的燃烧热ΔH=_________ 。
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为_________ g。
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________ 。
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1(1)H2的燃烧热ΔH=
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
20-21高二下·青海海东·阶段练习 查看更多[3]
青海省海东市第二中学2020-2021学年高二4月月考化学试题(已下线)第1章 化学反应与能量(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
更新时间:2021-06-07 20:50:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】依据事实,写出下列反应的热化学方程式
(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为_______ 。
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_______ 。
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:_______ 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是_______ 。
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为_______ 。
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_______ 。

(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1) 碳与适量水蒸气反应生成CO和H2,需吸收
碳与适量水蒸气反应生成CO和H2,需吸收 热量,此反应的热化学方程式为
热量,此反应的热化学方程式为_________________
(2)已知 ;
;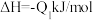
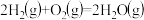 ;
;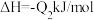
 ;
;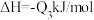
常温下,取体积比4:1的甲烷和氢气的混合气体 (标准状况下),经完全燃烧后恢复至室温,则放出的热量为
(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___________
 碳与适量水蒸气反应生成CO和H2,需吸收
碳与适量水蒸气反应生成CO和H2,需吸收 热量,此反应的热化学方程式为
热量,此反应的热化学方程式为(2)已知
 ;
;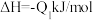
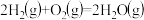 ;
;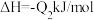
 ;
;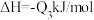
常温下,取体积比4:1的甲烷和氢气的混合气体
 (标准状况下),经完全燃烧后恢复至室温,则放出的热量为
(标准状况下),经完全燃烧后恢复至室温,则放出的热量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求写热化学方程式:
(1)25℃、101kPa条件下充分燃烧一定量的C2H2气体放出热量为1300kJ,经测定,将生成的CO2通入足量澄清石灰水中产生100g白色沉淀,写出表示C2H2气体充分燃烧的热化学方程式:___ ;
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式:___ 。
(1)25℃、101kPa条件下充分燃烧一定量的C2H2气体放出热量为1300kJ,经测定,将生成的CO2通入足量澄清石灰水中产生100g白色沉淀,写出表示C2H2气体充分燃烧的热化学方程式:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式:
您最近一年使用:0次
【推荐1】请认真观察图,然后回答问题:
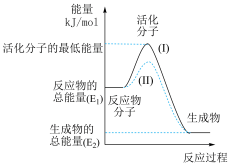
(1)图中所示反应是___ (填“吸热”或“放热”)反应
(2)图中所示反应的ΔH=___ (用含E1、E2的代数式表示)。
(3)下列4个反应中,符合示意图描述的反应的是____ (填代号)。
A.盐酸与NaOH反应 B.Na与H2O反应生成H2
C.铝热反应 D.灼热的炭与水蒸气反应生成CO和H2
(4)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:___ 。

(1)图中所示反应是
(2)图中所示反应的ΔH=
(3)下列4个反应中,符合示意图描述的反应的是
A.盐酸与NaOH反应 B.Na与H2O反应生成H2
C.铝热反应 D.灼热的炭与水蒸气反应生成CO和H2
(4)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】近年来,由CO2催化加氢合成甲醇的相关研究受到越来越多的关注.该方法既可解决CO2废气的利用问题,又可开发生产甲醇的新途径,具有良好的应用前景.已知4.4 g CO2气体与H2经催化加氢生成CH3OH气体和水蒸气时放出4.95 kJ的能量.
(1)该反应的热化学方程式为:_____ .
(2)在270℃、8 MPa和适当催化剂的条件下,CO2的转化率达到22%,则4.48 m3(已折合为标准状况)的CO2能合成CH3OH气体的物质的量是______ ,此过程中能放出热量_____ kJ.
(3)又已知H2O(g)===H2O(l) ΔH=-44 kJ/mol,则22 g CO2气体与H2反应生成CH3OH气体和液态水时放出热量为______ .
(1)该反应的热化学方程式为:
(2)在270℃、8 MPa和适当催化剂的条件下,CO2的转化率达到22%,则4.48 m3(已折合为标准状况)的CO2能合成CH3OH气体的物质的量是
(3)又已知H2O(g)===H2O(l) ΔH=-44 kJ/mol,则22 g CO2气体与H2反应生成CH3OH气体和液态水时放出热量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)已知断裂1mol H﹣H键、1mol N≡N键分别需要吸收436kJ、946kJ的能量,生成1mol N﹣H键放出391kJ的能量,试写出N2(g)与H2(g)反应生成NH3(g)的热化学方程式:____________________________ .
(2)已知:C(s)+O2(g)═CO2(g)△H=﹣437.3kJ•mol﹣1
H2(g)+ O2(g)=H2O(g)△H=﹣285.8kJ•mol﹣1
O2(g)=H2O(g)△H=﹣285.8kJ•mol﹣1
CO(g)+ O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1
O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1
则煤的气化主要反应的热化学方程式是:C(s)+H2O(g)═CO(g)+H2(g)△H=______ .
(2)已知:C(s)+O2(g)═CO2(g)△H=﹣437.3kJ•mol﹣1
H2(g)+
 O2(g)=H2O(g)△H=﹣285.8kJ•mol﹣1
O2(g)=H2O(g)△H=﹣285.8kJ•mol﹣1CO(g)+
 O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1
O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1则煤的气化主要反应的热化学方程式是:C(s)+H2O(g)═CO(g)+H2(g)△H=
您最近一年使用:0次

 ,则
,则
 。
。
 ;
; 。
。 的燃烧热为
的燃烧热为 的燃烧热为
的燃烧热为 和
和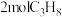 组成的混合气体完全燃烧生成
组成的混合气体完全燃烧生成 和
和 时放出的热量为
时放出的热量为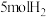 和
和 的混合气体完全燃烧生成
的混合气体完全燃烧生成 ,则在混合气体中
,则在混合气体中 和
和

