回答下列问题
(1)下列反应中,属于放热反应的是__________ ,属于吸热反应的是________ 。
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有______________________ 。
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有____________ ;表示中和热的热化学方程式有_____________________ 。
(1)下列反应中,属于放热反应的是
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有
更新时间:2022-12-05 16:51:13
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知反应2Al+3H2SO4=Al2(SO4)3+3H2↑的能量变化趋势如图所示:
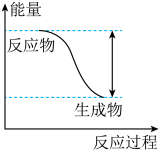
(1)该反应为______ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是_____ (填字母)。
(3)①若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:_____ (填“正”或“负”)极,该极上发生的电极反应为:______ 。
②标况下当电池中共收集到2.24L氢气时,外电路共转移______ mol电子。

(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
| A.改铝片为铝粉 | B.改稀硫酸为98%的浓硫酸 |
| C.升高温度 | D.使用催化剂 |
②标况下当电池中共收集到2.24L氢气时,外电路共转移
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下列反应中,属于放热反应的是_____________ 。
① 煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ② 燃烧木炭取暖 ③生石灰与水反应 ④ 酸与碱的中和反应 ⑤ 氢气还原氧化铜 ⑥ 灼热的木炭与CO2反应
① 煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ② 燃烧木炭取暖 ③生石灰与水反应 ④ 酸与碱的中和反应 ⑤ 氢气还原氧化铜 ⑥ 灼热的木炭与CO2反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(I)回答下列问题:
(1)下列反应中,属于放热反应的是____ (填序号,下同),属于吸热反应的是____ 。
①物质燃烧 ②二氧化碳通过炽热的碳 ③氢氧化钠溶于水的过程 ④炸药爆炸 ⑤碳酸钙高温分解
(II)表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ)。
根据上述数据回答下列问题:
(2)下列物质本身具有的能量最低的是____ 。
(3)下列氢化物中,最稳定的是____ 。
(4)X2+H2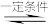 2HX(X代表Cl、Br、I)是
2HX(X代表Cl、Br、I)是____ (填“吸热”或“放热”)反应。
(5)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是____ 。
(1)下列反应中,属于放热反应的是
①物质燃烧 ②二氧化碳通过炽热的碳 ③氢氧化钠溶于水的过程 ④炸药爆炸 ⑤碳酸钙高温分解
(II)表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ)。
| 物质 | Cl2 | Br2 | I2 | H2 |
| 能量/kJ | 243 | 193 | 151 | 436 |
| 物质 | HF | HCl | HBr | HI |
| 能量/kJ | 568 | 432 | 366 | 298 |
(2)下列物质本身具有的能量最低的是
| A.H2 | B.Cl2 | C.Br2 | D.I2 |
| A.HF | B.HCl | C.HBr | D.HI |
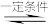 2HX(X代表Cl、Br、I)是
2HX(X代表Cl、Br、I)是(5)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】依据事实,写出下列反应的热化学方程式。
(1)1mol N2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量__________ 。
(2)1mol N2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量_________ 。
(1)1mol N2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量
(2)1mol N2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察图,然后回答问题:
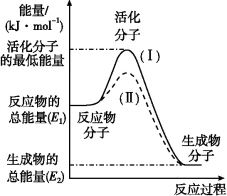
(1)图中所示反应是___ (填“吸热”或“放热”)反应,该反应的ΔH=___ (用含E1、E2的代数式表示)。
(2)下列4个反应中符合示意图描述的反应的是___ (填代号)。
A.水蒸气与炭反应
B.用水稀释氢氧化钠溶液
C.铝粉与四氧化三铁反应
D.灼热的炭与CO2反应
(3)已知0.5molCH4(g)与0.5mol水蒸气在25℃、101kPa时,完全反应生成CO和H2的混合气体,吸收了akJ热量,该反应的热化学方程式是___ 。

(1)图中所示反应是
(2)下列4个反应中符合示意图描述的反应的是
A.水蒸气与炭反应
B.用水稀释氢氧化钠溶液
C.铝粉与四氧化三铁反应
D.灼热的炭与CO2反应
(3)已知0.5molCH4(g)与0.5mol水蒸气在25℃、101kPa时,完全反应生成CO和H2的混合气体,吸收了akJ热量,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__ 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式___ 。
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:___ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–12NO(g)+O2(g)
 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.已知下列热化学方程式:①H2(g)+ O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,
②H2(g)+ O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
③C(s)+ O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为___________ ;(填序号)
(2)燃烧1gH2生成气态水,放出的热量为___________ 。
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量___________ (填“大于”“等于”或“小于”)57.3kJ,原因是___________ 。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热∆H ___________ 0。
 O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,②H2(g)+
 O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,③C(s)+
 O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为
(2)燃烧1gH2生成气态水,放出的热量为
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题
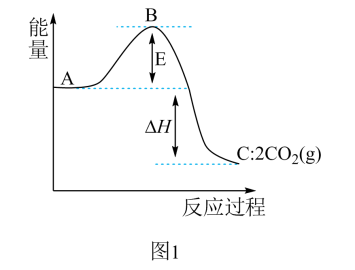
(1)
 的反应过程的能量变化如图1所示,则图中A表示
的反应过程的能量变化如图1所示,则图中A表示_______ 。该反应的逆反应的活化能为(用E、 表示)
表示)_______ 。
(2)已知:298K时,
 kJ∙mol−1
kJ∙mol−1

 kJ∙mol−1
kJ∙mol−1
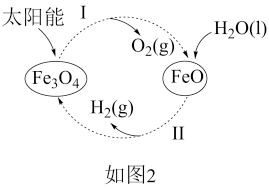
① 的燃烧热
的燃烧热
_______ kJ∙mol−1。
②以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图2。
的过程如图2。
过程Ⅰ: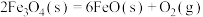
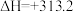 kJ∙mol−1
kJ∙mol−1
过程Ⅱ:……
请回答:ⅰ.过程Ⅰ中能量转化的形式是_______ 。
ⅱ.过程Ⅱ的热化学方程式为_______ 。
(3)50 mL 0.50 mol∙L−1盐酸与50 mL 0.55 mol∙L−1 NaOH溶液在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为23.2℃。(假设反应前后溶液的比热容均为4.18 J·g ·℃
·℃ 、溶液的密度均为1.00g·cm
、溶液的密度均为1.00g·cm )则反应
)则反应 的
的
_______ kJ∙mol−1。(结果保留3位有效数字)
(1)

 的反应过程的能量变化如图1所示,则图中A表示
的反应过程的能量变化如图1所示,则图中A表示 表示)
表示)
(2)已知:298K时,

 kJ∙mol−1
kJ∙mol−1
 kJ∙mol−1
kJ∙mol−1
①
 的燃烧热
的燃烧热
②以太阳能为热源分解
 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图2。
的过程如图2。过程Ⅰ:
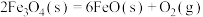
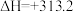 kJ∙mol−1
kJ∙mol−1过程Ⅱ:……
请回答:ⅰ.过程Ⅰ中能量转化的形式是
ⅱ.过程Ⅱ的热化学方程式为
(3)50 mL 0.50 mol∙L−1盐酸与50 mL 0.55 mol∙L−1 NaOH溶液在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为23.2℃。(假设反应前后溶液的比热容均为4.18 J·g
 ·℃
·℃ 、溶液的密度均为1.00g·cm
、溶液的密度均为1.00g·cm )则反应
)则反应 的
的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:______________________________________ 。
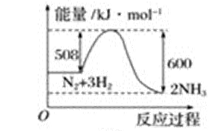
(2)根据下图写出热化学方程式__________________________________________ 。
(3)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__________________ 。
(4)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol–1
2SO3(g) ΔH=-196.6 kJ·mol–1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol–1
2NO2(g) ΔH=-113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式____________________ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)根据下图写出热化学方程式

(3)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(4)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ·mol–1
2SO3(g) ΔH=-196.6 kJ·mol–12NO(g)+O2(g)
 2NO2(g) ΔH=-113.0 kJ·mol–1
2NO2(g) ΔH=-113.0 kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)已知:H—H键的键能为436kJ/mol,H—N键的键能为391kJ/mol,根据化学方程式:N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ/mol。请计算出N≡N键的键能为________ 。
(2)①已知:C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol,
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g) 时ΔH=________ kJ/mol。
②当把0.4mol液态肼和0.8mol液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为___________ ;
③已知11g丙烷(C3H8)在298K和101Kpa条件下完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式:___________ 。
(2)①已知:C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol,
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g) 时ΔH=
②当把0.4mol液态肼和0.8mol液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为
③已知11g丙烷(C3H8)在298K和101Kpa条件下完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+C12(g) =2HCl(g) ΔH= - 184.6 kJ•mol-1;该反应属于_______ (填“热吸”或“放热”)反应 。
(2)下列反应中,属于放热反应的是_______ (填序号)。
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(3)已知破坏1 mol H-H 键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ 。则由氢气和碘单质反应生成2molHI 需要放出_______ kJ 的热量。
(4)常温常压下,1 mol乙醇完全燃烧生成CO2气体和液态水放出的热量为1367 kJ,写出乙醇燃烧热的热化学方程式:_______
(5)已知稀溶液中,1mol HCl与NaOH溶液恰好完全反应时,放出57.3kJ热量,写出表示HCl与NaOH反应的中和热的热化学方程式_______ 。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+C12(g) =2HCl(g) ΔH= - 184.6 kJ•mol-1;该反应属于
(2)下列反应中,属于放热反应的是
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(3)已知破坏1 mol H-H 键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ 。则由氢气和碘单质反应生成2molHI 需要放出
(4)常温常压下,1 mol乙醇完全燃烧生成CO2气体和液态水放出的热量为1367 kJ,写出乙醇燃烧热的热化学方程式:
(5)已知稀溶液中,1mol HCl与NaOH溶液恰好完全反应时,放出57.3kJ热量,写出表示HCl与NaOH反应的中和热的热化学方程式
您最近一年使用:0次

 葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出
葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出 热量:
热量: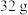 铜粉在足量氧气中反应生成氧化铜固体时放出
铜粉在足量氧气中反应生成氧化铜固体时放出 热量:
热量: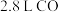 气体在氧气中完全燃烧生成二氧化碳气体时放出
气体在氧气中完全燃烧生成二氧化碳气体时放出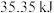 热量:
热量: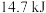 热量:
热量:

