氨(NH3)、肼(N2H4)是两种氮的氢化物。
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是___ 。
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?___ ,(若能,请说明理由),(若不能,请说明还需补充的数据)___ 。
途径Ⅰ.N2 NH3(ΔH1)
NH3(ΔH1)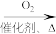 NO、H2O(l)(ΔH2)
NO、H2O(l)(ΔH2)
途径Ⅱ.N2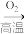 NO(ΔH)
NO(ΔH)
(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:___ 。
(4)在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
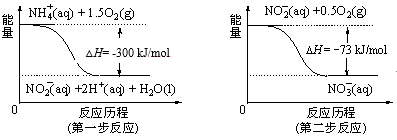
①第一步反应是___ (填“放热”或“吸热”)反应。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___ 。
(1)合成氨的反应是一个放热反应。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如图:

状态②、③、④中,能量最高的状态是
(2)已知途径Ⅰ两步转化反应的反应热分别为ΔH1、ΔH2,途径Ⅱ所示反应的反应热为ΔH,能否由途径Ⅰ的反应热推出途径Ⅱ的ΔH?
途径Ⅰ.N2
 NH3(ΔH1)
NH3(ΔH1)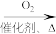 NO、H2O(l)(ΔH2)
NO、H2O(l)(ΔH2)途径Ⅱ.N2
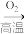 NO(ΔH)
NO(ΔH)(3)发射卫星时用肼(N2H4)作燃料、二氧化氮(NO2)作氧化剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1= +67kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2= -500kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
(4)在微生物的作用下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
更新时间:2021/01/25 16:10:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。
已知:C3H8(g) → CH4(g) + HC≡CH(g) + H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g) → CH4(g) + HC≡CH(g) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g) → CH3CH=CH2(g) + H2(g)的△H=___________ kJ·mol-1;
(2)已知H2(g) + Br2(l) = 2HBr(g) ΔH=-72 kJ/mol,蒸发1 mol Br2(l)需要吸收的能量为30 kJ。
则反应:H2(g) + Br2(g) = 2HBr(g) ΔH=____________ kJ/mol,若断裂1 mol H2(g)分子中的化学键需要吸收能量436kJ, 断裂1 mol HBr(g)分子中的化学键需要吸收能量369kJ,则断裂1 mol Br2(g)分子中的化学键需要吸收的能量为:____________ kJ。
已知:C3H8(g) → CH4(g) + HC≡CH(g) + H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g) → CH4(g) + HC≡CH(g) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g) → CH3CH=CH2(g) + H2(g)的△H=
(2)已知H2(g) + Br2(l) = 2HBr(g) ΔH=-72 kJ/mol,蒸发1 mol Br2(l)需要吸收的能量为30 kJ。
则反应:H2(g) + Br2(g) = 2HBr(g) ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知下列反应:SO2(g)+2OH-(aq)= (aq)+H2O(l) ΔH1,ClO-(aq)+
(aq)+H2O(l) ΔH1,ClO-(aq)+ (aq)=
(aq)= (aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+
(aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+ (aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
(aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=_____ 。
 (aq)+H2O(l) ΔH1,ClO-(aq)+
(aq)+H2O(l) ΔH1,ClO-(aq)+ (aq)=
(aq)= (aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+
(aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+ (aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
(aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】推动煤炭清洁高效利用是未来煤炭利用的发展方向,其中煤制天然气(主要成分甲烷)能对燃气资源有重要补充作用。在催化剂作用下,其涉及的主要反应如下:
CO(g)+3H2(g) ⇌CH4(g)+H2O(g) ΔH1=-206.2 kJ·mol-1 Ⅰ
CO(g)+H2O(g) ⇌CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 Ⅱ
CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH3 Ⅲ
荷兰埃因霍温大学学者结合实验与计算机模拟结果,研究了在催化剂钴表面上反应Ⅰ的反应历程,如图所示,其中吸附在钴催化剂表面上的物种用*标注。
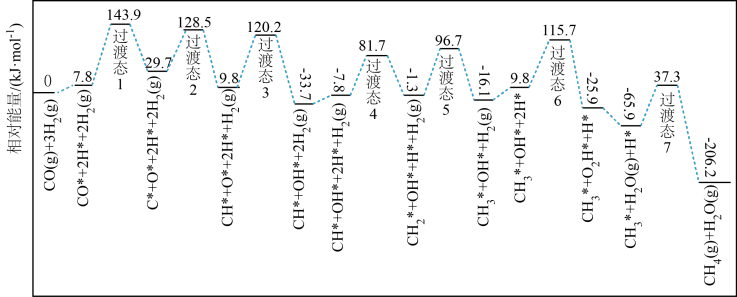
(1)该历程中最大能垒E正=_______ kJ·mol-1,写出该步骤的化学方程式:_______
(2)ΔH3=_______ kJ·mol-1
CO(g)+3H2(g) ⇌CH4(g)+H2O(g) ΔH1=-206.2 kJ·mol-1 Ⅰ
CO(g)+H2O(g) ⇌CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 Ⅱ
CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH3 Ⅲ
荷兰埃因霍温大学学者结合实验与计算机模拟结果,研究了在催化剂钴表面上反应Ⅰ的反应历程,如图所示,其中吸附在钴催化剂表面上的物种用*标注。

(1)该历程中最大能垒E正=
(2)ΔH3=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题
(1)0.1mol 完全燃烧生成液态水和
完全燃烧生成液态水和 ,放出88.96kJ热量,
,放出88.96kJ热量, 的燃烧热为
的燃烧热为
___________ kJ/mol。
(2)单斜硫和正交硫转化为 的能量变化图如图。
的能量变化图如图。
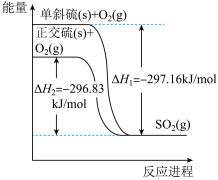
32g单斜硫转化为正交硫的反应热为
___________ kJ/mol,单斜硫比正交硫的稳定性___________ (填“强”或“弱”)。
(3) 和
和 在一定条件下能发生反应:
在一定条件下能发生反应: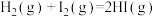
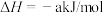
已知:
 a、b、c均大于零
a、b、c均大于零
断开1mol H-I键所需能量为___________ kJ/mol。
(1)0.1mol
 完全燃烧生成液态水和
完全燃烧生成液态水和 ,放出88.96kJ热量,
,放出88.96kJ热量, 的燃烧热为
的燃烧热为
(2)单斜硫和正交硫转化为
 的能量变化图如图。
的能量变化图如图。
32g单斜硫转化为正交硫的反应热为

(3)
 和
和 在一定条件下能发生反应:
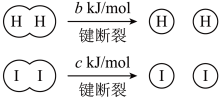
在一定条件下能发生反应: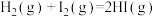
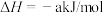
已知:
 a、b、c均大于零
a、b、c均大于零断开1mol H-I键所需能量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ/mol,H—H键的键能是436.0 kJ/mol;由N2和H2合成1 mol NH3时可放出46.2 kJ的热量。则N—H键的键能是______ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式______ 。
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是______ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】 在101kPa时,
在101kPa时, 在
在 中完全燃烧生成2mol液态水,放出
中完全燃烧生成2mol液态水,放出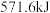 的热量,请写出
的热量,请写出 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
 已知1g碳粉在氧气中完全燃烧放出的热量是
已知1g碳粉在氧气中完全燃烧放出的热量是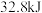 ,试写出相关的热化学方程式
,试写出相关的热化学方程式_________ 。
 已知在常温常压下:
已知在常温常压下:
①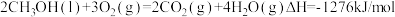
②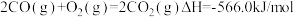
③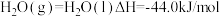
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______
 将
将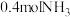 和
和 充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。

① 下,5min内该反应的平均反应速率
下,5min内该反应的平均反应速率
________________
②若不考虑催化剂的影响,5min时 下和
下和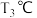 下逆反应速率较快的为
下逆反应速率较快的为________________  填“
填“ ”或“
”或“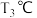 ”
” ,原因为
,原因为________
 在101kPa时,
在101kPa时, 在
在 中完全燃烧生成2mol液态水,放出
中完全燃烧生成2mol液态水,放出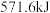 的热量,请写出
的热量,请写出 燃烧热的热化学方程式为
燃烧热的热化学方程式为 已知1g碳粉在氧气中完全燃烧放出的热量是
已知1g碳粉在氧气中完全燃烧放出的热量是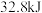 ,试写出相关的热化学方程式
,试写出相关的热化学方程式 已知在常温常压下:
已知在常温常压下:①
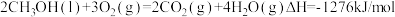
②
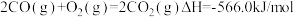
③
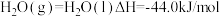
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
 将
将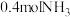 和
和 充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
①
 下,5min内该反应的平均反应速率
下,5min内该反应的平均反应速率
②若不考虑催化剂的影响,5min时
 下和
下和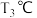 下逆反应速率较快的为
下逆反应速率较快的为 填“
填“ ”或“
”或“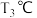 ”
” ,原因为
,原因为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】汽油是一种重要的车用燃料。
(1)汽油的主要成分为 的烃类混合物,如
的烃类混合物,如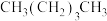 等。
等。
①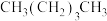 中各碳原子之间的成键方式为
中各碳原子之间的成键方式为___________ 。
②写出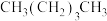 一种同分异构体的结构简式:
一种同分异构体的结构简式:___________ 。
(2)辛烷 燃烧时的能量变化可用图
燃烧时的能量变化可用图___________ (填“A”或“B”)表示。 和
和 的反应,其能量变化示意图如下。
的反应,其能量变化示意图如下。___________ 结合,过程i需要的能量比较多。
②比较常温时的稳定性:
___________ (填“ ”或“
”或“ ”)
”)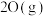 。
。
③ 为
为___________ (填“放热”或“吸热”)反应。
(1)汽油的主要成分为
 的烃类混合物,如
的烃类混合物,如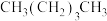 等。
等。①
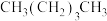 中各碳原子之间的成键方式为
中各碳原子之间的成键方式为②写出
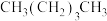 一种同分异构体的结构简式:
一种同分异构体的结构简式:(2)辛烷
 燃烧时的能量变化可用图
燃烧时的能量变化可用图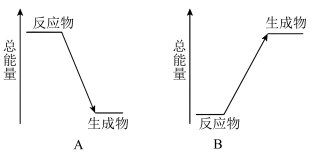
 和
和 的反应,其能量变化示意图如下。
的反应,其能量变化示意图如下。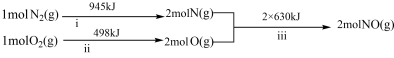
②比较常温时的稳定性:

 ”或“
”或“ ”)
”)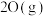 。
。③
 为
为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)下列过程不一定属于放热过程的是_______ (填标号)。
A.形成化学键B.燃料燃烧C.化合反应 D.葡萄糖的氧化分解E.酸碱中和F.炸药爆炸
(2)已知A和B是同种元素形成的两种单质,A转化为B时需要吸收能量,则A和B中较稳定的是_______ (填“A”或“B”)。
(3)某化学反应中,反应物的总能量为 ,生成物的总能量为
,生成物的总能量为 ,且
,且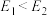 ,则该反应是
,则该反应是_______ (填“放热”或“吸热”)反应。
(4)等质量的下列各物质完全燃烧,放出热量较多的是_______ (填标号,下同)。
A.固体硫B.硫蒸气
(5)已知 和
和 反应时放热,且断裂
反应时放热,且断裂
 键、
键、 氧氧键、
氧氧键、
 键需要吸收的能量分别为
键需要吸收的能量分别为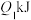 、
、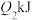 、
、 。下列关系一定正确的是
。下列关系一定正确的是_______ 。
A.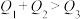 B.
B.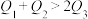
C.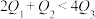 D.
D.
A.形成化学键B.燃料燃烧C.化合反应 D.葡萄糖的氧化分解E.酸碱中和F.炸药爆炸
(2)已知A和B是同种元素形成的两种单质,A转化为B时需要吸收能量,则A和B中较稳定的是
(3)某化学反应中,反应物的总能量为
 ,生成物的总能量为
,生成物的总能量为 ,且
,且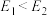 ,则该反应是
,则该反应是(4)等质量的下列各物质完全燃烧,放出热量较多的是
A.固体硫B.硫蒸气
(5)已知
 和
和 反应时放热,且断裂
反应时放热,且断裂
 键、
键、 氧氧键、
氧氧键、
 键需要吸收的能量分别为
键需要吸收的能量分别为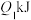 、
、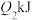 、
、 。下列关系一定正确的是
。下列关系一定正确的是A.
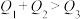 B.
B.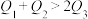
C.
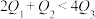 D.
D.
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学反应中的物质变化和能量变化与化学键密切相关。依据所学知识回答下列问题:
1.(1)将装有二氧化氮和四氧化二氮混合气体的烧瓶分别侵入冷水和热水中,观察到的现象是______________________ ,由此得出的结论是_______________________________________ 。
2.(2)某同学根据原电池原理。将离子反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,在该原电池中,以FeCl3 为电解质溶液,以石墨为正极材料,负极材料应选用_______________ ,负极上发生________ 反应(填写“氧化“或“还原”)。当反应进行一段时间,测得负极电极质量减轻了6.4g,原电池的电路中转移电子的物质的量是____________________________ 。
3.(3)从能量角度看,断裂化学键吸收能量,形成化学键释放能量。
已知:断裂1molH-H键吸收的能量为436kJ,断裂气态ImolI-I键吸收的能量为151kJ,形成lmolH-I键放出的能量为299kJ。
则由氢气和碘蒸气反应生成1molHI需要________ (填“放出“或“吸收”)_______ kJ的热量
1.(1)将装有二氧化氮和四氧化二氮混合气体的烧瓶分别侵入冷水和热水中,观察到的现象是
2.(2)某同学根据原电池原理。将离子反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,在该原电池中,以FeCl3 为电解质溶液,以石墨为正极材料,负极材料应选用
3.(3)从能量角度看,断裂化学键吸收能量,形成化学键释放能量。
已知:断裂1molH-H键吸收的能量为436kJ,断裂气态ImolI-I键吸收的能量为151kJ,形成lmolH-I键放出的能量为299kJ。
则由氢气和碘蒸气反应生成1molHI需要
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列热化学反应方程式:
(1)1molN2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量:_________________________
(2)1molN2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量:____________________________
(3)1molCu(s)能与一定量的O2(g)起反应生成CuO(s),放出157kJ热量:____________
(4)1molC8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518kJ热量:_______________
(1)1molN2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量:
(2)1molN2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量:
(3)1molCu(s)能与一定量的O2(g)起反应生成CuO(s),放出157kJ热量:
(4)1molC8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518kJ热量:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是________________ (任答一点)
(2)在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________ 生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为______________
③该反应的热化学方程式为__________________________________________________
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________ kJ·mol-1
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________ kJ·mol-1
(1)氢能被称为绿色能源的原因是
(2)在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量
②氢气的燃烧热为
③该反应的热化学方程式为
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素。其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。完成下列填空:
(1)元素Y的原子其核外有_______ 种运动状态不同的电子存在;
(2)在上述元素所构成的单质或化合物中,可用作自来水消毒剂的有_______ 、_______ (至少写出两种,填写化学式);
(3)已知X2M的燃烧热为 187kJ/mol。(提示:燃烧热的定义:1mol可燃物充分燃烧生成稳定化合物时所放出的热量。)写出X2M燃烧的热化学方程式:_________ 。
(1)元素Y的原子其核外有
(2)在上述元素所构成的单质或化合物中,可用作自来水消毒剂的有
(3)已知X2M的燃烧热为 187kJ/mol。(提示:燃烧热的定义:1mol可燃物充分燃烧生成稳定化合物时所放出的热量。)写出X2M燃烧的热化学方程式:
您最近一年使用:0次



