有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是________________ (任答一点)
(2)在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________ 生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为______________
③该反应的热化学方程式为__________________________________________________
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________ kJ·mol-1
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________ kJ·mol-1
(1)氢能被称为绿色能源的原因是
(2)在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量
②氢气的燃烧热为
③该反应的热化学方程式为
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=
更新时间:2017-05-20 20:36:18
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列燃烧热的热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式______ 。
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式___________ 。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知:
①H2O(g)=H2(g)+1/2O2(g) ΔH=+241.8kJ·mol-1
②C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ•mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ•mol-1
填空:
(1)上述反应中属于吸热反应的是_______ (填序号)。
(2)表示C的燃烧热的热化学方程式为_______ (填序号)。
(3)10g H2完全燃烧生成水蒸气,放出的热量为_______ 。
(4)写出CO燃烧的热化学方程式_______ 。
(5)计算反应C(s)+H2O(g)=H2(g)+CO(g)的ΔH=_______ 。
①H2O(g)=H2(g)+1/2O2(g) ΔH=+241.8kJ·mol-1
②C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ•mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ•mol-1
填空:
(1)上述反应中属于吸热反应的是
(2)表示C的燃烧热的热化学方程式为
(3)10g H2完全燃烧生成水蒸气,放出的热量为
(4)写出CO燃烧的热化学方程式
(5)计算反应C(s)+H2O(g)=H2(g)+CO(g)的ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是___ (请填序号)。
(2)H2的燃烧热为__ ;C的燃烧热为_____ 。
(3)燃烧10 g H2生成液态水,放出的热量为___ 。
(4)CO的燃烧热为___ ;其热化学方程式为______ 。
(5) H2O(l) =H2O(g) ΔH=____ 。
①H2(g)+
 O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)CO的燃烧热为
(5) H2O(l) =H2O(g) ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】填空。
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:_______ 。
(2)火箭发射时可用肼( )为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知:
)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知: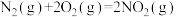
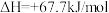 ;
;
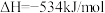 ;则
;则 和
和 反应的热化学方程式为
反应的热化学方程式为_______ 。
(3)根据下图写出热化学方程式_______ 。

(4)加入催化剂该反应的反应热 是否发生了改变
是否发生了改变_______ (填“是”或“否”)。
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
(2)火箭发射时可用肼(
 )为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知:
)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知: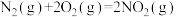
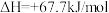 ;
;
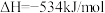 ;则
;则 和
和 反应的热化学方程式为
反应的热化学方程式为(3)根据下图写出热化学方程式

(4)加入催化剂该反应的反应热
 是否发生了改变
是否发生了改变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】目前煤在我国依然是第一能源,煤的气化可以实现煤的综合利用,提高煤的利用价值。
已知:煤气化反应为C(s) + H2O(g) = CO(g)+H2(g) ΔH
① C(s)+O2(g) = CO2(g) ΔH1=-393.5 kJ/mol
② CO(g)+ O2(g) = CO2(g) ΔH2=-283.0 kJ/mol
O2(g) = CO2(g) ΔH2=-283.0 kJ/mol
③ H2(g)+ O2(g) = H2O(g) ΔH3=-242.0 kJ/mol
O2(g) = H2O(g) ΔH3=-242.0 kJ/mol
(1)ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH =_______ ;ΔH = _______ kJ/mol。
(2)从两个不同的角度评价将煤转化为CO和H2再燃烧的优点是________ 。
已知:煤气化反应为C(s) + H2O(g) = CO(g)+H2(g) ΔH
① C(s)+O2(g) = CO2(g) ΔH1=-393.5 kJ/mol
② CO(g)+
 O2(g) = CO2(g) ΔH2=-283.0 kJ/mol
O2(g) = CO2(g) ΔH2=-283.0 kJ/mol③ H2(g)+
 O2(g) = H2O(g) ΔH3=-242.0 kJ/mol
O2(g) = H2O(g) ΔH3=-242.0 kJ/mol(1)ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH =
(2)从两个不同的角度评价将煤转化为CO和H2再燃烧的优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。
(1)已知:H2O(l)=H2O(g) △H=+44.0kJ•mol-1,甲烷完全燃烧与不完全燃烧的热效应如图所示。

CO的燃烧热△H=_______ kJ•mol-1。
(2)已知拆开1molH-H、1molN-H、1molN≡N化学键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(3)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如图。

①第二步反应的△H_______ 0(填“>”、“<”或“=”)。
②从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应。
(1)已知:H2O(l)=H2O(g) △H=+44.0kJ•mol-1,甲烷完全燃烧与不完全燃烧的热效应如图所示。

CO的燃烧热△H=
(2)已知拆开1molH-H、1molN-H、1molN≡N化学键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(3)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如图。

①第二步反应的△H
②从图像分析决定生产尿素的总反应的反应速率的步骤是第
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________ 。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________ 。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。

___________
②写出表示丙烷燃烧热的热化学方程式:_______________________________________ 。
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。

②写出表示丙烷燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知下列热化学方程式:
①H2(g) + O2(g) = H2O(l)△H = -285.8 kJ / mol
O2(g) = H2O(l)△H = -285.8 kJ / mol
②C(s) + O2(g) = CO2(g)△H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g)△H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是______ (填序号,下同),属于吸热反应的是____ 。
(2)1 mol H2完全燃烧生成液态水,放出的热量为____ kJ。
(3)写出下列反应的热化学方程式
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量;
_______________________________________________
②2 molCu(s) 与适量O2(g)反应生成CuO(s),放出314 kJ热量;
_______________________________________________
①H2(g) +
 O2(g) = H2O(l)△H = -285.8 kJ / mol
O2(g) = H2O(l)△H = -285.8 kJ / mol②C(s) + O2(g) = CO2(g)△H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g)△H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1 mol H2完全燃烧生成液态水,放出的热量为
(3)写出下列反应的热化学方程式
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量;
②2 molCu(s) 与适量O2(g)反应生成CuO(s),放出314 kJ热量;
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】请回答下列问题:
(1)①现有0.1mol/L的纯碱溶液,若用pH试纸测定溶液的pH,其正确的操作是_________ 。
②纯碱溶液呈碱性的原因是(用离子方程式表示)__________ 。
(2)①已知4.4g丙烷完全燃烧生成二氧化碳气体和液态水,并放出222.0kJ的热量,请写出反应的热化学方程式:______________ 。
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ/mol,实验测得甲烷与丙烷的混合气体1mol完全燃烧生成液态水和二氧化碳气体时,放热1776.7kJ,则混合气体中甲烷与丙烷的体积比为___________ 。
(1)①现有0.1mol/L的纯碱溶液,若用pH试纸测定溶液的pH,其正确的操作是
②纯碱溶液呈碱性的原因是(用离子方程式表示)
(2)①已知4.4g丙烷完全燃烧生成二氧化碳气体和液态水,并放出222.0kJ的热量,请写出反应的热化学方程式:
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ/mol,实验测得甲烷与丙烷的混合气体1mol完全燃烧生成液态水和二氧化碳气体时,放热1776.7kJ,则混合气体中甲烷与丙烷的体积比为
您最近一年使用:0次
【推荐1】I.金刚石和石墨燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
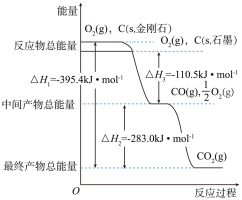
(1)在通常状况下,金刚石和石墨中____ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为____ 。
(2)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为____ kJ·mol-1。
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:____ 。
II.2SO2(g)+O2(g) 2SO3(g) ΔH=akJ·mol-1,反应过程的能量变化如图所示,已知1molSO2(g)完全转化为lmolSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ·mol-1,反应过程的能量变化如图所示,已知1molSO2(g)完全转化为lmolSO3(g)放热99kJ。请回答:
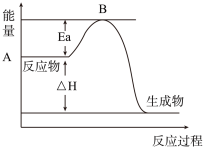
(4)a=____ kJ·mol-1。
(5)Ea的大小对该反应的ΔH____ (填“有”或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点____ (填“升高”、“降低”或“不变”)。
(6)III.由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=____ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)

(1)在通常状况下,金刚石和石墨中
(2)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:
II.2SO2(g)+O2(g)
 2SO3(g) ΔH=akJ·mol-1,反应过程的能量变化如图所示,已知1molSO2(g)完全转化为lmolSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ·mol-1,反应过程的能量变化如图所示,已知1molSO2(g)完全转化为lmolSO3(g)放热99kJ。请回答:
(4)a=
(5)Ea的大小对该反应的ΔH
(6)III.由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学键的键能是指气态原子间形成1 mol化学键时释放的能量。如H(g)+I(g)→H-I(g)放出297 kJ的能量,即H-I键的键能为297 kJ·mol-1,也可以理解为破坏1 mol H-I键需要吸收297 kJ的热量。下表是一些键能的数据(单位:kJ·mol-1)。
回答下列问题:
(1)一个化学反应的反应热(设反应物、生成物均为气态)与反应物和生成物中的键能之间有密切的关系。由表中数据计算下列热化学方程式中的热效应:H2(g)+Cl2(g)=2HCl(g) ΔH=_______ 。
(2)根据表中数据判断CCl4的稳定性_______ (填“大于”或“小于”)CF4的稳定性。
(3)试预测C-Br键的键能范围(填具体数值):_______ <C-Br键的键能<_______ 。
| 共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 |
| H-H | 436 | Cl-Cl | 243 | H-Cl | 431 | H-O | 467 |
| S=S | 255 | H-S | 339 | C-F | 427 | C-O | 358 |
| C-Cl | 330 | C-I | 218 | H-F | 565 | N≡N | 945 |
回答下列问题:
(1)一个化学反应的反应热(设反应物、生成物均为气态)与反应物和生成物中的键能之间有密切的关系。由表中数据计算下列热化学方程式中的热效应:H2(g)+Cl2(g)=2HCl(g) ΔH=
(2)根据表中数据判断CCl4的稳定性
(3)试预测C-Br键的键能范围(填具体数值):
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】按要求书写
(1)氨气的电子式:___________ ,乙炔的结构简式:_____________ ;
(2)工业上利用乙烯催化水化法制取乙醇,化学反应方程式:_____________ 反应类型:____________ ;
(3)苯与浓硝酸在50~60℃下发生硝化反应:__________ ,反应类型:_____________ ;
(4)已知键能如下:
写出N2和H2合成NH3的热化学方程式:______ 。
(1)氨气的电子式:
(2)工业上利用乙烯催化水化法制取乙醇,化学反应方程式:
(3)苯与浓硝酸在50~60℃下发生硝化反应:
(4)已知键能如下:
化学键 | H-H | N-N | N-H | N |
键能/kJ·mol-1 | 432 | 247 | 389 | 942 |
写出N2和H2合成NH3的热化学方程式:
您最近一年使用:0次

 N
N

