名校
解题方法
1 . 常温下,下列有关电解质溶液的说法不正确 的是
A.向Na2CO3溶液中通入NH3,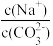 减小 减小 |
B.将0.1 mol·L-1的K2C2O4溶液从25 ℃升温至35 ℃,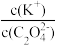 增大 增大 |
C.向0.1 mol·L-1的HF溶液中滴加NaOH溶液至中性, =1 =1 |
D.向0.1 mol·L-1的CH3COONa溶液中加入少量水,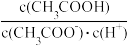 增大 增大 |
您最近一年使用:0次
2022-03-23更新
|
554次组卷
|
17卷引用:广西防城港市2018届高三1月模拟考试理综化学试题
广西防城港市2018届高三1月模拟考试理综化学试题安徽省长丰县双墩中学2018-2019学年高二上学期期末调研化学试题【全国百强校】山西省山西大学附属中学2019届高三上学期9月模块诊断化学试题安徽省肥东县第二中学2019-2020学年高二上学期期中考试化学试题备考突破2020高三化学专题强化集训——盐类水解中的三大守恒的应用夯基提能2020届高三化学选择题对题专练 ——选修四化学反应原理——电离平衡常数及其影响因素专练 (2)【百强校】天津市静海区第一中学2020届高三下学期第七周周末训练化学试题天津市实验中学2020届高三下学期4月第一次测试化学试题广东省云浮市2018-2019学年高二上学期期末考试化学试题甘肃省白银市第十中学2019-2020学年高二上学期期中考试化学试题解题达人.化学选择题(2021全国卷)巩固小卷02河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高三上学期期末考试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题安徽省桐城中学2022-2023学年高二上学期月考(1)化学试题河南省郑州市2021-2022学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第49练 盐类的水解
2 . 以下是某药物中间体D的合成过程:
A(C6H6O)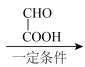 B
B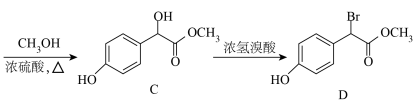
(1)A的结构简式为_________________ ,A转化为B的反应类型是____________ 。
(2)D中含氧官能团的名称是__________ 。
(3)鉴别B、C 可以用的试剂名称是______________ 。
(4)D在一定条件下与足量NaOH溶液反应的化学方程式是_________________ 。
(5)同时符合下到条件的D的所有同分异构体(不考虑立体异构)有________ 种。
①能与NaHCO3溶液反应产生气体;②苯环上只有2个取代基;③遇氯化铁溶液发生显色反应。其中核磁共振氢谱显示为5组峰,且峰面积比为3∶1∶2∶2∶1的同分异构体的结构简式是________________________________ (写结构简式)。
(6)已知:
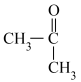 +CH≡CH
+CH≡CH 
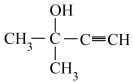
请设计合成路线以A和C2H2为原料合成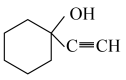 (无机试剂任选):
(无机试剂任选):____________ 。
A(C6H6O)
 B
B
(1)A的结构简式为
(2)D中含氧官能团的名称是
(3)鉴别B、C 可以用的试剂名称是
(4)D在一定条件下与足量NaOH溶液反应的化学方程式是
(5)同时符合下到条件的D的所有同分异构体(不考虑立体异构)有
①能与NaHCO3溶液反应产生气体;②苯环上只有2个取代基;③遇氯化铁溶液发生显色反应。其中核磁共振氢谱显示为5组峰,且峰面积比为3∶1∶2∶2∶1的同分异构体的结构简式是
(6)已知:
 +CH≡CH
+CH≡CH 

请设计合成路线以A和C2H2为原料合成
 (无机试剂任选):
(无机试剂任选):
您最近一年使用:0次
解题方法
3 . (1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表达式为________ 。
(2)2-巯基烟酸(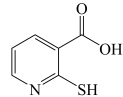 )水溶性优于2 –巯基烟酸氧钒配合物(
)水溶性优于2 –巯基烟酸氧钒配合物(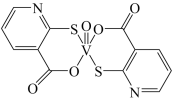 )的原因是
)的原因是___________________________________________________________________ 。
(3)各原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,下列物质中存在“离域π键”的是________ 。
A.SO2B.SO42-C.H2S D.CS2
(4)尿素(H2NCONH2)尿素分子中,原子杂化轨道类型有________ ,σ键与π键数目之比为________ 。
(5)氮化硼(BN )是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如左下图 )和六方氮化硼(如右下图),前者类似于金刚石,后者与石墨相似。

①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。左上图中原子坐标参数A为(0,0,0),D为( ,
, ,0),则E原子的坐标参数为
,0),则E原子的坐标参数为________ 。X-射线衍射实验测得立方氮化硼晶胞边长为361.5pm,则立方氮化硼晶体中N与B的原子半径之和为________ pm( =1.732)。
=1.732)。
②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表这式为________ pm。(已知正六边形面积为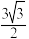 a2,a为边长)
a2,a为边长)
(2)2-巯基烟酸(
 )水溶性优于2 –巯基烟酸氧钒配合物(
)水溶性优于2 –巯基烟酸氧钒配合物( )的原因是
)的原因是(3)各原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,下列物质中存在“离域π键”的是
A.SO2B.SO42-C.H2S D.CS2
(4)尿素(H2NCONH2)尿素分子中,原子杂化轨道类型有
(5)氮化硼(BN )是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如左下图 )和六方氮化硼(如右下图),前者类似于金刚石,后者与石墨相似。

①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。左上图中原子坐标参数A为(0,0,0),D为(
 ,
, ,0),则E原子的坐标参数为
,0),则E原子的坐标参数为 =1.732)。
=1.732)。②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表这式为
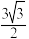 a2,a为边长)
a2,a为边长)
您最近一年使用:0次
4 . 冶金厂的炉渣中主要成分为CuO、Cu、Ag、Bi、Pb,还含有少量的SiO2和Au,从炉渣中回收有价金属的一种工艺流程如图所示。

回答下列问题:
(1)氧化浸取时加入H2O2的目的是__________________________ (只要回答出一点即可)。
(2)熔炼时加入Na2CO3的目的是除硅,该过程的化学方程式是_____________________________ 。
(3)加入NaOH溶液的目的是调节溶液的pH ,水解时通入水蒸气的目的是_______________________ 。
(4)流程中加入N2H4·H2O还原得到银的化学方程式是_____________________________ 。
(5)沉银和铅时,已知Ksp(AgCl)=1.8×10-10,Ksp(PbCl2)=1.8×10-5,当AgCl和PbCl2共沉且c(Pb2+)∶c(Ag+)=107时,溶液中的c(Cl-)=________ mol·L-1。
(6)用流程中得到的铅制取Pb(NO3)2。 用石墨作电极,电解Pb(NO3)2和Cu( NO3)2的混合溶液制取PbO2,阳极发生的电极反应式是_______________________ ,若电解液中不加入Cu( NO3)2,阴极反应式是______________________ ,这样做的主要缺点是____________________________________ 。

回答下列问题:
(1)氧化浸取时加入H2O2的目的是
(2)熔炼时加入Na2CO3的目的是除硅,该过程的化学方程式是
(3)加入NaOH溶液的目的是调节溶液的pH ,水解时通入水蒸气的目的是
(4)流程中加入N2H4·H2O还原得到银的化学方程式是
(5)沉银和铅时,已知Ksp(AgCl)=1.8×10-10,Ksp(PbCl2)=1.8×10-5,当AgCl和PbCl2共沉且c(Pb2+)∶c(Ag+)=107时,溶液中的c(Cl-)=
(6)用流程中得到的铅制取Pb(NO3)2。 用石墨作电极,电解Pb(NO3)2和Cu( NO3)2的混合溶液制取PbO2,阳极发生的电极反应式是
您最近一年使用:0次
5 . 亚硝酰氯是工业上重要的原料,是合成有机物的中间体。
2NO(g)+Cl2(g) 2ClNO(g) △H<0
2ClNO(g) △H<0
(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后NO的转化率α1=_______ 。其它条件保持不变,反应在恒压条件下进行,平衡时NO的转化率α2_______ α1(填“>”“<”或“=”)。
(2)若使反应2NO(g)+Cl2(g) 2ClNO(g) 的平衡常数增大,可采用的措施是
2ClNO(g) 的平衡常数增大,可采用的措施是_______ 。
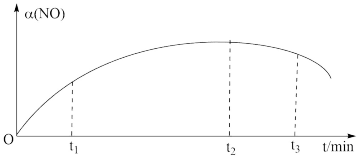
(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g) 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是_______ 。
(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g) 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
①V3_______ 2 (填写“大于”、“小于”或“等于”);
②容器Ⅱ中化学平衡常数K=_______ ;
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是_______ ;容器Ⅴ与容器Ⅰ的体积不同,则容器Ⅴ中反应达到平衡时气体总压强(P )的范围是_______ 。

2NO(g)+Cl2(g)
 2ClNO(g) △H<0
2ClNO(g) △H<0(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后NO的转化率α1=
(2)若使反应2NO(g)+Cl2(g)
 2ClNO(g) 的平衡常数增大,可采用的措施是
2ClNO(g) 的平衡常数增大,可采用的措施是(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g)
 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是
(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g)
 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:| 容器编号 | 温度/℃ | 容器体积/L | 平衡时ClNO含量(占比) |
| Ⅰ | T1 | 2 |  |
| Ⅱ | T2=T1 | 3 | W2 |
| Ⅲ | T3>T1 | V3 |  |
| Ⅳ | T4 | V4 | W4 |
| Ⅴ | T5 | V5 | W5 |
②容器Ⅱ中化学平衡常数K=
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是

您最近一年使用:0次
2018-03-31更新
|
222次组卷
|
2卷引用:广西防城港市2018届高三毕业班3月份模拟考试理综化学试题
名校
解题方法
6 . 二氧化硫是重要的化工原料,用途非常广泛。
实验一:SO2可以抑制细菌滋生,具有防腐功效。某实验小组欲用下图所示装置测定某品牌葡萄酒中(葡萄酒中含有乙醇、有机酸等)的SO2含量。
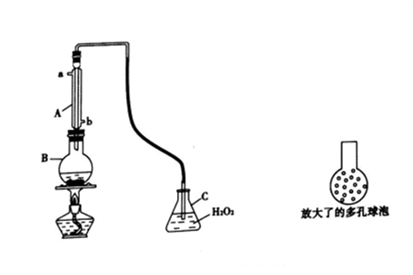
(1)仪器A的名称是________ ;使用该装置主要目的是____________________ 。
(2)B中加入 300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,C中化学方程式为_________________________________________ 。
(3)将输入C装置中的导管顶端改成具有多孔的球泡(如图所示)。可提高实验的准确度,理由是_______________________________________ 。
(4)除去C中的H2O2 然后用0.09mol·L-1NaOH标准溶液滴定。
①用碱式滴定管量取0.09mol·L-1NaOH标准溶液前的一步操作是___________________________ ;
②用该方法测定葡萄酒中SO2的含量偏高,主要原因是__________________________________ ,利用现有的装置,提出改进的措施是_______________________________________________ 。
(5)利用C中的溶液,有很多实验方案测定葡萄酒中SO2的含量。现有0.1mol·L-1BaCl2溶液,实验器材不限,简述实验步骤:________________________________ 。
实验一:SO2可以抑制细菌滋生,具有防腐功效。某实验小组欲用下图所示装置测定某品牌葡萄酒中(葡萄酒中含有乙醇、有机酸等)的SO2含量。

(1)仪器A的名称是
(2)B中加入 300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,C中化学方程式为
(3)将输入C装置中的导管顶端改成具有多孔的球泡(如图所示)。可提高实验的准确度,理由是
(4)除去C中的H2O2 然后用0.09mol·L-1NaOH标准溶液滴定。
①用碱式滴定管量取0.09mol·L-1NaOH标准溶液前的一步操作是
②用该方法测定葡萄酒中SO2的含量偏高,主要原因是
(5)利用C中的溶液,有很多实验方案测定葡萄酒中SO2的含量。现有0.1mol·L-1BaCl2溶液,实验器材不限,简述实验步骤:
您最近一年使用:0次
2018-03-31更新
|
217次组卷
|
2卷引用:广西防城港市2018届高三毕业班3月份模拟考试理综化学试题
7 . 若用AG表示溶液的酸度,其表达式为:AG=lg[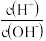 ]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是
]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是
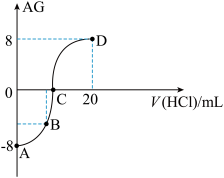
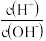 ]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是
]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是
| A.MOH电离方程式是MOH=M++OH- |
| B.C 点加入盐酸的体积为10mL |
| C.若B点加入的盐酸溶液体积为5 mL,所得溶液中:c(M+)+2c(H+)=c(MOH) + 2c(OH-) |
| D.滴定过程中从A点到D点溶液中水的电离程度逐渐增大 |
您最近一年使用:0次
8 . 微生物燃料电池在净化废水的同时能获得能源或得到有价值的化学产品,左下图为其工作原理,右下图为废水中Cr2O72-离子浓度与去除率的关系。下列说法不正确的是

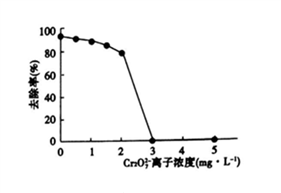


| A.正极反应式是O2+4H++4e-=2H2O,Cr2O72-+14H++6e-=2Cr3++7H2O |
| B.电池工作时,N极附近溶液pH增大 |
| C.处理1molCr2O72-时有6molH+从交换膜左侧向右侧迁移 |
| D.Cr2O72-离子浓度较大时,可能会造成还原菌失活 |
您最近一年使用:0次
9 . 前20号主族元素W、 X、Y 、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3 倍。X、Y 、Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。含有元素Z的盐的焰色反应为紫色。下到说法正确的是
| A.原子半径的大小W<X<Y<Z | B.简单氢化物的热稳定性W>X |
| C.Z的单质与水反应比Y的单质与水反应剧烈 | D.工业上通过电解W、Y组成的化合物制备单质Y |
您最近一年使用:0次
10 . 某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl- 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出)
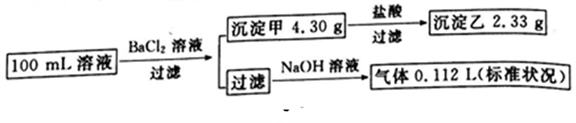
下列说法一定正确的是

下列说法一定正确的是
| A.溶液中一定含有Na+,Na+浓度是0.35mol/L |
| B.溶液中只有SO42-、CO32-、NH4+离子 |
| C.溶液中可能含有Cl- ,一定没有Fe3+ |
| D.取原溶液少许加入硝酸酸化的AgNO3溶液检验是否有Cl- |
您最近一年使用:0次



