1 . 常温下,在特制容器中加入20mL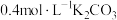 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
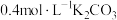 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
A.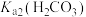 的数量级为 的数量级为 |
| B.滴定过程中,水的电离程度始终在减小 |
C.cd段反应的离子方程式为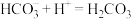 |
D.f点对应的溶液中存在: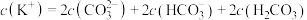 |
您最近一年使用:0次
2024-05-29更新
|
81次组卷
|
2卷引用:广西壮族自治区玉林市五校2023-2024学年高二下学期5月联考 化学试题
名校
2 . 工业上用废铁屑(含 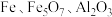 及少量泥沙)制取铁氧磁体,其生产工艺流程如图:
及少量泥沙)制取铁氧磁体,其生产工艺流程如图:
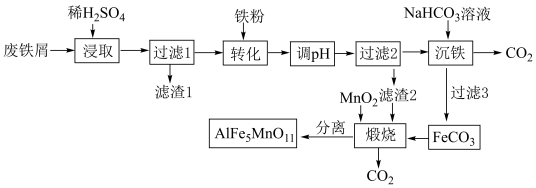
已知:各离子开始沉淀与完全沉淀的 如下:
如下:
请回答下列问题:
(1) 可表示为
可表示为 ,则
,则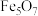 可用类似的氧化物形式表示为
可用类似的氧化物形式表示为_______ 。
(2)加快浸取速率的措施有(写1个)_______ ;滤渣1是_______ 。
(3)调 时最大不能超过
时最大不能超过_______ 。
(4)“转化”步骤中发生反应的离子方程式_______ ;“沉铁”步骤中发生反应的离子方程式_______ 。
(5)得到的 需要洗涤干净所吸附的离子,判断已洗涤干净的实验操作方法是
需要洗涤干净所吸附的离子,判断已洗涤干净的实验操作方法是_______ 。
(6)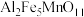 中
中 为
为 价,则其中含
价,则其中含 价的铁与
价的铁与 价的铁的物质的量之比为
价的铁的物质的量之比为_______ ;若生成 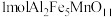 ,则电子转移
,则电子转移_______  。
。
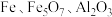 及少量泥沙)制取铁氧磁体,其生产工艺流程如图:
及少量泥沙)制取铁氧磁体,其生产工艺流程如图:
已知:各离子开始沉淀与完全沉淀的
 如下:
如下: |  |  | |
| 开始沉淀 | 7.2 | 1.5 | 3.5 |
| 完全沉淀 | 9.7 | 3.7 | 5.5 |
(1)
 可表示为
可表示为 ,则
,则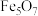 可用类似的氧化物形式表示为
可用类似的氧化物形式表示为(2)加快浸取速率的措施有(写1个)
(3)调
 时最大不能超过
时最大不能超过(4)“转化”步骤中发生反应的离子方程式
(5)得到的
 需要洗涤干净所吸附的离子,判断已洗涤干净的实验操作方法是
需要洗涤干净所吸附的离子,判断已洗涤干净的实验操作方法是(6)
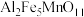 中
中 为
为 价,则其中含
价,则其中含 价的铁与
价的铁与 价的铁的物质的量之比为
价的铁的物质的量之比为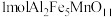 ,则电子转移
,则电子转移 。
。
您最近一年使用:0次
名校
解题方法
3 . Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图。
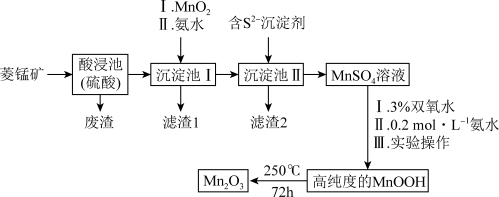
25℃时,相关物质的Ksp见表。
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为___________ 价。
(2)向“沉淀池Ⅰ”中加入MnO2,MnO2的作用是___________ ,在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为___________ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为___________ 。
(4)MnSO4转化为MnOOH中“Ⅲ实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为___________ 。
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。

①以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为___________ 。
②MnS晶胞结构如图所示,其中Mn的配位数为___________ 。
③已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为___________ pm(列出计算式即可)。

25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池Ⅰ”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“Ⅲ实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。

①以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为
②MnS晶胞结构如图所示,其中Mn的配位数为
③已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
您最近一年使用:0次
解题方法
4 . 氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。
(1)元素铬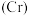 的几种化合物(化合物中氧元素均为
的几种化合物(化合物中氧元素均为 价)存在下列转化关系,
价)存在下列转化关系,


 溶液
溶液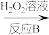
 溶液
溶液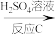
 溶液
溶液
① 中铬元素化合价为
中铬元素化合价为_______ ,上述过程属于氧化还原反应的是________ (填字母)。
②已知B反应中 只发生如下过程:
只发生如下过程: ,则B反应被还原的元素是
,则B反应被还原的元素是________ (填化学式),写出B反应的化学方程式________ , 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是________ 。
(2)近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为: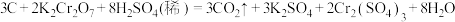 。
。
请回答下列问题。
①分析元素化合价可知该反应的氧化产物为___________ (填化学式)。
②根据化合价,推测 能和
能和___________ 反应(填标号)。
A. B.
B. C.
C. D.
D.
③ 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用 将酸性废液中的
将酸性废液中的 还原成
还原成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)化工厂常用浓氨水检验管道是否漏气,其原理为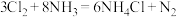 ,被氧化的
,被氧化的 与被还原的
与被还原的 的分子个数之比为
的分子个数之比为___________ 。
(1)元素铬
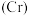 的几种化合物(化合物中氧元素均为
的几种化合物(化合物中氧元素均为 价)存在下列转化关系,
价)存在下列转化关系,

 溶液
溶液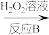
 溶液
溶液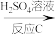
 溶液
溶液①
 中铬元素化合价为
中铬元素化合价为②已知B反应中
 只发生如下过程:
只发生如下过程: ,则B反应被还原的元素是
,则B反应被还原的元素是 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是(2)近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
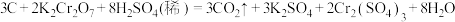 。
。请回答下列问题。
①分析元素化合价可知该反应的氧化产物为
②根据化合价,推测
 能和
能和A.
 B.
B. C.
C. D.
D.
③
 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用 将酸性废液中的
将酸性废液中的 还原成
还原成 ,反应的离子方程式为
,反应的离子方程式为(3)化工厂常用浓氨水检验管道是否漏气,其原理为
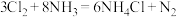 ,被氧化的
,被氧化的 与被还原的
与被还原的 的分子个数之比为
的分子个数之比为
您最近一年使用:0次
名校
5 . 某小组回收锌锰电池废料(主要含 、
、 等)制备高锰酸钾,简易流程如图所示。
等)制备高锰酸钾,简易流程如图所示。
 、
、 等)制备高锰酸钾,简易流程如图所示。
等)制备高锰酸钾,简易流程如图所示。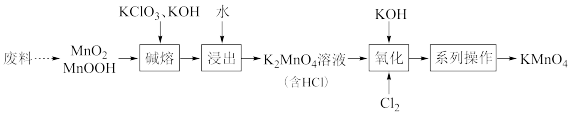
| A.“浸出”过程使用过滤操作,用到的玻璃仪器有:玻璃棒、烧杯、漏斗 |
B.“系列操作”中,进行高温干燥 |
C.“氧化”操作利用 氧化 氧化 制备 制备 ,可推知在碱性条件下 ,可推知在碱性条件下 氧化性大于 氧化性大于 |
D.“碱熔”的产物 是氧化产物 是氧化产物 |
您最近一年使用:0次
2023-11-09更新
|
515次组卷
|
6卷引用:广西玉林市2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
6 . 铟被广泛应用于电子工业、航空航天、太阳能电池新材料等高科技领域。从铜烟灰氧压酸浸渣(主要含 )中提取铟的工艺如图所示。
)中提取铟的工艺如图所示。
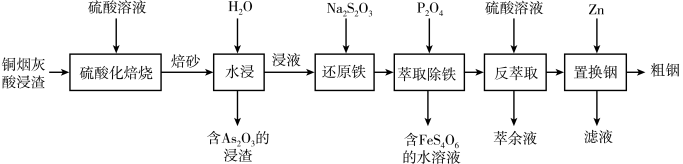
已知:①焙烧后金属元素均以硫酸盐的形式存在;② 微溶于水;③
微溶于水;③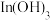 性质与
性质与 类似;④
类似;④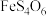 为强电解质。
为强电解质。
回答下列问题:
(1)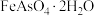 中铁元素化合价为
中铁元素化合价为 价,
价, 的化合价为
的化合价为_________ .
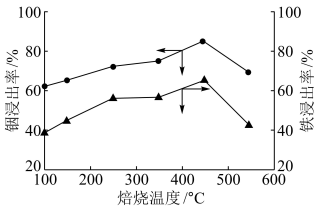
(2)“硫酸化焙烧”时,其他条件一定,焙烧温度对“水浸”时铟、铁浸出率的影响如图所示。适宜的焙烧温度是_________  。
。
(3)“水浸”工艺中的浸渣除了 外,还含有
外,还含有_________ .
(4)“还原铁”工艺反应的离子方程式为_________ .
(5)“萃取除铁”工艺中,用30%的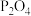 作萃取剂时,发现当溶液
作萃取剂时,发现当溶液 后,铟萃取率随
后,铟萃取率随 值的升高而下降,原因是
值的升高而下降,原因是_________ 。
(6)“置换铟”时,发现会有少量的气体 生成,
生成, 的电子式为
的电子式为_________ ,生成 的化学方程式为
的化学方程式为_________ 。
(7)整个工艺流程中,可循环利用的溶液是_________ .
 )中提取铟的工艺如图所示。
)中提取铟的工艺如图所示。
已知:①焙烧后金属元素均以硫酸盐的形式存在;②
 微溶于水;③
微溶于水;③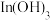 性质与
性质与 类似;④
类似;④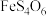 为强电解质。
为强电解质。回答下列问题:
(1)
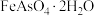 中铁元素化合价为
中铁元素化合价为 价,
价, 的化合价为
的化合价为(2)“硫酸化焙烧”时,其他条件一定,焙烧温度对“水浸”时铟、铁浸出率的影响如图所示。适宜的焙烧温度是
 。
。
(3)“水浸”工艺中的浸渣除了
 外,还含有
外,还含有(4)“还原铁”工艺反应的离子方程式为
(5)“萃取除铁”工艺中,用30%的
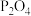 作萃取剂时,发现当溶液
作萃取剂时,发现当溶液 后,铟萃取率随
后,铟萃取率随 值的升高而下降,原因是
值的升高而下降,原因是(6)“置换铟”时,发现会有少量的气体
 生成,
生成, 的电子式为
的电子式为 的化学方程式为
的化学方程式为(7)整个工艺流程中,可循环利用的溶液是
您最近一年使用:0次
名校
解题方法
7 . 已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳;在空气中加热则生成氧化铁和二氧化碳。某化学兴趣小组用下图所示的装置模拟炼铁过程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量),

实验过程中,先打开 通入一氧化碳再加热;装置
通入一氧化碳再加热;装置 中固体质量不再减少后,停止加热,待装置
中固体质量不再减少后,停止加热,待装置 冷却到室温后关闭
冷却到室温后关闭 。实验测得装置
。实验测得装置 中固体减少了
中固体减少了 ,装置
,装置 中液体质量增加了
中液体质量增加了 。回答下列问题:
。回答下列问题:
(1)仪器①的名称是___________ 。
(2)写出装置A中发生的一个反应的化学方程式___________ ;步骤“装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K”的目的是___________ 。
(3)能判断生成的二氧化碳全部被装置B吸收的依据是:装置B中质量增加且___________ 。
(4)若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a___________ (填)“>”、“=”或“<”)b。
(5)D处为收集尾气的装置,应选择___________ 装置(填“甲”、“乙”或“丙”)。
(6)碳酸亚铁在空气中加热则生成四氧化三铁和二氧化碳,该反应的化学方程式是___________ 。

实验过程中,先打开
 通入一氧化碳再加热;装置
通入一氧化碳再加热;装置 中固体质量不再减少后,停止加热,待装置
中固体质量不再减少后,停止加热,待装置 冷却到室温后关闭
冷却到室温后关闭 。实验测得装置
。实验测得装置 中固体减少了
中固体减少了 ,装置
,装置 中液体质量增加了
中液体质量增加了 。回答下列问题:
。回答下列问题:(1)仪器①的名称是
(2)写出装置A中发生的一个反应的化学方程式
(3)能判断生成的二氧化碳全部被装置B吸收的依据是:装置B中质量增加且
(4)若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a
(5)D处为收集尾气的装置,应选择
(6)碳酸亚铁在空气中加热则生成四氧化三铁和二氧化碳,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
8 . 已知H3PO4是一种三元中强酸。25℃时,向某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如图所示。下列说法正确的是
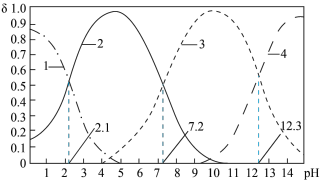

A.曲线2表示HPO ,曲线4表示PO ,曲线4表示PO |
B.25℃时,H3PO4的电离常数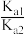 =10-5.1 =10-5.1 |
| C.pH=7.2时,溶液中由水电离出的c(H+)=10-6.8mol•L-1 |
D.pH=12.3时,溶液中5c(Na+)=2c(H3PO4)+2c(H2PO )+2c(HPO )+2c(HPO )+2c(PO )+2c(PO ) ) |
您最近一年使用:0次
2023-10-15更新
|
1259次组卷
|
5卷引用:广西玉林市2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
9 . 下列有关实验现象和解释或结论都正确的组合是
| 选项 | 实验操作 | 现象 | 解释或结论 |
A | 相同条件下,分别测量0.1molL1和0.01molL1醋酸溶液的导电性 | 前者的导电性强 | 醋酸浓度越大,电离程度越大 |
B | 向FeCl3和KSCN的混合溶液中加入KCl固体 | 血红色溶液变浅 | 增大KCl的浓度,使得平衡逆向移动 |
C | 两支试管各盛4mL0.1mol/L酸性高锰酸钾溶液,分别加入2mL0.1mol/L草酸溶液和2mL0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
D | 把充有NO2和N2O4的平衡球装置分别放入热水和冷水中 | 热水中颜色更深 | 其他条件不变时,温度升高,平衡向吸热反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-04更新
|
598次组卷
|
4卷引用:广西玉林市2023-2024学年高二上学期11月期中考试化学试题
10 . 酯类光刻胶K的一种合成路线如图所示。
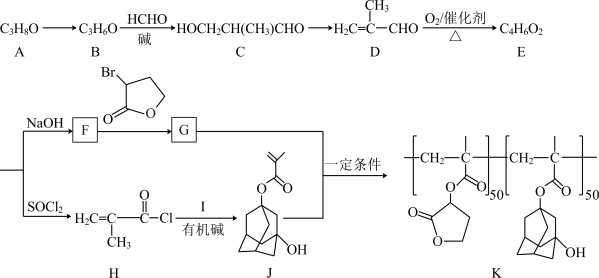
回答下列问题:
(1)J中含氧官能团的名称是_______ ;B→C的反应类型是_______ 。
(2)对C命名时,主官能团为醛基,羟基为取代基,则C的名称是_______ 。
(3)写出F→G的化学方程式:_______ 。
(4)已知I为二元醇,H→J中有机碱的作用是_______ 。
(5)L是E的同系物且Mr(L)-Mr(E)=14,L的结构有_______ 种(不包括立体异构体)。
(6)以乙醇为原料合成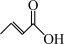 ,设计合成路线(无机试剂任选)
,设计合成路线(无机试剂任选)_______ 。

回答下列问题:
(1)J中含氧官能团的名称是
(2)对C命名时,主官能团为醛基,羟基为取代基,则C的名称是
(3)写出F→G的化学方程式:
(4)已知I为二元醇,H→J中有机碱的作用是
(5)L是E的同系物且Mr(L)-Mr(E)=14,L的结构有
(6)以乙醇为原料合成
 ,设计合成路线(无机试剂任选)
,设计合成路线(无机试剂任选)
您最近一年使用:0次



