解题方法
1 . 如图为某实验测得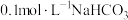 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线,
变化曲线,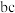 段有少量
段有少量 放出。下列说法正确的是
放出。下列说法正确的是
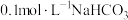 溶液在升温过程中(不考虑水挥发)的
溶液在升温过程中(不考虑水挥发)的 变化曲线,
变化曲线,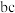 段有少量
段有少量 放出。下列说法正确的是
放出。下列说法正确的是
A. 点溶液的 点溶液的 等于 等于 点溶液的 点溶液的 |
B. 点时, 点时,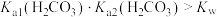 |
C. 点溶液中, 点溶液中,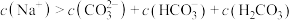 |
D. 段, 段, 减小说明升温抑制了 减小说明升温抑制了 的水解 的水解 |
您最近一年使用:0次
2 . 丙卡巴肼( )是一种抗癌前药,其合成路线如图所示:
)是一种抗癌前药,其合成路线如图所示:
请回答下列问题:
(1) 中含有的官能团名称为
中含有的官能团名称为___________ 。
(2)物质 的结构简式为
的结构简式为___________ 。
(3)化合物 的分子式为
的分子式为___________ 。
(4) 与足量
与足量 溶液反应的化学方程式是
溶液反应的化学方程式是___________ 。
(5)生成 的反应中
的反应中 的作用是
的作用是___________ 。
(6)在 的同分异构体中,同时满足下列条件的结构有
的同分异构体中,同时满足下列条件的结构有___________ 种(不考虑立体异构)。
①遇 溶液显色
溶液显色
②苯环上只有两种氢和两个取代基
③羟基不连在双键碳原子上
(7)参照上述合成路线,以甲苯为主要原料,设计制备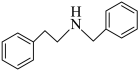 的合成路线:
的合成路线:___________ (无机试剂和图中试剂任选)。
 )是一种抗癌前药,其合成路线如图所示:
)是一种抗癌前药,其合成路线如图所示: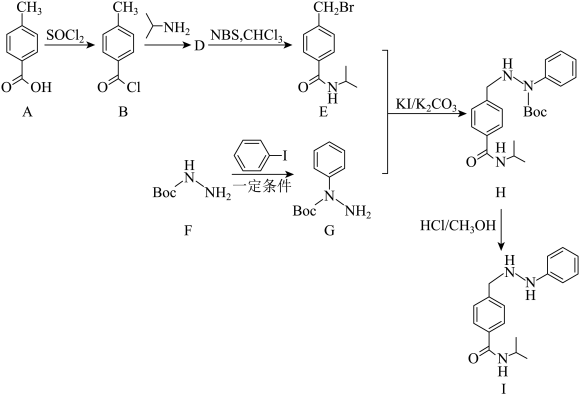
已知:①NBS的结构为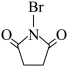

请回答下列问题:
(1)
 中含有的官能团名称为
中含有的官能团名称为(2)物质
 的结构简式为
的结构简式为(3)化合物
 的分子式为
的分子式为(4)
 与足量
与足量 溶液反应的化学方程式是
溶液反应的化学方程式是(5)生成
 的反应中
的反应中 的作用是
的作用是(6)在
 的同分异构体中,同时满足下列条件的结构有
的同分异构体中,同时满足下列条件的结构有①遇
 溶液显色
溶液显色②苯环上只有两种氢和两个取代基
③羟基不连在双键碳原子上
(7)参照上述合成路线,以甲苯为主要原料,设计制备
 的合成路线:
的合成路线:
您最近一年使用:0次
2024-05-31更新
|
99次组卷
|
2卷引用:2024届广西壮族自治区贵港市高三下学期模拟预测化学试题
解题方法
3 . 研究 的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
(1)在 加氢合成
加氢合成 的体系中,同时发生以下反应:
的体系中,同时发生以下反应:
反应 .
.

反应 .
.

反应 .
.
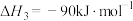
反应 的
的
___________  ,该反应在
,该反应在___________ (填“高温”、“低温”或“任意温度”)下能自发。
(2)向体积为1L的密闭容器中,投入 和
和 ,平衡时CO或
,平衡时CO或 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如图:
转化率随温度的变化如图: 的反应速率
的反应速率 ,
,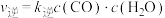 ,
, 、
、 为速率常数,c为物质的量浓度。
为速率常数,c为物质的量浓度。
①图中m代表的物质是___________ 。
②150~400℃范围内,随着温度升高, 的平衡产量的变化趋势是
的平衡产量的变化趋势是___________ 。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ;若p点时体系总压强为
;若p点时体系总压强为 ,反应
,反应 的
的
___________ (保留2位有效数字)。
④由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态,原因是___________ 。
(3)将 通入一定浓度的
通入一定浓度的 溶液至饱和,通电后在电极上反应生成
溶液至饱和,通电后在电极上反应生成 ,原理如图所示(阴、阳极区溶液均为
,原理如图所示(阴、阳极区溶液均为 溶液)。生成尿素的电极反应式为
溶液)。生成尿素的电极反应式为___________ 。
 的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。(1)在
 加氢合成
加氢合成 的体系中,同时发生以下反应:
的体系中,同时发生以下反应:反应
 .
.

反应
 .
.

反应
 .
.
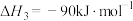
反应
 的
的
 ,该反应在
,该反应在(2)向体积为1L的密闭容器中,投入
 和
和 ,平衡时CO或
,平衡时CO或 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如图:
转化率随温度的变化如图: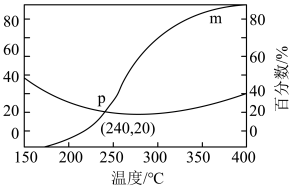
 的反应速率
的反应速率 ,
,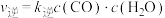 ,
, 、
、 为速率常数,c为物质的量浓度。
为速率常数,c为物质的量浓度。①图中m代表的物质是
②150~400℃范围内,随着温度升高,
 的平衡产量的变化趋势是
的平衡产量的变化趋势是③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ;若p点时体系总压强为
;若p点时体系总压强为 ,反应
,反应 的
的
④由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态,原因是
(3)将
 通入一定浓度的
通入一定浓度的 溶液至饱和,通电后在电极上反应生成
溶液至饱和,通电后在电极上反应生成 ,原理如图所示(阴、阳极区溶液均为
,原理如图所示(阴、阳极区溶液均为 溶液)。生成尿素的电极反应式为
溶液)。生成尿素的电极反应式为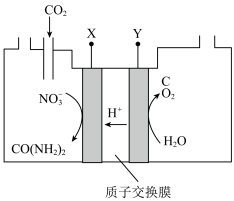
您最近一年使用:0次
解题方法
4 . 由重晶石矿(主要成分是 ,还含有
,还含有 等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如下。
等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如下。
 ,还含有
,还含有 等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如下。
等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如下。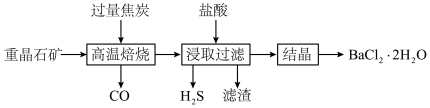
A.“高温焙烧”时焦炭和 发生反应,氧化剂与还原剂的物质的量之比为4:1 发生反应,氧化剂与还原剂的物质的量之比为4:1 |
| B.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
C.“浸取过滤”得到的滤渣为 |
| D.为提高产率,结晶得到的氯化钡晶体可用乙醇进行洗涤 |
您最近一年使用:0次
解题方法
5 . 南宁伊岭岩溶洞水体中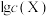 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示,
)与pH的关系如图所示,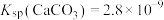 。下列说法错误的是
。下列说法错误的是
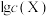 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示,
)与pH的关系如图所示,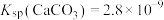 。下列说法错误的是
。下列说法错误的是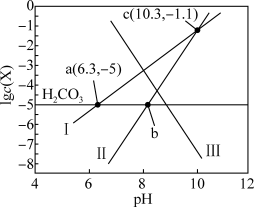
A.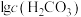 不变的原因是水体中的 不变的原因是水体中的 与空气中的 与空气中的 保持平衡 保持平衡 |
B.该温度下 与 与 为线性关系 为线性关系 |
C. 时, 时,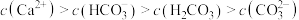 |
D.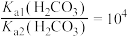 |
您最近一年使用:0次
解题方法
6 . 利用 和CO反应生成
和CO反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:
反应
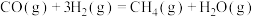
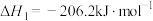
反应


向密闭容器中充入一定量 和CO发生上述反应,保持温度和容器体积一定,平衡时CO和
和CO发生上述反应,保持温度和容器体积一定,平衡时CO和 的转化率、
的转化率、 和
和 的产率及随起始
的产率及随起始 的变化情况如下图所示。
的变化情况如下图所示。 的产率
的产率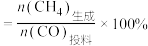 ,
, 的选择性
的选择性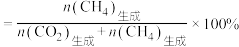 ]。
]。
下列说法错误的是
 和CO反应生成
和CO反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:反应

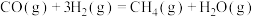
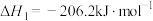
反应



向密闭容器中充入一定量
 和CO发生上述反应,保持温度和容器体积一定,平衡时CO和
和CO发生上述反应,保持温度和容器体积一定,平衡时CO和 的转化率、
的转化率、 和
和 的产率及随起始
的产率及随起始 的变化情况如下图所示。
的变化情况如下图所示。
 的产率
的产率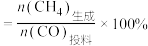 ,
, 的选择性
的选择性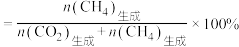 ]。
]。下列说法错误的是
A.曲线b表示 的转化率 的转化率 |
| B.当容器内气体总压强保持不变时,反应I、II均达到平衡状态 |
C.随着 增大, 增大, 的产率先增大后减小 的产率先增大后减小 |
D.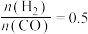 ,反应达平衡时, ,反应达平衡时, 的选择性为20% 的选择性为20% |
您最近一年使用:0次
解题方法
7 . 盐泥是氯碱工业的废渣,主要含镁、钙、铁、铝、锰的硅酸盐和碳酸盐,可用于提取 ,工艺流程如图所示:
,工艺流程如图所示: .常见氢氧化物的溶度积Ksp如下表:
.常见氢氧化物的溶度积Ksp如下表:
 .物质的溶解度S(g/100g水)
.物质的溶解度S(g/100g水)
(1)基态Fe原子价层电子轨道排布图为___________
(2)滤渣 的主要成分为
的主要成分为___________ (填化学式)。
(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是___________ 。
(4)滤渣 含有
含有 、写出生成
、写出生成 的离子反应方程式
的离子反应方程式___________ 。
(5)滤液 中
中
___________ 。
(6)从滤液 中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④
中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④___________ ,⑤过滤、洗涤得产品。
(7) 作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释
作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释 能结合
能结合 的原因:
的原因:___________ 。
 ,工艺流程如图所示:
,工艺流程如图所示:
 .常见氢氧化物的溶度积Ksp如下表:
.常见氢氧化物的溶度积Ksp如下表: |  |  |  |  |  |
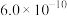 | 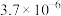 | 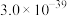 |  | 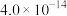 | 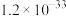 |
 .物质的溶解度S(g/100g水)
.物质的溶解度S(g/100g水)| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
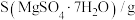 | 20.3 | 23.3 | 25.2 | 30.8 | 35.3 | 35.8 | 33.4 |
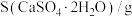 | 0.223 | 0.224 | 0.255 | 0.265 | 0.244 | 0.234 | 0.205 |
(1)基态Fe原子价层电子轨道排布图为
(2)滤渣
 的主要成分为
的主要成分为(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是
(4)滤渣
 含有
含有 、写出生成
、写出生成 的离子反应方程式
的离子反应方程式(5)滤液
 中
中
(6)从滤液
 中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④
中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④(7)
 作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释
作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释 能结合
能结合 的原因:
的原因: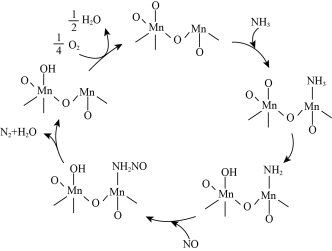
您最近一年使用:0次
解题方法
8 . 废旧锂离子电池的回收利用具有重要的经济和环境意义。一种将废旧锂离子电池的正极材料 转化为
转化为 的装置如图所示,工作时在厌氧细菌作用下,甲酸盐转化为
的装置如图所示,工作时在厌氧细菌作用下,甲酸盐转化为 。已知右侧装置为原电池,电极a、b、c本身均不参与反应。下列说法正确的是
。已知右侧装置为原电池,电极a、b、c本身均不参与反应。下列说法正确的是
 转化为
转化为 的装置如图所示,工作时在厌氧细菌作用下,甲酸盐转化为
的装置如图所示,工作时在厌氧细菌作用下,甲酸盐转化为 。已知右侧装置为原电池,电极a、b、c本身均不参与反应。下列说法正确的是
。已知右侧装置为原电池,电极a、b、c本身均不参与反应。下列说法正确的是
| A.装置工作时,b电极附近溶液pH逐渐减小 |
| B.电极a电势高于电极b,C室所用甲酸盐应为锂盐 |
| C.d电极的质量增加14g,b电极上生成22.4L气体 |
D.a电极反应式为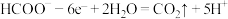 |
您最近一年使用:0次
解题方法
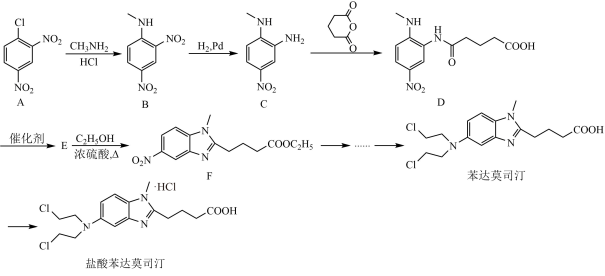
9 . 盐酸苯达莫司汀(Bendamustine)是一种抗癌药物。盐酸苯达莫司汀的一种合成路线如图: 的化学名称为
的化学名称为___________ ,B→C的反应类型为___________ 。
(2)D中碳原子的杂化为___________ ,F中含氧官能团的名称___________ 。
(3)E→F反应的化学方程式为___________ 。
(4)合成药物时将苯达莫司汀制成盐酸盐的目的可能是___________ 。
(5)链状有机物G是 的同分异构体,并且G能发生水解反应,1molG发生银镜反应后生成4mol单质Ag,符合上述条件的G的结构有
的同分异构体,并且G能发生水解反应,1molG发生银镜反应后生成4mol单质Ag,符合上述条件的G的结构有___________ 种(不考虑立体异构)。
(6)参照题干中的信息及已学知识,请写出以甲苯和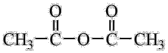 为原料,制
为原料,制 的合成路线图
的合成路线图___________ 。
 的化学名称为
的化学名称为(2)D中碳原子的杂化为
(3)E→F反应的化学方程式为
(4)合成药物时将苯达莫司汀制成盐酸盐的目的可能是
(5)链状有机物G是
 的同分异构体,并且G能发生水解反应,1molG发生银镜反应后生成4mol单质Ag,符合上述条件的G的结构有
的同分异构体,并且G能发生水解反应,1molG发生银镜反应后生成4mol单质Ag,符合上述条件的G的结构有(6)参照题干中的信息及已学知识,请写出以甲苯和
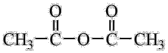 为原料,制
为原料,制 的合成路线图
的合成路线图
您最近一年使用:0次
名校
解题方法
10 . 以乙酸—4—甲基苯酚酯(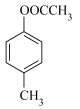 )为主要原料,可以合成重要的医药中间体H(
)为主要原料,可以合成重要的医药中间体H(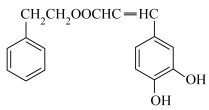 ),其合成线路如下:
),其合成线路如下:
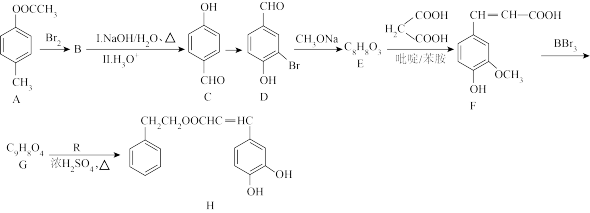
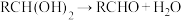 。
。②
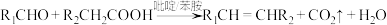 。
。③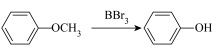
(1)C的化学名称为
(2)
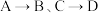 的反应类型相同,均属于
的反应类型相同,均属于 的反应条件为
的反应条件为(3)H中含氧官能团名称为
(4)
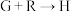 的化学方程式为
的化学方程式为(5)M是R的同分异构体,遇氯化铁溶液发生显色反应,则符合条件的M的结构可能有
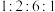 的结构简式为
的结构简式为
您最近一年使用:0次
2024-05-06更新
|
164次组卷
|
4卷引用:广西壮族自治区贵港市2024届高三下学期收网考化学试题
广西壮族自治区贵港市2024届高三下学期收网考化学试题2024届山西省晋中市平遥县第二中学校高三下学期冲刺调研押题卷理综(二)-高中化学(已下线)江苏省淮安市淮海中学2024届高三下学期第三次模拟考试化学试题2024届山西省晋城市第一中学校高三下学期模拟预测理综试题-高中化学



