解题方法
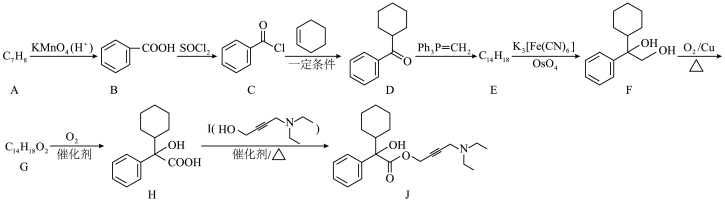
1 . 化合物J可用于治疗原发性血小板减少症、血小板无力症等,其合成路线如下:
(1)A的化学名称是___________ ;J中含氧官能团的名称为___________ 。
(2)H→J的反应类型为___________ 。
(3)已知—Ph表示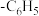 ,由D生成E的反应为
,由D生成E的反应为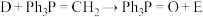 ,则E的结构简式是
,则E的结构简式是___________ 。
(4)F→G的化学方程式是___________ 。
(5)X是相对分子质量比C大14的同系物,满足下列条件的X的同分异构体有___________ 种(不考虑立体异构)。
①属于芳香族化合物;
②能发生银镜反应。
其中,核磁共振氢谱中有4组峰且峰面积之比为 的结构简式为
的结构简式为___________ (任写一种)。
(6)参考上述信息,写出以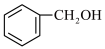 和
和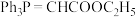 为原料制备
为原料制备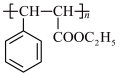 的路线:
的路线:___________ (其他试剂任选)。
(1)A的化学名称是
(2)H→J的反应类型为
(3)已知—Ph表示
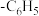 ,由D生成E的反应为
,由D生成E的反应为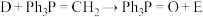 ,则E的结构简式是
,则E的结构简式是(4)F→G的化学方程式是
(5)X是相对分子质量比C大14的同系物,满足下列条件的X的同分异构体有
①属于芳香族化合物;
②能发生银镜反应。
其中,核磁共振氢谱中有4组峰且峰面积之比为
 的结构简式为
的结构简式为(6)参考上述信息,写出以
 和
和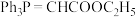 为原料制备
为原料制备 的路线:
的路线:
您最近一年使用:0次
2 . 2023年第19届杭州亚运会上,主火炬塔的燃料首次使用废碳再生的绿色甲醇,实现循环内的零排放,这也是首次在大型体育赛事上使用这种绿色燃料。回答下列问题:
(1)已知:①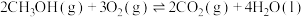

②

③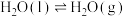

则 的反应热
的反应热
___________  (用含
(用含 、
、 、
、 的代数表示)。
的代数表示)。
(2)在恒容的密闭体系中进行反应 。下列示意图正确且能说明该反应进行到
。下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是___________ (填标号)。
时刻达到平衡状态的是___________ (填标号)。
(3) 的反应历程如图所示(吸附在催化剂表面的物质用*标注,如*
的反应历程如图所示(吸附在催化剂表面的物质用*标注,如* 表示
表示 吸附在催化剂表面;图中*H已省略)
吸附在催化剂表面;图中*H已省略)
___________ eV。
②下列措施有利于提高平衡时 转化率的有
转化率的有___________ (填标号)。
a.使用更高效的催化剂 b.加压 c.增大 的初始投入量
的初始投入量
(4)恒压下,将 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ:
混合,在不同催化剂作用下发生反应Ⅰ: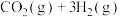

 和反应Ⅱ:
和反应Ⅱ:
 ,在相同时间段内
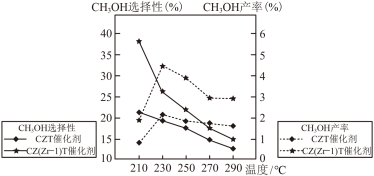
,在相同时间段内 的选择性和产率随温度的变化如图(其中,
的选择性和产率随温度的变化如图(其中, 的选择性=
的选择性=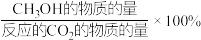 )。
)。 的产率随温度升高而降低的原因可能是
的产率随温度升高而降低的原因可能是___________ 。
②恒压下,通过上述过程合成甲醇的适宜条件是___________ (填标号)。
A.210℃ B.230℃ C.催化剂CZT D.催化剂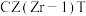
(5)一定条件下,将2mol 和4mol
和4mol  充入密闭容器中,发生反应:
充入密闭容器中,发生反应: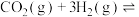
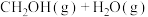 ,
, 的平衡转化率与温度、平衡总压强的关系如图所示。
的平衡转化率与温度、平衡总压强的关系如图所示。 、
、 、
、 由大到小的顺序为
由大到小的顺序为___________ 。
②在 条件下255℃时,该反应的压强平衡常数
条件下255℃时,该反应的压强平衡常数
___________  (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)已知:①
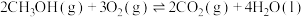

②


③
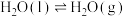

则
 的反应热
的反应热
 (用含
(用含 、
、 、
、 的代数表示)。
的代数表示)。(2)在恒容的密闭体系中进行反应
 。下列示意图正确且能说明该反应进行到
。下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是___________ (填标号)。
时刻达到平衡状态的是___________ (填标号)。A. | B.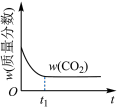 |
C.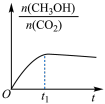 | D.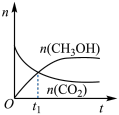 |
(3)
 的反应历程如图所示(吸附在催化剂表面的物质用*标注,如*
的反应历程如图所示(吸附在催化剂表面的物质用*标注,如* 表示
表示 吸附在催化剂表面;图中*H已省略)
吸附在催化剂表面;图中*H已省略)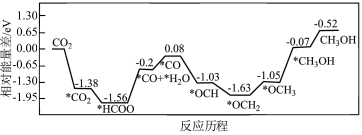

②下列措施有利于提高平衡时
 转化率的有
转化率的有a.使用更高效的催化剂 b.加压 c.增大
 的初始投入量
的初始投入量(4)恒压下,将
 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ:
混合,在不同催化剂作用下发生反应Ⅰ: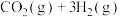

 和反应Ⅱ:
和反应Ⅱ:
 ,在相同时间段内
,在相同时间段内 的选择性和产率随温度的变化如图(其中,
的选择性和产率随温度的变化如图(其中, 的选择性=
的选择性=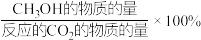 )。
)。
 的产率随温度升高而降低的原因可能是
的产率随温度升高而降低的原因可能是②恒压下,通过上述过程合成甲醇的适宜条件是
A.210℃ B.230℃ C.催化剂CZT D.催化剂
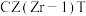
(5)一定条件下,将2mol
 和4mol
和4mol  充入密闭容器中,发生反应:
充入密闭容器中,发生反应: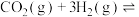
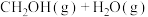 ,
, 的平衡转化率与温度、平衡总压强的关系如图所示。
的平衡转化率与温度、平衡总压强的关系如图所示。
 、
、 、
、 由大到小的顺序为
由大到小的顺序为②在
 条件下255℃时,该反应的压强平衡常数
条件下255℃时,该反应的压强平衡常数
 (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
3 . 废钼催化剂中钼、钴、镍等有价金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如图:
等)中回收有价金属的工艺流程如图:
(1)基态Mo原子的价层电子排布式为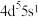 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为___________ 。
(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,这样做的优点是___________ ;“焙烧”时生成的气体A的主要成分为___________ 。 转化为
转化为 ,写出“碱浸”时
,写出“碱浸”时 参与反应的离子方程式:
参与反应的离子方程式:___________ 。
(4)已知 和
和 不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是
不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是___________ 。
(5)已知: ,“除铁”后所得滤液中
,“除铁”后所得滤液中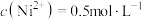 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中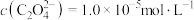 ,则沉镍率=
,则沉镍率=___________ [沉镍率=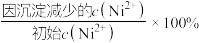 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。
(6) 在加热过程中会生成
在加热过程中会生成 ,已知
,已知 中钴显+2价和+3价,
中钴显+2价和+3价, 晶体的晶胞结构如图所示,则顶点上的离子为
晶体的晶胞结构如图所示,则顶点上的离子为___________ (用离子符号表示)。
 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如图:
等)中回收有价金属的工艺流程如图: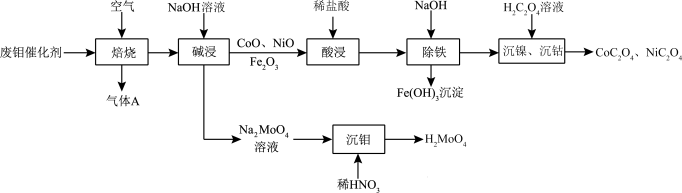
(1)基态Mo原子的价层电子排布式为
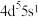 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,这样做的优点是

 转化为
转化为 ,写出“碱浸”时
,写出“碱浸”时 参与反应的离子方程式:
参与反应的离子方程式:(4)已知
 和
和 不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是
不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是(5)已知:
 ,“除铁”后所得滤液中
,“除铁”后所得滤液中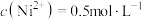 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中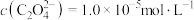 ,则沉镍率=
,则沉镍率=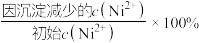 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。(6)
 在加热过程中会生成
在加热过程中会生成 ,已知
,已知 中钴显+2价和+3价,
中钴显+2价和+3价, 晶体的晶胞结构如图所示,则顶点上的离子为
晶体的晶胞结构如图所示,则顶点上的离子为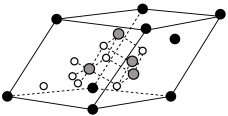
您最近一年使用:0次
名校
解题方法
4 . 以乙酸—4—甲基苯酚酯(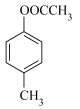 )为主要原料,可以合成重要的医药中间体H(
)为主要原料,可以合成重要的医药中间体H(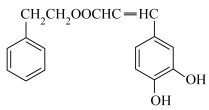 ),其合成线路如下:
),其合成线路如下:
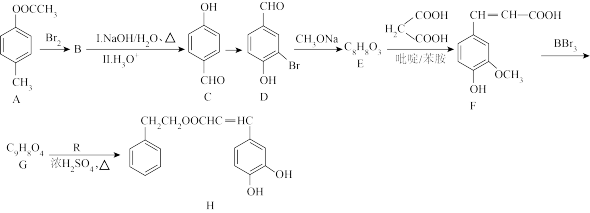
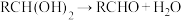 。
。②
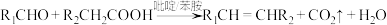 。
。③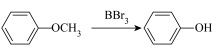
(1)C的化学名称为
(2)
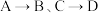 的反应类型相同,均属于
的反应类型相同,均属于 的反应条件为
的反应条件为(3)H中含氧官能团名称为
(4)
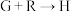 的化学方程式为
的化学方程式为(5)M是R的同分异构体,遇氯化铁溶液发生显色反应,则符合条件的M的结构可能有
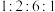 的结构简式为
的结构简式为
您最近一年使用:0次
2024-05-06更新
|
164次组卷
|
3卷引用:广西壮族自治区贵港市2024届高三下学期收网考化学试题
广西壮族自治区贵港市2024届高三下学期收网考化学试题2024届山西省晋中市平遥县第二中学校高三下学期冲刺调研押题卷理综(二)-高中化学(已下线)江苏省淮安市淮海中学2024届高三下学期第三次模拟考试化学试题
名校
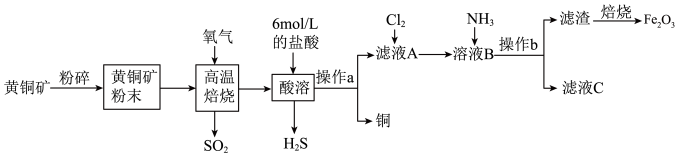
5 . Cu和Fe2O3在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价,Fe为+2价)制取Cu和Fe2O3的工艺流程如图所示:__________ 。
(2)CuFeS2中S元素的化合价是______ ,高温焙烧时生成FeS及另外两种产物,则发生的化学反应方程式为____________ 。
(3)操作a为____________ 。
(4)向滤液A中通入Cl2的目的是__________ 。
(5)向溶液B中通入NH3发生反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
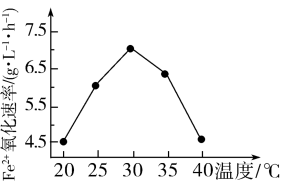
由下图可知,使用硫杆菌的最佳温度为______ ℃,若反应温度过高,反应速率下降,其原因是_______________ 。
(2)CuFeS2中S元素的化合价是
(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O由下图可知,使用硫杆菌的最佳温度为
您最近一年使用:0次
6 . 下列实验、现象与结论不对应的一组是
| 选项 | 实验 | 现象 | 结论 |
| A | 向某溶液滴加盐酸,无明显现象,再加BaCl2溶液 | 产生白色沉淀 | 溶液中含有 |
| B | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有 |
| C | 向某溶液中滴加稀盐酸,将产生的气体通入澄清石灰水中 | 澄消石灰水变浑浊 | 该溶液中不一定含有 |
| D | 用洁净的铂丝蘸取某溶液在酒精灯外焰上灼烧 | 观察不到紫色 | 溶液中一定没有钾元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 某化学小组同学对FeCl3溶液与Na2SO3溶液的反应进行探究
(1)请用离子方程式表示Na2SO3溶液显碱性的原因___________ 。
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为___________ ,取反应后的溶液中加入K3[Fe(CN)6]溶液,观察到___________ (填现象),证实了此结论。
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因___________ 。
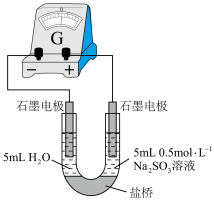
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入___________ ,观察到___________ (填实验现象),证实此浓度下的FeCl3溶液与Na2SO3溶液可以发生氧化还原反应。 可形成难电离的红色配合物:
可形成难电离的红色配合物: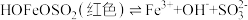 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因___________ 。
(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受___________ 因素影响(至少写出两项)。
| 实验操作 | 现象 | |
| ① |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,溶液变为淡黄色,始终无沉淀生成。 |
② |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,生成红褐色沉淀,上层清液为无色。 |
(1)请用离子方程式表示Na2SO3溶液显碱性的原因
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入
 可形成难电离的红色配合物:
可形成难电离的红色配合物: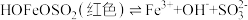 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受
您最近一年使用:0次
名校
8 . 将38.4g Cu与一定量浓硝酸恰好完全相互反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到 和
和 的混合溶液,反应过程及有关数据如图所示:
的混合溶液,反应过程及有关数据如图所示:
 和
和 的混合溶液,反应过程及有关数据如图所示:
的混合溶液,反应过程及有关数据如图所示:
| A.硝酸在反应中既体现氧化性又体现酸性 |
B.混合液中,含 、 、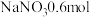 |
C.氮的氧化物混合物中 的物质的量是 的物质的量是 |
D.若浓硝酸体积为 ,则其物质的量浓度为 ,则其物质的量浓度为 |
您最近一年使用:0次
9 . 难溶盐  可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 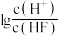 的关系如图所示,下列说法
的关系如图所示,下列说法错误 的是
 可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 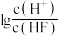 的关系如图所示,下列说法
的关系如图所示,下列说法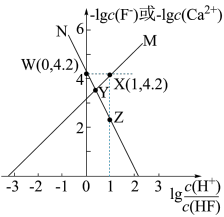
A.随着盐酸的加入, 不断溶解 不断溶解 |
B. 代表−lgc(F−)与 代表−lgc(F−)与 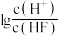 的变化曲线 的变化曲线 |
C.难溶盐  的溶度积常数Ksp(CaF2)=1.0×10−7.4 的溶度积常数Ksp(CaF2)=1.0×10−7.4 |
D. 点溶液中存在lgc(Ca2+)—2 点溶液中存在lgc(Ca2+)—2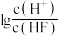 =—4.2 =—4.2 |
您最近一年使用:0次
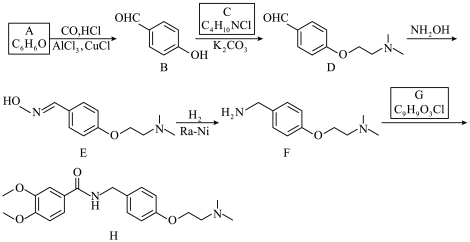
10 . 化合物H是合成盐酸伊托必利的中间体,其合成路线如下:
(1)H中含氧官能团的名称是___________ 。
(2)B的化学名称为___________ 。
(3)C的结构简式为___________ ,E→F的反应类型为___________ 。
(4)B转化为D的过程中, 的作用是
的作用是___________ 。
(5)E中氮原子的杂化方式为___________ 。
(6)G有多种同分异构体,符合下列条件的有___________ 种(不考虑立体异构),其中核磁共振氢谱有5组峰,峰面积比为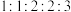 的结构简式为
的结构简式为___________ (写出一种)。
a.遇 溶液显紫色 b.与
溶液显紫色 b.与 溶液反应生成
溶液反应生成 c.苯环上有2个取代基
c.苯环上有2个取代基
(7)已知: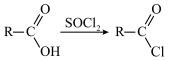 。利用题给相关信息,写出以甲苯和
。利用题给相关信息,写出以甲苯和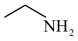 为原料合成
为原料合成 的路线图
的路线图___________ (合成过程中无机试剂任选)。
(1)H中含氧官能团的名称是
(2)B的化学名称为
(3)C的结构简式为
(4)B转化为D的过程中,
 的作用是
的作用是(5)E中氮原子的杂化方式为
(6)G有多种同分异构体,符合下列条件的有
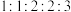 的结构简式为
的结构简式为a.遇
 溶液显紫色 b.与
溶液显紫色 b.与 溶液反应生成
溶液反应生成 c.苯环上有2个取代基
c.苯环上有2个取代基(7)已知:
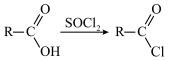 。利用题给相关信息,写出以甲苯和
。利用题给相关信息,写出以甲苯和 为原料合成
为原料合成 的路线图
的路线图
您最近一年使用:0次
2024-04-24更新
|
758次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型12 有机推断题(25题)-2024年高考化学常考点必杀300题(新高考通用)





