名校
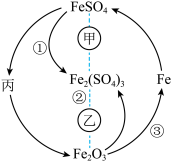
1 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近一年使用:0次
2024-04-21更新
|
168次组卷
|
2卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
2 .  是一种高效、安全消毒剂。目前已开发出多种电解法制取
是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取
气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入
;方法二:如图丙,电极上通入 
 酸性溶液中电解
酸性溶液中电解 制取
制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
(1)图甲中,操作Ⅰ、Ⅱ为_______ ,试剂 Ⅱ为_______ (填化学式)
(2)图乙中,电解精制饱和食盐水产生 的电极反应式为
的电极反应式为________ ;电解一段时间,若有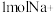 通过离子交换膜,在电极A上产生的气体体积(标准状况)为
通过离子交换膜,在电极A上产生的气体体积(标准状况)为______ L。
(3)图丙中,阴极电极反应式为_______ ;电解一段时间后,阴极区(溶液体积变化忽略不计 溶液的 pH
溶液的 pH______ (填“变大”、“变小”、“不变”)
(4)若以图丁所示电池作图乙的电源,则 a端与______ 相连(填 “e”或 “f”),图乙中阳极的另一产物可不断补充到图丁的正极区,该物质是_______ (填化学式)
(5)工业生产中,还可以用酸性 溶液还原
溶液还原 制得
制得 ,则每生成0.2mol
,则每生成0.2mol ,转移电子的数目为
,转移电子的数目为___________ 。
 是一种高效、安全消毒剂。目前已开发出多种电解法制取
是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取
气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入
;方法二:如图丙,电极上通入 
 酸性溶液中电解
酸性溶液中电解 制取
制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
(1)图甲中,操作Ⅰ、Ⅱ为
(2)图乙中,电解精制饱和食盐水产生
 的电极反应式为
的电极反应式为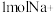 通过离子交换膜,在电极A上产生的气体体积(标准状况)为
通过离子交换膜,在电极A上产生的气体体积(标准状况)为(3)图丙中,阴极电极反应式为
 溶液的 pH
溶液的 pH(4)若以图丁所示电池作图乙的电源,则 a端与
(5)工业生产中,还可以用酸性
 溶液还原
溶液还原 制得
制得 ,则每生成0.2mol
,则每生成0.2mol ,转移电子的数目为
,转移电子的数目为
您最近一年使用:0次
2024-01-22更新
|
163次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期1月考试化学试卷
3 . 根据下列物质:① ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:
(1)以上物质中属于强电解质的是________ (填编号)
(2)常温,测得 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为___________ (结果保留一位小数)
(3)常温, ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。
(4)室温下,将三支装入含酚酞的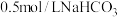 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:___________ ;一段时间后,甲烧杯试管中溶液颜色___________ (填“变深”、“变浅”、“不变”);结合方程式解释乙烧杯中加CaO后其试管内颜色变化的原因:__________ 。
(5)将1g 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
 ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:(1)以上物质中属于强电解质的是
(2)常温,测得
 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为(3)常温,
 ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。| A.向冰醋酸中加水,溶液的导电能力先增大后减小 |
B.向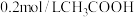 溶液中加水稀释, 溶液中加水稀释, 增大 增大 |
C.等温等浓度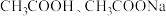 混合溶液中: 混合溶液中: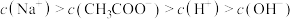 |
D.pH为3的 溶液中,水电离的 溶液中,水电离的 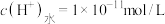 |
(4)室温下,将三支装入含酚酞的
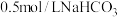 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:(5)将1g
 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下: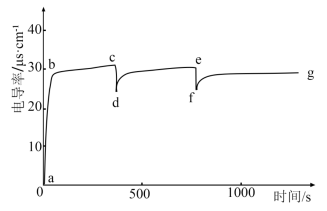
| A.c、e点电导率相等 |
| B.d、f点为饱和溶液 |
C.b→c电导率基本不变的原因是 到溶解平衡 到溶解平衡 |
| D.g点再加10mL蒸馏水可重复c→d、e→f图像 |
您最近一年使用:0次
2024-01-22更新
|
106次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期1月考试化学试卷
4 . 电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)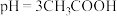 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的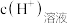 之比是
之比是___________ 。
(2)25℃时,将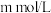 的醋酸和
的醋酸和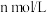 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中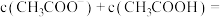
___________ ,m与n的大小关系是m___________ n(填“>”“=”或“<”)。
(3)将 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③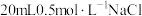 溶液④
溶液④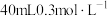 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是___________ (用字母表示)。
(4)氯化铁溶液蒸干并灼烧的产物是___________ ,原因是___________ 。
(5)25℃时,醋酸的电离常数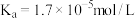 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
___________  (保留到小数点后一位)。
(保留到小数点后一位)。
(1)
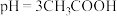 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的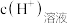 之比是
之比是(2)25℃时,将
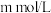 的醋酸和
的醋酸和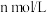 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中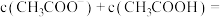
(3)将
 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③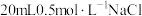 溶液④
溶液④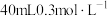 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是(4)氯化铁溶液蒸干并灼烧的产物是
(5)25℃时,醋酸的电离常数
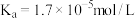 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
 (保留到小数点后一位)。
(保留到小数点后一位)。
您最近一年使用:0次
解题方法
5 . 某小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
【实验1】试剂:酸化的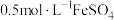 溶液(
溶液( ),
),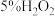 溶液(
溶液( )
)
(1)上述实验中 溶液与
溶液与 溶液反应的离子方程式是
溶液反应的离子方程式是_______ 。
(2)产生气泡的原因是_______ 。
【实验Ⅱ】试剂:未酸化的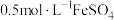 溶液(
溶液( ),
), 溶液(
溶液( )
)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加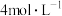 盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有
盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有 ,经检验还含有
,经检验还含有 。检验棕黄色沉淀中
。检验棕黄色沉淀中 的方法是
的方法是_______ 。
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ. 溶液氧化
溶液氧化 消耗
消耗
ⅱ. 氧化的产物发生了水解
氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是_______ 。
②实验验证假设ⅱ:取_______ ,加热,溶液变为红褐色, 下降,证明假设ⅱ成立。
下降,证明假设ⅱ成立。
(5)将 溶液加入
溶液加入 溶液后,产生红褐色胶体,反应的离子方程式是:
溶液后,产生红褐色胶体,反应的离子方程式是:_______ 。
 溶液的反应。
溶液的反应。【实验1】试剂:酸化的
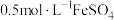 溶液(
溶液( ),
),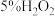 溶液(
溶液( )
)| 操作 | 现象 |
取 上述 上述 溶液于试管中,加入5滴 溶液于试管中,加入5滴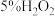 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与
溶液与 溶液反应的离子方程式是
溶液反应的离子方程式是(2)产生气泡的原因是
【实验Ⅱ】试剂:未酸化的
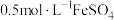 溶液(
溶液( ),
), 溶液(
溶液( )
)| 操作 | 现象 |
取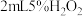 溶液于试管中,加入5滴上述 溶液于试管中,加入5滴上述 溶液 溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液 |
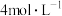 盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有
盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有 ,经检验还含有
,经检验还含有 。检验棕黄色沉淀中
。检验棕黄色沉淀中 的方法是
的方法是(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.
 溶液氧化
溶液氧化 消耗
消耗
ⅱ.
 氧化的产物发生了水解
氧化的产物发生了水解①根据实验Ⅱ记录否定假设ⅰ,理由是
②实验验证假设ⅱ:取
 下降,证明假设ⅱ成立。
下降,证明假设ⅱ成立。(5)将
 溶液加入
溶液加入 溶液后,产生红褐色胶体,反应的离子方程式是:
溶液后,产生红褐色胶体,反应的离子方程式是:
您最近一年使用:0次
2023-07-05更新
|
362次组卷
|
3卷引用:2024届广西桂林市高三下学期4月月考化学试卷
名校
解题方法
6 . 一碳产品是石油的良好替代品,一碳化学与绿色化工结合可以实现经济与环境的协调发展。甲醇-水蒸气重整制氢方法是目前比较成熟的制氢方法,且具有良好的应用前景。甲醇-水蒸气重整制氢的部分反应过程如图1所示:
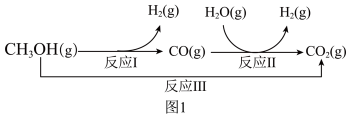
(1)已知一定条件下
反应I:CH3OH(g) ⇌CO(g)+2H2(g) ΔH1=+90.7kJ·mol-1
反应II:H2O(g)+CO(g) ⇌H2(g)+CO2(g) ΔH2=-41.2kJ·mol-1
反应III:CH3OH(g)+H2O(g) ⇌CO2(g)+3H2(g) ΔH3
该条件下反应III的ΔH3=_______ 。
(2)已知反应II在进气比[n(CO):n(H2O)]不同时,在不同温度(T1、T2)下,测得相应的CO的平衡转化率如图2所示。
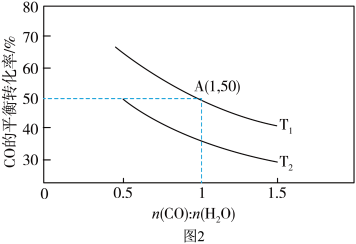
①比较T1、T2的大小,T1_______ T2(填“>”“<”或“=”)。原因为: _______
②T1温度时,按下表数据开始反应建立平衡:
应进行到t时刻时,判断v(正)、v(逆)的大小关系为断v(正)_______ v(逆(填“>“<”或“=”)。
(3)CO2在生产中有着广泛的用途。在弱酸性溶液中,电解活化CO2可以制备乙醇,原理如图所示。
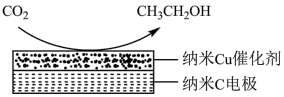
CO2参与反应的一极为_______ (填“阴极”或“阳极”),电极反应式是_______ 。

(1)已知一定条件下
反应I:CH3OH(g) ⇌CO(g)+2H2(g) ΔH1=+90.7kJ·mol-1
反应II:H2O(g)+CO(g) ⇌H2(g)+CO2(g) ΔH2=-41.2kJ·mol-1
反应III:CH3OH(g)+H2O(g) ⇌CO2(g)+3H2(g) ΔH3
该条件下反应III的ΔH3=
(2)已知反应II在进气比[n(CO):n(H2O)]不同时,在不同温度(T1、T2)下,测得相应的CO的平衡转化率如图2所示。

①比较T1、T2的大小,T1
②T1温度时,按下表数据开始反应建立平衡:
| CO | H2O | H2 | CO2 | |
| 起始浓度/(mol·L-1) | 2 | 1 | 0 | 0 |
| t时刻浓度/(mol·L-1) | 1.5 | 0.5 | 0.5 | 0.5 |
(3)CO2在生产中有着广泛的用途。在弱酸性溶液中,电解活化CO2可以制备乙醇,原理如图所示。
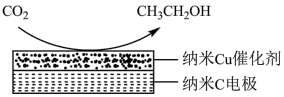
CO2参与反应的一极为
您最近一年使用:0次
名校
解题方法
7 . 钇是稀土元素之一。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),用NaOH初步处理钇矿石可以得到Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2的共熔物。工业上利用该共熔物制取氧化钇,并获得副产物铍,流程如图:
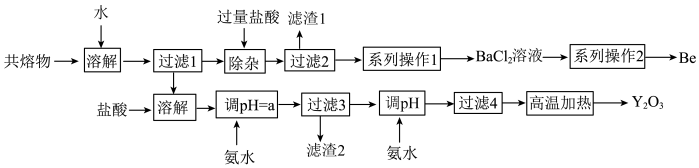
已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
(1)滤渣1的主要成分是_______ 。
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1_______ 。
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为_______ 。
(4)用氨水调节pH=a时,a的取值范围是_______ 。
(5)计算常温下Y3++3H2O Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=_______ 。(常温下Ksp[Y(OH)3]=8.0×10-23)
(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为_______ 。
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由_______ 。

已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为
(4)用氨水调节pH=a时,a的取值范围是
(5)计算常温下Y3++3H2O
 Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由
您最近一年使用:0次
解题方法
8 . 亚硝酸钠(NaNO2)主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用NOx表示)制备亚硝酸钠,简易流程如图。

已知:NO2+NO+Na2CO3=2NaNO2+CO2,2NO2+Na2CO3=NaNO2+NaNO3+CO2

(1)利用饱和NH4Cl溶液和饱和NaNO2溶液在加热条件下反应可制得N2,该反应的化学方程式为______ ;实验时装置B中应间断性通入适量的O2,其目的是______ 。
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是______ ;NO不能单独被纯碱溶液吸收,为了使NOx完全被纯碱溶液吸收且产品纯度最高,x=______ 。
(3)装置D的作用是______ ,采用“倒置漏斗”措施的目的是______ 。
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品(不含Na2CO3杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
上述实验______ (填标号)的结论不可靠,理由是______ 。经实验测得实验丙反应后的溶液中氮元素仅以NO 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为______ 。
(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯-比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
取0.001gNaNO2样品溶于蒸馏水配成1000mL稀溶液,取4.00mL该稀溶液测得吸光度为2.7000,对比标准曲线数据可知,该亚硝酸钠产品纯度为______ (列出计算式即可,已知1μg=10-6g)。

已知:NO2+NO+Na2CO3=2NaNO2+CO2,2NO2+Na2CO3=NaNO2+NaNO3+CO2

(1)利用饱和NH4Cl溶液和饱和NaNO2溶液在加热条件下反应可制得N2,该反应的化学方程式为
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是
(3)装置D的作用是
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品(不含Na2CO3杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 | HNO2是弱酸 |
| 乙 | 滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶液变蓝 | 酸性条件下NO 具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性KMnO4溶液中,振荡,酸性KMnO4溶液褪色 | 酸性条件NO 具有还原性 具有还原性 |
 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯-比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
| 标准使用液浓度/(μg•mL‑1) | 取标准液体积/mL | 相当于亚硝酸钠的质量/μg | 吸光度A |
| 1 | 4.00 | 4 | 2.7045 |
您最近一年使用:0次
解题方法
9 . 有下列物质:
①氢氧化钡②Al2(SO4)3③液态HCl④稀硫酸⑤二氧化碳⑥铁⑦碳酸钠⑧蔗糖⑨熔融氯化钠⑩
请回答下列问题:
(1)可以导电的有___________ (填序号)。
(2)属于电解质的有___________ (填序号)。
(3)属于非电解质的有___________ (填序号)。
(4)②在水中的电离方程式为___________ 。
(5)请写出④与⑦反应的离子方程式___________ 。
(6)请写出②与①反应的化学方程式___________ 。
①氢氧化钡②Al2(SO4)3③液态HCl④稀硫酸⑤二氧化碳⑥铁⑦碳酸钠⑧蔗糖⑨熔融氯化钠⑩

请回答下列问题:
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
(5)请写出④与⑦反应的离子方程式
(6)请写出②与①反应的化学方程式
您最近一年使用:0次
10 . 氮氧化物的有效去除和资源的充分利用是当今社会的重要研究课题。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) ΔH1 = -907.0 kJ•mol-1
4NH3(g) +3O2(g)=2N2(g)+6H2O(g) ΔH2= -1269.0 kJ•mol-1
若4NH3(g) +6NO(g) 5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为
5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为_______ kJ•mol-1 (用含E逆的代数式表示)。
(2)已知:①2NO(g)+2ICl(g) 2NOCl (g)+I2(g)
2NOCl (g)+I2(g)
②2NOCl(g) 2NO(g)+Cl2(g)
2NO(g)+Cl2(g)
③I2(g)+Cl2(g) 2ICl(g)
2ICl(g)
若向VL恒容密闭容器中加 2mol NO和 2mol ICl发生上述反应,达到平衡时,容器中 NOCl (g)为amol,Cl2(g)为b mol,此时 I2(g)的浓度为_______ mol•L-1(用含 a、b、V 的代数式表示,下同),反应③的平衡常数为_______ 。
(3)某化工厂排出的尾气(含 CO、N2O)治理的方法为在密闭容器中发生如下反应:CO(g)+N2O(g) CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:_______ 。
(4)已知4CO(g) +2NO2(g) 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行,为探究温度及不同催化剂对该反应的影响,保持其它初始条件不变重复实验,在相同时间内测得 N2产率与温度的关系如图所示。在催化剂乙作用下,图中 M 点对应的速率(对应温度400℃)v正_______ (填“>”、“<” 或“=”) v逆,温度高于400℃,N2产率降低的原因可能是_______ 。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) ΔH1 = -907.0 kJ•mol-1
4NH3(g) +3O2(g)=2N2(g)+6H2O(g) ΔH2= -1269.0 kJ•mol-1
若4NH3(g) +6NO(g)
 5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为
5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为(2)已知:①2NO(g)+2ICl(g)
 2NOCl (g)+I2(g)
2NOCl (g)+I2(g) ②2NOCl(g)
 2NO(g)+Cl2(g)
2NO(g)+Cl2(g)③I2(g)+Cl2(g)
 2ICl(g)
2ICl(g)若向VL恒容密闭容器中加 2mol NO和 2mol ICl发生上述反应,达到平衡时,容器中 NOCl (g)为amol,Cl2(g)为b mol,此时 I2(g)的浓度为
(3)某化工厂排出的尾气(含 CO、N2O)治理的方法为在密闭容器中发生如下反应:CO(g)+N2O(g)
 CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
(4)已知4CO(g) +2NO2(g)
 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
您最近一年使用:0次
2022-05-12更新
|
857次组卷
|
5卷引用:2024届广西桂林市高三下学期4月月考化学试卷
2024届广西桂林市高三下学期4月月考化学试卷天津市和平区2022届高三第二次质量调查化学试题湖南省邵东市第三中学2021-2022学年高三下学期5月月考化学试题湖南省祁东县育贤中学2022-2023学年高二上学期第一次月考化学试题(已下线)专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)



