 是一种高效、安全消毒剂。目前已开发出多种电解法制取
是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取
气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入
;方法二:如图丙,电极上通入 
 酸性溶液中电解
酸性溶液中电解 制取
制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
(1)图甲中,操作Ⅰ、Ⅱ为
(2)图乙中,电解精制饱和食盐水产生
 的电极反应式为
的电极反应式为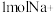 通过离子交换膜,在电极A上产生的气体体积(标准状况)为
通过离子交换膜,在电极A上产生的气体体积(标准状况)为(3)图丙中,阴极电极反应式为
 溶液的 pH
溶液的 pH(4)若以图丁所示电池作图乙的电源,则 a端与
(5)工业生产中,还可以用酸性
 溶液还原
溶液还原 制得
制得 ,则每生成0.2mol
,则每生成0.2mol ,转移电子的数目为
,转移电子的数目为
更新时间:2024-01-22 23:46:40
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
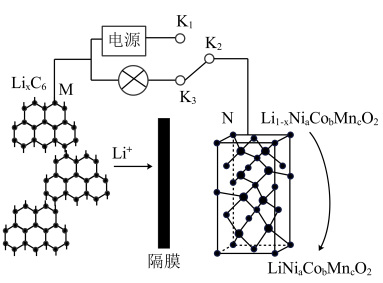
【推荐1】目前的新能源汽车多采用三元锂电池,某三元锂电池工作原理如图所示,该电池离子导体为有机锂盐溶液。
(1)锂离子电池的电极材料为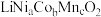 ,当
,当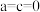 且
且 时该物质中Co元素的化合价为
时该物质中Co元素的化合价为_____________ , 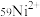 的中子数为31,1mol
的中子数为31,1mol 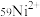 含有电子
含有电子_____________ mol。
(2)连接 、
、 时,N为
时,N为_____________ 极,电极电势高的电极发生_____________ (填“氧化”或“还原”)反应,被氧化的物质为_____________ (填化学式)。
(3)连接 、
、 时,N极的电极反应式为
时,N极的电极反应式为__________________ ,当外电路通过0.1mol电子时,通过隔膜的 质量为
质量为______ g。
(1)锂离子电池的电极材料为
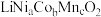 ,当
,当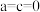 且
且 时该物质中Co元素的化合价为
时该物质中Co元素的化合价为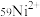 的中子数为31,1mol
的中子数为31,1mol 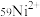 含有电子
含有电子(2)连接
 、
、 时,N为
时,N为(3)连接
 、
、 时,N极的电极反应式为
时,N极的电极反应式为 质量为
质量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】党的二十大报告提出,加强基础研究,突出原创,鼓励自由探索。一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。

(1)燃料电池放电过程中负极的电极反应式___________ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将___________ (填“增大”、“减小”或“不变”)。
(3)乙装置中物质A是___________ (填化学式);阴极的电极反应式是___________ 。
(4)若在标准状况下,甲装置有11.2LO2参加反应,则乙装置中转化SO2和NO的物质的量共有___________ mol;丙装置中阴极析出铜的质量为___________ g。

(1)燃料电池放电过程中负极的电极反应式
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(3)乙装置中物质A是
(4)若在标准状况下,甲装置有11.2LO2参加反应,则乙装置中转化SO2和NO的物质的量共有
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】现代生活离不开方便实用的化学电源。各种各样的化学电源都是依据原电池的原理制造的。回答下列问题:
(1)锂离子电池具有质量小、体积小、储存和输出能量大等特点。一种锂离子电池负极材料为嵌锂石墨,正极材料为 (钴酸锂),电解质溶液为
(钴酸锂),电解质溶液为 (六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为
(六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为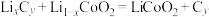 。
。
①放电时,负极反应式为______ 。 由
由______ 极向______ 极迁移(填“正”或“负”)。
②充电时,电池的______ (填“正”或“负”)极应与电源的正极相连,充电时该极的电极反应式为____________ 。
(2)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,DMFC的工作原理如图所示。
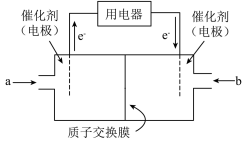
①通入a物质一侧的电极反应式为____________ 。
②通入11.2 L(折算为标准状况下)甲醇蒸气,测得电路中转移1.8 mol电子,则甲醇的利用率为______ 。
(3)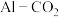 电池工作原理如图所示,利用该电池能有效地将
电池工作原理如图所示,利用该电池能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝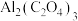 。
。
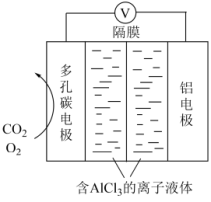
①电池的总反应式为____________ 。
②电池的正极反应式: (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 是催化剂,催化过程可表示为:
是催化剂,催化过程可表示为:
ⅰ.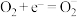 ⅱ.……
ⅱ.……
写出反应ⅱ的离子方程式:____________ 。
(1)锂离子电池具有质量小、体积小、储存和输出能量大等特点。一种锂离子电池负极材料为嵌锂石墨,正极材料为
 (钴酸锂),电解质溶液为
(钴酸锂),电解质溶液为 (六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为
(六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为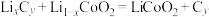 。
。①放电时,负极反应式为
 由
由②充电时,电池的
(2)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,DMFC的工作原理如图所示。

①通入a物质一侧的电极反应式为
②通入11.2 L(折算为标准状况下)甲醇蒸气,测得电路中转移1.8 mol电子,则甲醇的利用率为
(3)
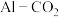 电池工作原理如图所示,利用该电池能有效地将
电池工作原理如图所示,利用该电池能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝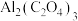 。
。
①电池的总反应式为
②电池的正极反应式:
 (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 是催化剂,催化过程可表示为:
是催化剂,催化过程可表示为:ⅰ.
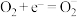 ⅱ.……
ⅱ.……写出反应ⅱ的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】将CO2还原为HCOOH是实现“碳中和”的有效途径。
(1)利用反应CO2(g)+H2(g)⇌HCOOH(g);ΔH =+14.9 kJ·mol-1不能实现CO2直接加氢合成HCOOH,原因是___________ 。
(2)CO2通过电解法转化为HCOO-的反应机理如图1。Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可让H2O自由通过。
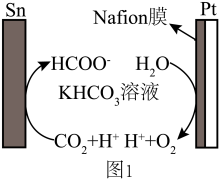
① Sn电极上生成HCOO-的电极反应式为___________ 。
② 电路中通过的电量与HCOO-产率的关系如图2所示。相同条件下,Pt电极有Nafion膜HCOO-产率明显提高,但电量>1000C后又显著下降,可能原因是___________ 。
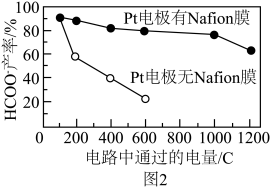
③ 若电解时将Nafion膜置于两个电极中间,保持电流恒定,20 h时向阳极区补充KHCO3,电压与时间关系如图3所示。0~20 h,电压增大的原因是___________ 。

(3)CO2电还原可能的反应机理如下图所示。Sn、In、Bi的活性位点对O的连接能力较强,Au、Cu的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附CO后不易脱离。
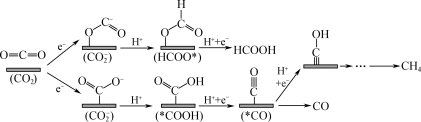
若还原产物主要为CH4时,应选择___________ (填“Sn”“Au”或“Cu”)作催化剂,简述分析过程:___________ 。
(1)利用反应CO2(g)+H2(g)⇌HCOOH(g);ΔH =+14.9 kJ·mol-1不能实现CO2直接加氢合成HCOOH,原因是
(2)CO2通过电解法转化为HCOO-的反应机理如图1。Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可让H2O自由通过。

① Sn电极上生成HCOO-的电极反应式为
② 电路中通过的电量与HCOO-产率的关系如图2所示。相同条件下,Pt电极有Nafion膜HCOO-产率明显提高,但电量>1000C后又显著下降,可能原因是

③ 若电解时将Nafion膜置于两个电极中间,保持电流恒定,20 h时向阳极区补充KHCO3,电压与时间关系如图3所示。0~20 h,电压增大的原因是

(3)CO2电还原可能的反应机理如下图所示。Sn、In、Bi的活性位点对O的连接能力较强,Au、Cu的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附CO后不易脱离。

若还原产物主要为CH4时,应选择
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH30.4mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量之差为17.3g。

(1)甲室中HCl、N2的质量之比为__________________ 。
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“________ ’’处(填数字,不考虑固体物质产生的压强),此时体系的平均相对分子质量为________ 。
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
(1)表中硫酸的质量分数为________ (不写单位,用含c1、ρ1,的代数式表示)。
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________ mol•L-1。
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度__________ 0.6c2 mol•L-1(填“大于”、“小于”或“等于”)(设混合后溶液的体积变化忽略不计)
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
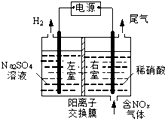
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:_________________________________ 。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为________ mol。

(1)甲室中HCl、N2的质量之比为
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量浓度/mol•L-1 | 溶液的密度/g•cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为
您最近一年使用:0次
【推荐3】氮氧化物是主要大气污染物,可采用多种方法消除,其中氢气选择性催化还原(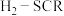 )是一种理想的方法。其相关反应如下:
)是一种理想的方法。其相关反应如下:
主反应:

副反应: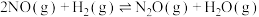

(1)已知:
 ,
,
 ,则
,则
_______ (用含有 和
和 的代数式表示)
的代数式表示)
(2)恒温条件下,将 、
、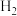 充入某恒容密闭容器中,在催化剂作用下进行反应。
充入某恒容密闭容器中,在催化剂作用下进行反应。
①下列有关说法错误 的是_______ 。(填字母序号)
a.当容器内的压强不再变化时说明主、副反应均达到平衡
b.平衡后,若向容器内再充入少量 ,主、副反应平衡常数均增大
,主、副反应平衡常数均增大
c.平衡后, 、
、 和
和 三者的物质的量之比保持不变
三者的物质的量之比保持不变
d.平衡后,
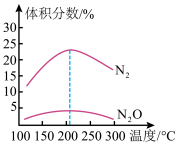
②在不同温度下,反应相同时间时测得混合气体中N2、 的体积分数随温度的变化关系如图所示,温度高于205℃时,
的体积分数随温度的变化关系如图所示,温度高于205℃时, 的体积分数随温度的升高而减小的原因可能
的体积分数随温度的升高而减小的原因可能_______ 。(答一点)
(3)某温度下,将 、
、 按物质的量比1:3充入某恒容密闭容器中,若平衡后
按物质的量比1:3充入某恒容密闭容器中,若平衡后 与
与 物质的量之比为3:1,
物质的量之比为3:1, 的转化率为80%,则
的转化率为80%,则 的有效去除率(转化为
的有效去除率(转化为 的
的 的量与起始量的比值)为
的量与起始量的比值)为_______ %, 的物质的量分数为
的物质的量分数为_______ %。(结果保留两位有效数字)
(4)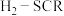 在
在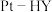 催化剂表面的反应机理如下图:
催化剂表面的反应机理如下图:
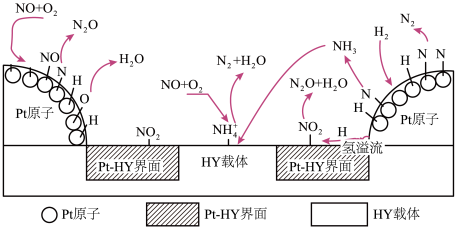
研究表明,在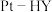 催化剂中,
催化剂中, 表面上形成的
表面上形成的 以
以 的形式被储存。随后在
的形式被储存。随后在 载体上,
载体上, 与
与 和
和 产生
产生 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。(已知发生反应的 、
、 物质的量之比为1:1)
物质的量之比为1:1)
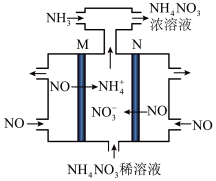
(5)除了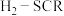 ,还有其他有效的方法消除氮氧化物,例如可用电解法将
,还有其他有效的方法消除氮氧化物,例如可用电解法将 转变为
转变为 ,其工作原理如图。M极为电解池的
,其工作原理如图。M极为电解池的_______ 极,N极的电极反应式为_______ 。
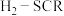 )是一种理想的方法。其相关反应如下:
)是一种理想的方法。其相关反应如下:主反应:


副反应:
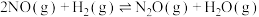

(1)已知:

 ,
,
 ,则
,则
 和
和 的代数式表示)
的代数式表示)(2)恒温条件下,将
 、
、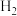 充入某恒容密闭容器中,在催化剂作用下进行反应。
充入某恒容密闭容器中,在催化剂作用下进行反应。①下列有关说法
a.当容器内的压强不再变化时说明主、副反应均达到平衡
b.平衡后,若向容器内再充入少量
 ,主、副反应平衡常数均增大
,主、副反应平衡常数均增大c.平衡后,
 、
、 和
和 三者的物质的量之比保持不变
三者的物质的量之比保持不变d.平衡后,

②在不同温度下,反应相同时间时测得混合气体中N2、
 的体积分数随温度的变化关系如图所示,温度高于205℃时,
的体积分数随温度的变化关系如图所示,温度高于205℃时, 的体积分数随温度的升高而减小的原因可能
的体积分数随温度的升高而减小的原因可能
(3)某温度下,将
 、
、 按物质的量比1:3充入某恒容密闭容器中,若平衡后
按物质的量比1:3充入某恒容密闭容器中,若平衡后 与
与 物质的量之比为3:1,
物质的量之比为3:1, 的转化率为80%,则
的转化率为80%,则 的有效去除率(转化为
的有效去除率(转化为 的
的 的量与起始量的比值)为
的量与起始量的比值)为 的物质的量分数为
的物质的量分数为(4)
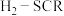 在
在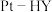 催化剂表面的反应机理如下图:
催化剂表面的反应机理如下图:
研究表明,在
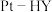 催化剂中,
催化剂中, 表面上形成的
表面上形成的 以
以 的形式被储存。随后在
的形式被储存。随后在 载体上,
载体上, 与
与 和
和 产生
产生 ,该反应的离子方程式为
,该反应的离子方程式为 、
、 物质的量之比为1:1)
物质的量之比为1:1)(5)除了
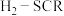 ,还有其他有效的方法消除氮氧化物,例如可用电解法将
,还有其他有效的方法消除氮氧化物,例如可用电解法将 转变为
转变为 ,其工作原理如图。M极为电解池的
,其工作原理如图。M极为电解池的
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】抗原检测盒中T线处是使用的胶体金(Au)标记物,一种从被FeS2包裹的含金矿物中提金的工艺流程如下:
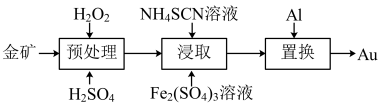
(1)①“预处理”时,FeS2被氧化为Fe2(SO4)3,写出该反应的离子方程式_______ 。
②研究发现H2O2在Fe2+的催化作用下产生具有强氧化能力的中间体·OH,·OH将金表面的FeS2氧化溶出。FeS2溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,FeS2溶出率逐渐提高的主要原因是_______ 。

(2)“置换”时需维持无氧环境,其主要原因是_______ 。
(3)测定样品中Au的含量:准确称取0.1000g试样,加入王水,将Au转化成具有强氧化性的氯金酸(HAuCl4),在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量0.4000mol·L-1 FeSO4溶液30.00mL,将HAuCl4完全还原为Au:滴加二苯胺磺酸钠作指示剂,用0.1000mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液18.00mL。
已知: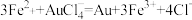

计算样品中金的质量分数(写出计算过程)_______ 。

(1)①“预处理”时,FeS2被氧化为Fe2(SO4)3,写出该反应的离子方程式
②研究发现H2O2在Fe2+的催化作用下产生具有强氧化能力的中间体·OH,·OH将金表面的FeS2氧化溶出。FeS2溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,FeS2溶出率逐渐提高的主要原因是

(2)“置换”时需维持无氧环境,其主要原因是
(3)测定样品中Au的含量:准确称取0.1000g试样,加入王水,将Au转化成具有强氧化性的氯金酸(HAuCl4),在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量0.4000mol·L-1 FeSO4溶液30.00mL,将HAuCl4完全还原为Au:滴加二苯胺磺酸钠作指示剂,用0.1000mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液18.00mL。
已知:
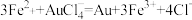

计算样品中金的质量分数(写出计算过程)
您最近一年使用:0次
填空题
|
较难
(0.4)
真题
名校
【推荐2】Ⅰ下列单元操作中采用了热交换设计的有_____
Ⅱ海水晒盐的卤水中还有氯化镁,以卤水为原料生产镁的一种工艺流程如下图所示。
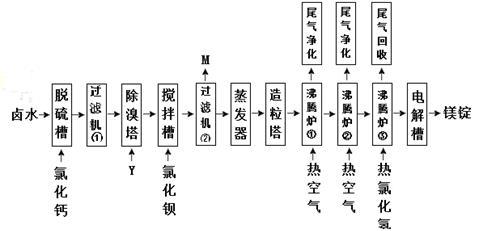
回答下列问题:
(1)脱硫槽、搅拌槽均用于脱除卤水中的___ (填离子符号),M的主要成分是____ (填化学式)。
(2)除溴塔中主要的离子方程式为_____________ 。
(3)沸腾炉①和②的主要作用是_________ 。沸腾炉③通入热氯化氢的主要目的是____ 。
(4)电解槽中阴极的电极反应方程式为_____________ 。
(5)电解槽中阳极产物为____________ ,该产物可直接用于本工艺流程中的________ 。
| A.电解食盐水制烧碱 |
| B.合成氨中的催化合成 |
| C.硫酸生产中的催化氧化 |
| D.氨碱法中的氨盐水碳酸化 |
Ⅱ海水晒盐的卤水中还有氯化镁,以卤水为原料生产镁的一种工艺流程如下图所示。

回答下列问题:
(1)脱硫槽、搅拌槽均用于脱除卤水中的
(2)除溴塔中主要的离子方程式为
(3)沸腾炉①和②的主要作用是
(4)电解槽中阴极的电极反应方程式为
(5)电解槽中阳极产物为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】铁铜单质及其化合物的应用范围很广。现有含氯化亚铁杂质的氯化铜晶体,为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:
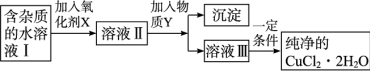
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)化学上通常认为残留在溶液中的离子浓度小于1×10﹣5mol/L时,沉淀就达到完全。已知Fe(OH)2的Ksp约为1.0×10﹣15,则a= 。
(2)加入氧化剂的目的是 ,X应选择 。
A.K2Cr2O7 B.浓HNO3 C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)设计实验从溶液Ⅲ中获得纯净的CuCl2•2H2O。简要描述实验步骤 。

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 完全沉淀的pH | 3.2 | a | 6.7 |
请回答下列问题:
(1)化学上通常认为残留在溶液中的离子浓度小于1×10﹣5mol/L时,沉淀就达到完全。已知Fe(OH)2的Ksp约为1.0×10﹣15,则a= 。
(2)加入氧化剂的目的是 ,X应选择 。
A.K2Cr2O7 B.浓HNO3 C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)设计实验从溶液Ⅲ中获得纯净的CuCl2•2H2O。简要描述实验步骤 。
您最近一年使用:0次



