将CO2还原为HCOOH是实现“碳中和”的有效途径。
(1)利用反应CO2(g)+H2(g)⇌HCOOH(g);ΔH =+14.9 kJ·mol-1不能实现CO2直接加氢合成HCOOH,原因是___________ 。
(2)CO2通过电解法转化为HCOO-的反应机理如图1。Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可让H2O自由通过。
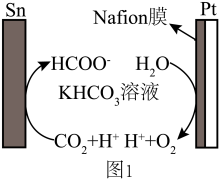
① Sn电极上生成HCOO-的电极反应式为___________ 。
② 电路中通过的电量与HCOO-产率的关系如图2所示。相同条件下,Pt电极有Nafion膜HCOO-产率明显提高,但电量>1000C后又显著下降,可能原因是___________ 。
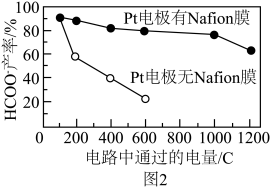
③ 若电解时将Nafion膜置于两个电极中间,保持电流恒定,20 h时向阳极区补充KHCO3,电压与时间关系如图3所示。0~20 h,电压增大的原因是___________ 。

(3)CO2电还原可能的反应机理如下图所示。Sn、In、Bi的活性位点对O的连接能力较强,Au、Cu的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附CO后不易脱离。
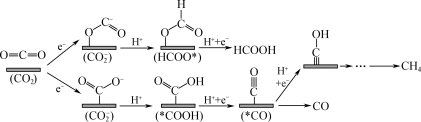
若还原产物主要为CH4时,应选择___________ (填“Sn”“Au”或“Cu”)作催化剂,简述分析过程:___________ 。
(1)利用反应CO2(g)+H2(g)⇌HCOOH(g);ΔH =+14.9 kJ·mol-1不能实现CO2直接加氢合成HCOOH,原因是
(2)CO2通过电解法转化为HCOO-的反应机理如图1。Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可让H2O自由通过。

① Sn电极上生成HCOO-的电极反应式为
② 电路中通过的电量与HCOO-产率的关系如图2所示。相同条件下,Pt电极有Nafion膜HCOO-产率明显提高,但电量>1000C后又显著下降,可能原因是

③ 若电解时将Nafion膜置于两个电极中间,保持电流恒定,20 h时向阳极区补充KHCO3,电压与时间关系如图3所示。0~20 h,电压增大的原因是

(3)CO2电还原可能的反应机理如下图所示。Sn、In、Bi的活性位点对O的连接能力较强,Au、Cu的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附CO后不易脱离。

若还原产物主要为CH4时,应选择
更新时间:2023-05-03 14:24:59
|
相似题推荐
【推荐1】I.一定条件下,在容积为 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
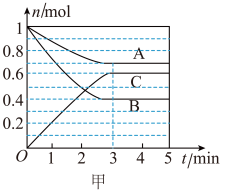
(1)该反应的化学方程式为___________ 。
(2)向一恒温恒容的密闭容器中充入 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
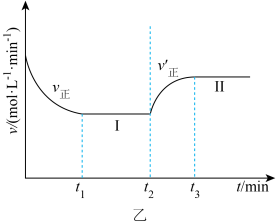
①根据图乙判断,在 时刻改变的外界条件是
时刻改变的外界条件是___________ 。
②平衡时A的体积分数
___________ 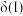 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
Ⅱ.在密闭容器中充入一定量的 ,发生反应:
,发生反应: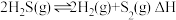 ,如图丙所示为
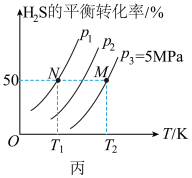
,如图丙所示为 气体分解生成
气体分解生成 和
和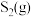 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)
___________ (填“>”“<”或“=”)0。
(4)图丙中压强( 、
、 、
、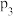 )由大到小的顺序为
)由大到小的顺序为___________ 。
(5)图丙中M点对应的平衡常数
___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
(1)该反应的化学方程式为
(2)向一恒温恒容的密闭容器中充入
 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
①根据图乙判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②平衡时A的体积分数

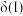 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。Ⅱ.在密闭容器中充入一定量的
 ,发生反应:
,发生反应: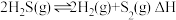 ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和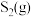 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)

(4)图丙中压强(
 、
、 、
、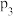 )由大到小的顺序为
)由大到小的顺序为(5)图丙中M点对应的平衡常数

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】综合利用CO2对环境保护及能开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是______ 。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是______ 。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A: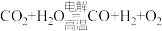
已知:

反应A的热化学方程式是_______ 。
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:
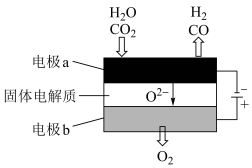
① 电极b发生_______ (填“氧化”或“还原”)反应。
② CO2在电极a放电的反应式是______ 。
(5)CO与H2在高温下合成C5H12(汽油的一种成分)减少碳排放。已知燃烧1 mol C5H12(g)生成H2O(g)放出约3540 kJ的热量。根据化学平衡原理,说明提高合成C5H12的产率可采取的措施是______ 。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
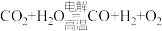
已知:

反应A的热化学方程式是
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生
② CO2在电极a放电的反应式是
(5)CO与H2在高温下合成C5H12(汽油的一种成分)减少碳排放。已知燃烧1 mol C5H12(g)生成H2O(g)放出约3540 kJ的热量。根据化学平衡原理,说明提高合成C5H12的产率可采取的措施是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】乙醇用途广泛且需求量大,寻求制备乙醇的新方法是研究的热点。
(1) 电催化制备乙醇。电解原理示意图如图1所示。
电催化制备乙醇。电解原理示意图如图1所示。
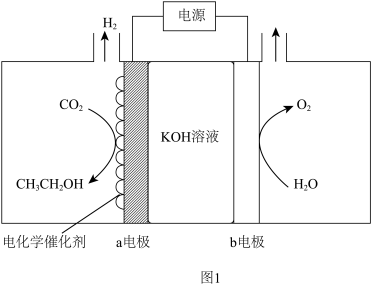
①a电极的电极反应式为_______ 。
②有效抑制a电极发生析氢反应的措施有_______ 。
(2) 催化加氢制备乙醇。
催化加氢制备乙醇。 在催化剂
在催化剂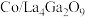 表面加氢制备乙醇的反应为
表面加氢制备乙醇的反应为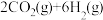

 ,反应机理如图2所示。
,反应机理如图2所示。
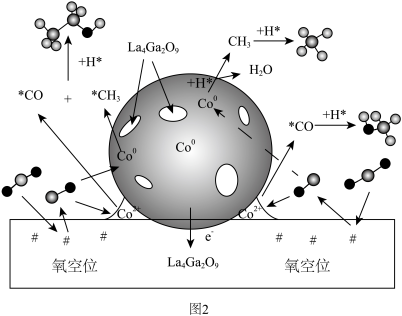
① 在
在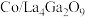 催化剂表面加氢生成
催化剂表面加氢生成 的过程可描述为
的过程可描述为_______ 。
②制取 的过程中可获得的副产物有
的过程中可获得的副产物有_______ 。
③随着反应进行,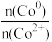 的值
的值_______ (填“增大”、“减小”或“不变”)。
④将 的混合气体置于密闭容器中,在
的混合气体置于密闭容器中,在 和不同温度下反应达到平衡时,
和不同温度下反应达到平衡时, 的转化率和
的转化率和 的选择性[
的选择性[ 的选择性
的选择性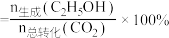 ]如图3所示。温度在时
]如图3所示。温度在时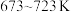 ,CO2的平衡转化率几乎不变,其原因可能为
,CO2的平衡转化率几乎不变,其原因可能为_______ 。
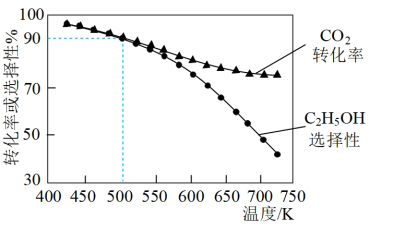
图3
(1)
 电催化制备乙醇。电解原理示意图如图1所示。
电催化制备乙醇。电解原理示意图如图1所示。
①a电极的电极反应式为
②有效抑制a电极发生析氢反应的措施有
(2)
 催化加氢制备乙醇。
催化加氢制备乙醇。 在催化剂
在催化剂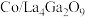 表面加氢制备乙醇的反应为
表面加氢制备乙醇的反应为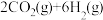

 ,反应机理如图2所示。
,反应机理如图2所示。
①
 在
在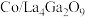 催化剂表面加氢生成
催化剂表面加氢生成 的过程可描述为
的过程可描述为②制取
 的过程中可获得的副产物有
的过程中可获得的副产物有③随着反应进行,
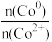 的值
的值④将
 的混合气体置于密闭容器中,在
的混合气体置于密闭容器中,在 和不同温度下反应达到平衡时,
和不同温度下反应达到平衡时, 的转化率和
的转化率和 的选择性[
的选择性[ 的选择性
的选择性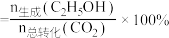 ]如图3所示。温度在时
]如图3所示。温度在时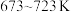 ,CO2的平衡转化率几乎不变,其原因可能为
,CO2的平衡转化率几乎不变,其原因可能为
图3
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)写出下列反应的离子方程式。
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应_____ 。
②硫代硫酸钠与稀硫酸反应_____ 。
③用硫氰化钾溶液检验Fe3+_____ 。
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由_____ 极区向_____ 极区迁移(填阴、阳);阳极电极反应式:____ ;阴极电极反应式:______ 。
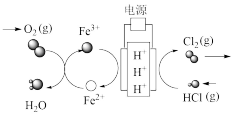
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:______ ;负极:_____ 。
(4)氯碱工业原理的化学方程式:______ 。如图为用阳离子交换膜法进行该工业生产的装置示意图,标出a~f处所对应的原料或产品:_____ 。

生成0.4kg烧碱时,转移电子的物质的量是____ mol。(相对原子质量Na-23、H-1、O-16)
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应
②硫代硫酸钠与稀硫酸反应
③用硫氰化钾溶液检验Fe3+
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由
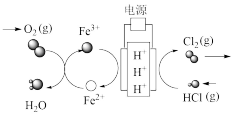
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:
(4)氯碱工业原理的化学方程式:

生成0.4kg烧碱时,转移电子的物质的量是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:

(1)金属M为____ ,操作1为______ 。
(2)加入H2O2的作用是(用离子方程式表示)_________________ ,加入氨水的作用是_______________________ 。
(3)由CoC2O4·2H2O转化为Co2O3的化学方程式是_____________________ 。
(4)知Li2CO3微溶于水,且水溶液呈碱性。其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是_____________ ,在常温条件下,饱和Li2CO3 溶液中离子浓度由大到小的排列顺序为_______________________ 。
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为____________ 。

(1)金属M为
(2)加入H2O2的作用是(用离子方程式表示)
(3)由CoC2O4·2H2O转化为Co2O3的化学方程式是
(4)知Li2CO3微溶于水,且水溶液呈碱性。其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol・L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】软锰矿(主要成分MnO2,含Fe,Al2O3,MgO杂质)的水悬浊液与烟气中的SO2反应可制备MnSO4·H2O,MnO2与SO2反应的化学方程式为MnO2 +SO2=MnSO4。已知下列信息:
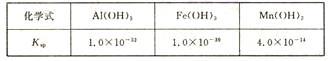
室温下几种氢氧化物的溶度积
回答下列问题:
(1)质量为17.40 g纯净MnO2最多能氧化____ L(标准状况) SO2。
(2)悬浊液吸收烟气后,Fe首先转化为Fe2+进入溶液,然后被_____ 氧化为Fe3+;要证明溶液中存在Fe3+,可选择的试剂是_____ (填标号)。
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室温下,将吸收液过滤,在滤液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是________ 。
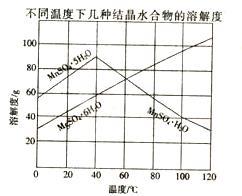
(4)从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为__________ 。

室温下几种氢氧化物的溶度积

回答下列问题:
(1)质量为17.40 g纯净MnO2最多能氧化
(2)悬浊液吸收烟气后,Fe首先转化为Fe2+进入溶液,然后被
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室温下,将吸收液过滤,在滤液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是
(4)从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4·H2O的过程如图所示:
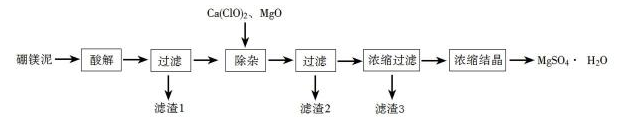
硼镁泥的主要成分如下表:
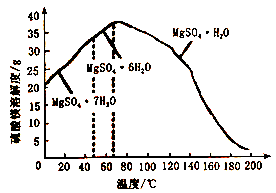
资料:B2O3溶于水形成硼酸,由于硼酸易溶于水,溶解度随温度的升高而升高,而硫酸镁在80℃溶解度最大,所以常规方法很难将二者分离,目前常采用高温结晶法。
回答下列问题:
(1)“滤渣1”中主要含有_________ (写化学式)。
(2)“滤渣2”中主要含有_________ (写化学式),判断”除杂"基本完成的检验方法正确的是
A.取上层清液,滴加苯酚试液不显紫色
B.取上层清液,滴加KSCN,不变红
C.取上层清液,滴加K3[Fe(CN)6]不产生蓝色沉淀
(3)氧化镁的作用是______ 。有同学认为用碳酸镁比用氧化镁要好,原因是________ 。
(4)分离滤渣3应趁热过滤的原因是___________ 。分离滤渣3后的母液中含有的溶质是_____ 和_____ ,可以采用加压、_____ 的方法得到一水合硫酸镁。

硼镁泥的主要成分如下表:
| MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
| 30%〜40% | 20%~25% | 5%〜15% | 2%~3% | 1%〜2% | 1%〜2% |
资料:B2O3溶于水形成硼酸,由于硼酸易溶于水,溶解度随温度的升高而升高,而硫酸镁在80℃溶解度最大,所以常规方法很难将二者分离,目前常采用高温结晶法。

回答下列问题:
(1)“滤渣1”中主要含有
(2)“滤渣2”中主要含有
A.取上层清液,滴加苯酚试液不显紫色
B.取上层清液,滴加KSCN,不变红
C.取上层清液,滴加K3[Fe(CN)6]不产生蓝色沉淀
(3)氧化镁的作用是
(4)分离滤渣3应趁热过滤的原因是
您最近一年使用:0次



