现代生活离不开方便实用的化学电源。各种各样的化学电源都是依据原电池的原理制造的。回答下列问题:
(1)锂离子电池具有质量小、体积小、储存和输出能量大等特点。一种锂离子电池负极材料为嵌锂石墨,正极材料为 (钴酸锂),电解质溶液为
(钴酸锂),电解质溶液为 (六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为
(六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为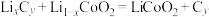 。
。
①放电时,负极反应式为______ 。 由
由______ 极向______ 极迁移(填“正”或“负”)。
②充电时,电池的______ (填“正”或“负”)极应与电源的正极相连,充电时该极的电极反应式为____________ 。
(2)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,DMFC的工作原理如图所示。
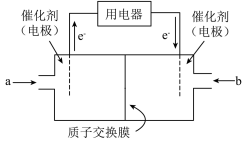
①通入a物质一侧的电极反应式为____________ 。
②通入11.2 L(折算为标准状况下)甲醇蒸气,测得电路中转移1.8 mol电子,则甲醇的利用率为______ 。
(3)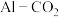 电池工作原理如图所示,利用该电池能有效地将
电池工作原理如图所示,利用该电池能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝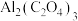 。
。
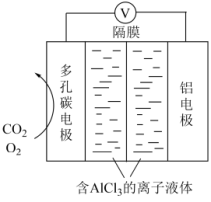
①电池的总反应式为____________ 。
②电池的正极反应式: (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 是催化剂,催化过程可表示为:
是催化剂,催化过程可表示为:
ⅰ.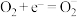 ⅱ.……
ⅱ.……
写出反应ⅱ的离子方程式:____________ 。
(1)锂离子电池具有质量小、体积小、储存和输出能量大等特点。一种锂离子电池负极材料为嵌锂石墨,正极材料为
 (钴酸锂),电解质溶液为
(钴酸锂),电解质溶液为 (六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为
(六氟磷酸锂)的碳酸酯溶液(无水)。该电池放电时的主要反应为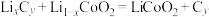 。
。①放电时,负极反应式为
 由
由②充电时,电池的
(2)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,DMFC的工作原理如图所示。

①通入a物质一侧的电极反应式为
②通入11.2 L(折算为标准状况下)甲醇蒸气,测得电路中转移1.8 mol电子,则甲醇的利用率为
(3)
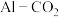 电池工作原理如图所示,利用该电池能有效地将
电池工作原理如图所示,利用该电池能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝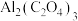 。
。
①电池的总反应式为
②电池的正极反应式:
 (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 是催化剂,催化过程可表示为:
是催化剂,催化过程可表示为:ⅰ.
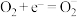 ⅱ.……
ⅱ.……写出反应ⅱ的离子方程式:
更新时间:2024-01-19 21:06:27
|
【知识点】 原电池、电解池综合考查解读
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】图中所示的四个容器中分别盛有不同的溶液,除A、B外,其余电极均为石墨电板。甲为铅蓄电池,其工作原理为:Pb+PbO2+2H2SO4 2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合S,发现H电极附近的溶液先变红,20min后,将S断开,此时C、D两极上产生的气体体积相同;据此回答:
2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合S,发现H电极附近的溶液先变红,20min后,将S断开,此时C、D两极上产生的气体体积相同;据此回答:

(1)B电极的电极材料是___________ (填“PbO2”或“Pb”)。
(2)丙装置中E电极上发生的电极反应式为___________ 。
(3)电解20min时,停止电解,此时要使乙中溶液灰复到原来的状态,只需要加入的一种物质及其物质的量是___________ 。
(4)20min后将乙装置与其他装置断开,然后在C、D两极间连接上灵敏电流计,发现电流计指针偏转,则此时乙装置中发生的总反应化学方程式为___________ 。
 2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合S,发现H电极附近的溶液先变红,20min后,将S断开,此时C、D两极上产生的气体体积相同;据此回答:
2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合S,发现H电极附近的溶液先变红,20min后,将S断开,此时C、D两极上产生的气体体积相同;据此回答:
(1)B电极的电极材料是
(2)丙装置中E电极上发生的电极反应式为
(3)电解20min时,停止电解,此时要使乙中溶液灰复到原来的状态,只需要加入的一种物质及其物质的量是
(4)20min后将乙装置与其他装置断开,然后在C、D两极间连接上灵敏电流计,发现电流计指针偏转,则此时乙装置中发生的总反应化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
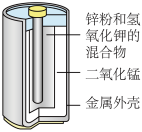
(1)如图是某锌锰干电池的基本构造图。该碱性锌锰干电池的总反应式为2MnO2+Zn+2H2O=2MnO(OH)+Zn(OH)2,该电池工作时正极的电极反应式为_____ 。
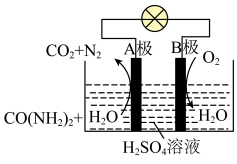
(2)尿素[CO(NH2)2]燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如图所示:负极电极反应为:_____ 。
(3)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。我校高一年级化学课外活动小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:

①该燃料电池A电极名称是_____ ,A电极的电极反应式为_____ 。
②N膜为_____ (填“阳离子交换膜”或“阴离子交换膜”)。
③当电路中有0.2mol电子转移时,正极室质量增加_____ g。
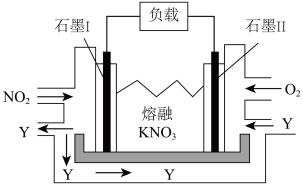
(4)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为_____ 。
(1)如图是某锌锰干电池的基本构造图。该碱性锌锰干电池的总反应式为2MnO2+Zn+2H2O=2MnO(OH)+Zn(OH)2,该电池工作时正极的电极反应式为

(2)尿素[CO(NH2)2]燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如图所示:负极电极反应为:

(3)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。我校高一年级化学课外活动小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:

①该燃料电池A电极名称是
②N膜为
③当电路中有0.2mol电子转移时,正极室质量增加
(4)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】某课外活动小组同学用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应为____________________________________ 。
(2)若开始时开关K与b连接,则B极的电极反应为______ ,总反应的离子方程式为________ 。有关上述实验,下列说法正确的是(填序号)___ 。
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应为______ 。
此时通过阴离子交换膜的离子数______ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_______________ 。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应为_____________________ 。

(1)若开始时开关K与a连接,则B极的电极反应为
(2)若开始时开关K与b连接,则B极的电极反应为
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应为
此时通过阴离子交换膜的离子数
②通电开始后,阴极附近溶液pH会增大,请简述原因
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应为
您最近一年使用:0次



