1 . 恒容密闭容器中充入X,在催化剂作用下发生反应: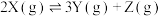 ,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
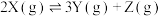 ,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是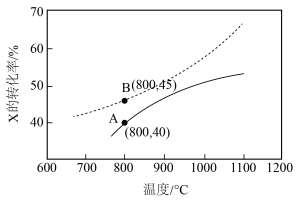
| A.该反应的ΔH<0 |
| B.催化剂可降低该反应的焓变,但不能提高平衡转化率 |
| C.通过延长反应时间,X的转化率能从A点交到B点 |
D.800℃时,A点物质X在0~t s内化学反应速率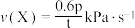 |
您最近一年使用:0次
名校
2 . 高纯MgO具有优良的电绝缘性、高导热性等,常被用作绝缘材料填料、高温耐热材料。由白云石[主要成分为 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下:
(1)请写出基态Ca原子的价电子排布式___________ 。
(2)步骤“煅烧1”中, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成 (
(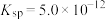 )。若铵浸液中
)。若铵浸液中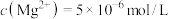 ,则其pH=
,则其pH=___________ ;滤饼“水化反应”后,将体系冷却到与铵浸液相同温度,得到主要含有 的悬浊液,其中
的悬浊液,其中
___________ 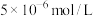 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4)“沉钙”时主要发生反应的离子方程式为___________ 。
(5)“碳化反应”时,镁化合物转化为可溶于水的___________ (填化学式,下同),滤渣的主要成分为___________ 。
(6)“热解”时生成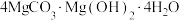 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下: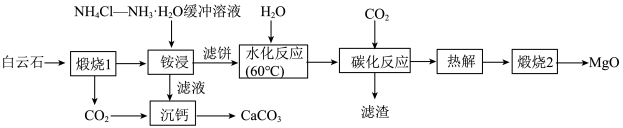
(1)请写出基态Ca原子的价电子排布式
(2)步骤“煅烧1”中,
 发生反应的化学方程式为
发生反应的化学方程式为(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成
 (
(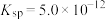 )。若铵浸液中
)。若铵浸液中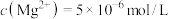 ,则其pH=
,则其pH= 的悬浊液,其中
的悬浊液,其中
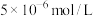 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)“沉钙”时主要发生反应的离子方程式为
(5)“碳化反应”时,镁化合物转化为可溶于水的
(6)“热解”时生成
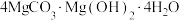 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
您最近一年使用:0次
名校
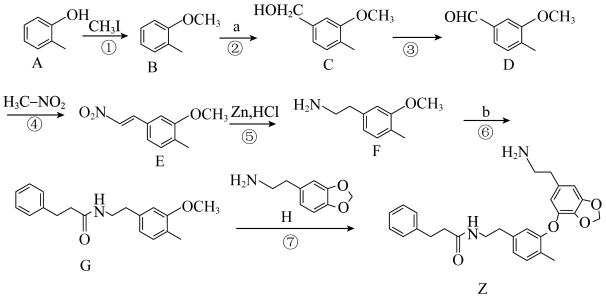
3 . 千金藤素常用于防治肿瘤病患者白细胞减少症、抗疟疾、调节免疫功能等,制备其关键中间体(Ⅰ)的一种合成路线如下:
(1)化合物A的名称为___________ ,碳原子的杂化方式为___________ 。
(2)反应②是原子利用率100%的反应,写出化合物a的一种用途___________ 。
(3)化合物C中含有的官能团名称为___________ ,请写出C转化为D的化学方程式___________ ,反应类型为___________ 。
(4)b能与碳酸氢钠溶液反应生成气体。芳香化合物X为b的同分异构体,能发生水解反应又能发生银镜反应,核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1,X的结构简式为___________ (写出一种)。
(5)参照上述路线,以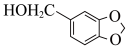 与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图_______ 。
(1)化合物A的名称为
(2)反应②是原子利用率100%的反应,写出化合物a的一种用途
(3)化合物C中含有的官能团名称为
(4)b能与碳酸氢钠溶液反应生成气体。芳香化合物X为b的同分异构体,能发生水解反应又能发生银镜反应,核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1,X的结构简式为
(5)参照上述路线,以
 与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
您最近一年使用:0次
4 . 为研究用 溶液将混合溶液中的
溶液将混合溶液中的 和
和 沉淀分离,绘制了25℃时AgCl和
沉淀分离,绘制了25℃时AgCl和 两种难溶化合物的溶解平衡曲线,如图,其中,
两种难溶化合物的溶解平衡曲线,如图,其中,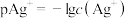 ,其余表达式类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
,其余表达式类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
 溶液将混合溶液中的
溶液将混合溶液中的 和
和 沉淀分离,绘制了25℃时AgCl和
沉淀分离,绘制了25℃时AgCl和 两种难溶化合物的溶解平衡曲线,如图,其中,
两种难溶化合物的溶解平衡曲线,如图,其中,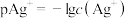 ,其余表达式类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
,其余表达式类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是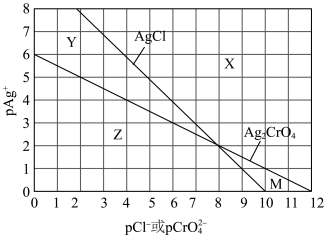
A.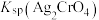 的数量级为 的数量级为 |
B.Y区域内可析出AgCl沉淀,而不析 出沉淀 出沉淀 |
C.向浓度均为0.1mol/L的 、 、 混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀 混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀 |
D.25℃时,向 、AgCl混合固体和水的溶解平衡体系中加少量水, 、AgCl混合固体和水的溶解平衡体系中加少量水,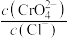 增大 增大 |
您最近一年使用:0次
名校
5 . 乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体。实验室中采用苯胺(在空气中易被氧化)和冰醋酸等原料制备乙酰苯胺,反应为: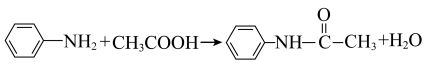 ;
;
| 摩尔质量(g/mol) | 熔点/℃ | 沸点/℃ | 密度/(g/cm³) | 溶解度/g | |||
| 水 | 乙醇 | 乙醚 | |||||
| 苯胺 | 93 | -6.2 | 184 | 1.022 | 3.6 | 混溶 | 混溶 |
| 冰醋酸 | 60 | 16.7 | 118 | 1.049 | 混溶 | 混溶 | 混溶 |
| 乙酰苯胺 | 135 | 115 | 305 | 1.212 | 溶于热水 | 溶 | 溶 |
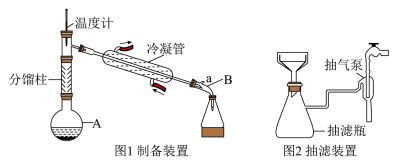
(1)加料:图1为制备装置(夹持、加热装置略),在仪器A中加入5.0mL苯胺、7.4mL冰醋酸和0.1g锌粉。仪器A的名称是
(2)加热制备粗产品;仪器A中加料后,加热至105℃。适宜使用
(3)过滤:反应结束后,将A中的反应混合物先趁热倒入适量冷水中,不断搅拌,使之充分冷却,再用图2所示的抽滤装置过滤。与普通过滤相比,抽滤的优点是
A.冷水 B.热水 C.乙醇 D.乙醚
(4)重结晶:①将粗乙酰苯胺放入适量水中,若观察到水中有油珠存在,可补加适量水,使油珠消失。根据下表乙酰苯胺的溶解度,上述水的温度选择
| 温度/℃ | 20 | 25 | 50 | 80 | 100 |
| 溶解度/g | 0.46 | 0.56 | 0.84 | 3.50 | 5.50 |
(5)产率计算:经过重结晶、干燥,得到乙酰苯胺产品5.0g,实验的产率是
您最近一年使用:0次
名校
6 . 根据下列实验操作及现象,所得结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 石蜡油催化分解,将产生的气体通入酸性高锰酸钾溶液,溶液紫色褪去 | 产生的气体有乙烯 |
| B | 向溶有 的 的 溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 |  具有强氧化性 具有强氧化性 |
| C | 25℃,用pH计测得某一元酸(HR)溶液的pH=2.8 | HR为弱电解质 |
| D | 向 溶液中加入95%乙醇,析出蓝色晶体 溶液中加入95%乙醇,析出蓝色晶体 |  在水-乙醇混合溶剂中溶解度较小 在水-乙醇混合溶剂中溶解度较小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 氮化铬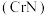 是一种良好的耐磨材料,难溶于水。实验小组用无水氯化铬
是一种良好的耐磨材料,难溶于水。实验小组用无水氯化铬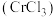 与氨气在高温下反应制备
与氨气在高温下反应制备 。
。
已知:① 的沸点是
的沸点是 ;②光气
;②光气 有毒,遇水生成
有毒,遇水生成 和
和
Ⅰ.制备无水氯化铬
反应原理为: 。相关实验装置如图(夹持装置略):
。相关实验装置如图(夹持装置略):
 .水浴加热并维持A的温度在
.水浴加热并维持A的温度在
 .打开
.打开 ,通入
,通入 并保证锥形瓶中每分钟有250个左右的气泡逸出
并保证锥形瓶中每分钟有250个左右的气泡逸出
 .点燃B处酒精喷灯,使瓷舟温度升至
.点燃B处酒精喷灯,使瓷舟温度升至 左右,反应一定时间
左右,反应一定时间
 .先后停止加热
.先后停止加热 ,冷却,并继续通入一段时间的
,冷却,并继续通入一段时间的
(1)C装置的名称是________________ 。
(2)A使用水浴加热的优点是_______________ 。
(3)D中反应的化学方程式为______________ 。
Ⅱ.制备氮化铬
某校化学兴趣小组设计如图装置在实验室制备氮化铬(加热及夹持装置略),其反应原理为:
已知: 易溶于水形成紫色的
易溶于水形成紫色的 离子,且易与水反应。
离子,且易与水反应。 装置是简易的氨气制备装置,导管
装置是简易的氨气制备装置,导管 的作用是
的作用是______________ 。
(5) 中盛放的试剂是
中盛放的试剂是__________ 。
(6)实验过程中需间歇性微热 处导管的目的是
处导管的目的是___________ 。
(7)请设计实验验证制得的 中是否含有
中是否含有
________________ 。
Ⅲ.测产品氮化铬的纯度
(8)向 所得产品中加入足量氢氧化钠溶液(杂质与氢氧化钠溶液不反应),然后将氨气全部蒸出,将氨气用
所得产品中加入足量氢氧化钠溶液(杂质与氢氧化钠溶液不反应),然后将氨气全部蒸出,将氨气用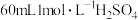 溶液完全吸收,剩余的硫酸用
溶液完全吸收,剩余的硫酸用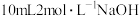 溶液恰好中和,则所得产品中氮化铬的纯度为
溶液恰好中和,则所得产品中氮化铬的纯度为_______________ 。
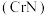 是一种良好的耐磨材料,难溶于水。实验小组用无水氯化铬
是一种良好的耐磨材料,难溶于水。实验小组用无水氯化铬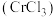 与氨气在高温下反应制备
与氨气在高温下反应制备 。
。已知:①
 的沸点是
的沸点是 ;②光气
;②光气 有毒,遇水生成
有毒,遇水生成 和
和
Ⅰ.制备无水氯化铬
反应原理为:
 。相关实验装置如图(夹持装置略):
。相关实验装置如图(夹持装置略):
 .水浴加热并维持A的温度在
.水浴加热并维持A的温度在
 .打开
.打开 ,通入
,通入 并保证锥形瓶中每分钟有250个左右的气泡逸出
并保证锥形瓶中每分钟有250个左右的气泡逸出 .点燃B处酒精喷灯,使瓷舟温度升至
.点燃B处酒精喷灯,使瓷舟温度升至 左右,反应一定时间
左右,反应一定时间 .先后停止加热
.先后停止加热 ,冷却,并继续通入一段时间的
,冷却,并继续通入一段时间的
(1)C装置的名称是
(2)A使用水浴加热的优点是
(3)D中反应的化学方程式为
Ⅱ.制备氮化铬
某校化学兴趣小组设计如图装置在实验室制备氮化铬(加热及夹持装置略),其反应原理为:

已知:
 易溶于水形成紫色的
易溶于水形成紫色的 离子,且易与水反应。
离子,且易与水反应。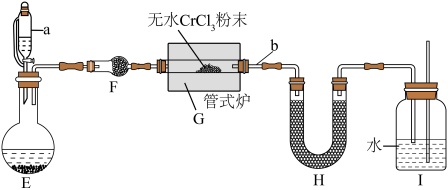
 装置是简易的氨气制备装置,导管
装置是简易的氨气制备装置,导管 的作用是
的作用是(5)
 中盛放的试剂是
中盛放的试剂是(6)实验过程中需间歇性微热
 处导管的目的是
处导管的目的是(7)请设计实验验证制得的
 中是否含有
中是否含有
Ⅲ.测产品氮化铬的纯度
(8)向
 所得产品中加入足量氢氧化钠溶液(杂质与氢氧化钠溶液不反应),然后将氨气全部蒸出,将氨气用
所得产品中加入足量氢氧化钠溶液(杂质与氢氧化钠溶液不反应),然后将氨气全部蒸出,将氨气用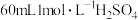 溶液完全吸收,剩余的硫酸用
溶液完全吸收,剩余的硫酸用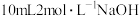 溶液恰好中和,则所得产品中氮化铬的纯度为
溶液恰好中和,则所得产品中氮化铬的纯度为
您最近一年使用:0次
8 .  是一种压电材料。一种以富钛渣(主要成分为
是一种压电材料。一种以富钛渣(主要成分为 ,含少量
,含少量 和
和 的氧化物杂质)和重晶石(主要成分是
的氧化物杂质)和重晶石(主要成分是 )为原料,制备钛酸钡的工艺流程如图所示。
)为原料,制备钛酸钡的工艺流程如图所示。 元素在不同
元素在不同 条件下的存在形式:
条件下的存在形式:
② ,
, ,
,
③ 易溶于水,
易溶于水, 微溶于水
微溶于水
回答下列问题:
(1)为提高沸腾氯化的速率,可采取的措施是_______________ (答出一点即可)。
(2)“焙烧”后固体产物是 ,则“焙烧”过程的化学方程式为
,则“焙烧”过程的化学方程式为_____________ 。“焙烧”过程中应避免氧气进入,主要原因是会产生污染性气体__________ (写化学式)。“沉淀1”中所得滤渣的主要成分是____________ (写化学式)。
(3)“沉淀2”中生成 的化学方程式为
的化学方程式为___________ (已知该反应还生成了 和
和 )。
)。
(4) 溶液显
溶液显_______ 性(填“酸”、“碱”或“中”),“沉淀2”中不可用 溶液代替的原因是
溶液代替的原因是_____________ 。
(5)立方钛酸钡晶体的结构如图所示。 周围与它最近且距离相等的
周围与它最近且距离相等的 有
有________ 个。
②该晶体晶胞的边长为 ,晶体密度为
,晶体密度为________  。(列出计算式,已知阿伏加德罗常数为
。(列出计算式,已知阿伏加德罗常数为 ,
, )
)
 是一种压电材料。一种以富钛渣(主要成分为
是一种压电材料。一种以富钛渣(主要成分为 ,含少量
,含少量 和
和 的氧化物杂质)和重晶石(主要成分是
的氧化物杂质)和重晶石(主要成分是 )为原料,制备钛酸钡的工艺流程如图所示。
)为原料,制备钛酸钡的工艺流程如图所示。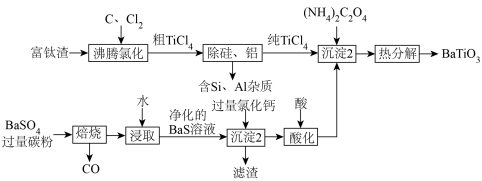
 元素在不同
元素在不同 条件下的存在形式:
条件下的存在形式: |  | 4~7 |  |
| 存在形式 |  |  |  |
 ,
, ,
,
③
 易溶于水,
易溶于水, 微溶于水
微溶于水回答下列问题:
(1)为提高沸腾氯化的速率,可采取的措施是
(2)“焙烧”后固体产物是
 ,则“焙烧”过程的化学方程式为
,则“焙烧”过程的化学方程式为(3)“沉淀2”中生成
 的化学方程式为
的化学方程式为 和
和 )。
)。(4)
 溶液显
溶液显 溶液代替的原因是
溶液代替的原因是(5)立方钛酸钡晶体的结构如图所示。
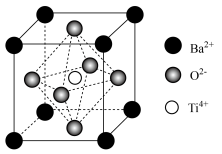
 周围与它最近且距离相等的
周围与它最近且距离相等的 有
有②该晶体晶胞的边长为
 ,晶体密度为
,晶体密度为 。(列出计算式,已知阿伏加德罗常数为
。(列出计算式,已知阿伏加德罗常数为 ,
, )
)
您最近一年使用:0次
9 . 常温下,在 (弱酸)溶液中滴加
(弱酸)溶液中滴加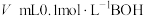 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
 (弱酸)溶液中滴加
(弱酸)溶液中滴加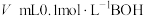 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是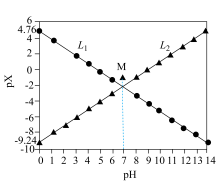
A. 代表 代表 与 与 的关系 的关系 |
B. 时达到 时达到 点, 点, 不水解 不水解 |
C.常温下, |
D.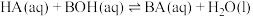 的平衡常数 的平衡常数 小于10000 小于10000 |
您最近一年使用:0次
名校
10 . 前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子的核外电子占据3个能级且每个能级上电子数相等,基态C原子价层电子排布式为 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
(1)基态E原子有___________ 种运动状态不同的电子,D位于元素周期表___________ 区。
(2)在A、B、C、D的简单氢化物中,沸点最高的是___________ (填化学式,下同);键角最大的是___________ 。
(3) 分子中D的杂化类型是
分子中D的杂化类型是___________ ;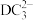 的空间结构为
的空间结构为___________ 。
(4)元素的基态气态原子得到一个电子形成 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:___________ 。
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为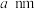 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为___________ ,该晶体密度为___________  。
。
 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:(1)基态E原子有
(2)在A、B、C、D的简单氢化物中,沸点最高的是
(3)
 分子中D的杂化类型是
分子中D的杂化类型是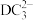 的空间结构为
的空间结构为(4)元素的基态气态原子得到一个电子形成
 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为
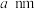 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为 。
。
您最近一年使用:0次



