名校
解题方法
1 . A、B、C、D、E为原子序数依次增大的前四周期元素。A是半径最小的元素,B的价电子层中有3个未成对电子;C与D同主族;E的最外层只有1个电子,但次外层有18个电子。五种元素形成的离子化合物可表示为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是A. 中含有 中含有 键数目为26 键数目为26 |
B.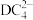 呈正四面体形 呈正四面体形 |
C.该化合物受热分解时首先失去的是 |
| D.A与B、C均可形成含有非极性共价键的化合物 |
您最近一年使用:0次
名校
解题方法
2 . 物质的结构决定其性质。下列实例与解释正确且相符的是
A.摩尔质量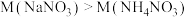 ,因此 ,因此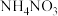 的熔点低于 的熔点低于 |
B.根据基团种类不同,推断酸性: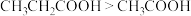 |
C. 分子间氢键数目多于HF,因此水的沸点高于氟化氢 分子间氢键数目多于HF,因此水的沸点高于氟化氢 |
| D.碘的非金属性较弱,因此碘的熔沸点较低 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法中正确的是
| A.碳化硅的熔点低于金刚石 | B. 是非极性分子 是非极性分子 |
C. 的空间构型为平面三角形 的空间构型为平面三角形 | D.ⅥA族元素氢化物的沸点从上到下依次升高 |
您最近一年使用:0次
4 . 4月29日发射入轨的天和核心舱,将开启我国空间站建设。聚碳酸酯无色透明,具有优异的抗冲击性,能用于制造宇航员的面罩、智能手机机身外壳等。双酚化合物是合成聚碳酸酯的单体之一,某种双酚化合物 的合成路线如下:
的合成路线如下: 中所含的官能团除苯环外,还有
中所含的官能团除苯环外,还有___________ 。
(2)写出反应类型。反应①___________ ;反应③___________ 。
(3)写出结构简式。
___________ ;
___________ 。
(4)写出反应④的化学方程式___________ 。
(5) 有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式
有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式___________ 。
(I)属于 -氨基酸,且苯环上有三个互为间位的取代基;
-氨基酸,且苯环上有三个互为间位的取代基;
(II)与 溶液作用无显色现象;
溶液作用无显色现象;
(III)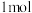 该同分异构体与足量
该同分异构体与足量 溶液反应时,最多能消耗
溶液反应时,最多能消耗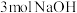 。
。
(6)最常见的聚碳酸酯是用双酚 (
(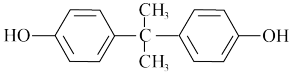 )与光气(
)与光气(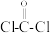 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式___________ 。
 的合成路线如下:
的合成路线如下: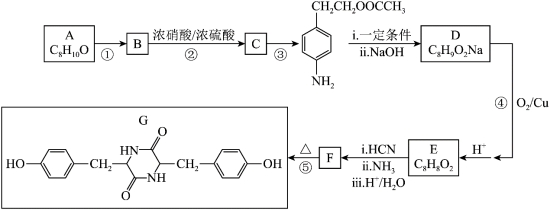
已知: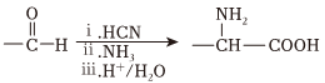
 中所含的官能团除苯环外,还有
中所含的官能团除苯环外,还有(2)写出反应类型。反应①
(3)写出结构简式。


(4)写出反应④的化学方程式
(5)
 有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式
有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式(I)属于
 -氨基酸,且苯环上有三个互为间位的取代基;
-氨基酸,且苯环上有三个互为间位的取代基;(II)与
 溶液作用无显色现象;
溶液作用无显色现象;(III)
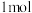 该同分异构体与足量
该同分异构体与足量 溶液反应时,最多能消耗
溶液反应时,最多能消耗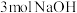 。
。(6)最常见的聚碳酸酯是用双酚
 (
( )与光气(
)与光气(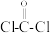 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列问题:
(1)金属氢化物是一类常用的储氢剂。氢化钠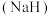 的晶体类型为
的晶体类型为___________ , 与
与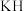 相比,熔点更高的是
相比,熔点更高的是___________ 。
(2)钛系贮氢合金中的钛锰合金,吸氢量更大,室温下易活化,基态锰原子的价层电子排布式为___________ 。与锰同周期且价层电子数相同的元素基态原子的价电子排布图为___________ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度
(氨硼烷)具有很高的储氢容量及相对低的放氢温度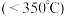 而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
①与 同周期元素中,第一电离能大于
同周期元素中,第一电离能大于 的元素有
的元素有___________ 种(填数字)。
②氨硼烷中的共价键可以分为两种,这两种共价键的数量比为___________ 。
③氨硼烷中的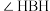
___________ (填“ ”、“
”、“ ”或“
”或“ ”)
”) 中的
中的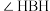 ,理由是
,理由是___________ 。
(4)咔唑(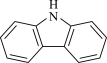 )是一种新型有机液体储氢材料,
)是一种新型有机液体储氢材料, 咔唑中含有的
咔唑中含有的 键的数目为
键的数目为___________ (设阿伏加德罗常数的值为 )。已知咔唑分子中
)。已知咔唑分子中 原子连接的
原子连接的 与两个苯环共平面,则分子中
与两个苯环共平面,则分子中 原子的杂化类型是
原子的杂化类型是___________ 。
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示,该晶体储氢时, 分子在晶胞的体心和棱心位置。
分子在晶胞的体心和棱心位置。 原子最近的
原子最近的 分子个数是
分子个数是___________ 。
②该晶体未储氢时的密度为 ,则铁原子的半径为
,则铁原子的半径为___________  。
。
(用含 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 ,假设晶胞中邻近的铁原子相切)
,假设晶胞中邻近的铁原子相切)
(1)金属氢化物是一类常用的储氢剂。氢化钠
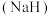 的晶体类型为
的晶体类型为 与
与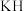 相比,熔点更高的是
相比,熔点更高的是(2)钛系贮氢合金中的钛锰合金,吸氢量更大,室温下易活化,基态锰原子的价层电子排布式为
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度
(氨硼烷)具有很高的储氢容量及相对低的放氢温度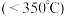 而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①与
 同周期元素中,第一电离能大于
同周期元素中,第一电离能大于 的元素有
的元素有②氨硼烷中的共价键可以分为两种,这两种共价键的数量比为
③氨硼烷中的
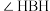
 ”、“
”、“ ”或“
”或“ ”)
”) 中的
中的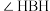 ,理由是
,理由是(4)咔唑(
 )是一种新型有机液体储氢材料,
)是一种新型有机液体储氢材料, 咔唑中含有的
咔唑中含有的 键的数目为
键的数目为 )。已知咔唑分子中
)。已知咔唑分子中 原子连接的
原子连接的 与两个苯环共平面,则分子中
与两个苯环共平面,则分子中 原子的杂化类型是
原子的杂化类型是(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示,该晶体储氢时,
 分子在晶胞的体心和棱心位置。
分子在晶胞的体心和棱心位置。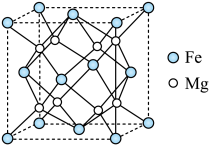
 原子最近的
原子最近的 分子个数是
分子个数是②该晶体未储氢时的密度为
 ,则铁原子的半径为
,则铁原子的半径为 。
。(用含
 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 ,假设晶胞中邻近的铁原子相切)
,假设晶胞中邻近的铁原子相切)
您最近一年使用:0次
6 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为___ 。
(2)有下列实验:___ 。深蓝色晶体的化学式为___ 。
②写出蓝色沉淀溶解成深蓝色溶液的离子方程式___ 。
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角___ (填“大”或“小”)。[Cu(NH3)4]SO4中存在的化学键类型有___ (填标号)。
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___ (填标号)。
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:___ (用“→”或“—”将配位键表示出来)。
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为
(2)有下列实验:

②写出蓝色沉淀溶解成深蓝色溶液的离子方程式
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:
您最近一年使用:0次
名校
解题方法
7 . 已知P4单质的结构如下,P4在KOH溶液中的变化是:P4+3KOH+3H2O=3KH2PO2+PH3下列说法正确的是
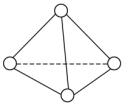
| A.31gP4含有1.5NA个P−P键 | B.产物PH3分子中所有的原子可能共平面 |
| C.P4中P原子为sp2杂化 | D.相关元素的电负性大小顺序:P>O>H>K |
您最近一年使用:0次
8 . 某实验小组采用如下实验探究该依地酸铁钠(强化补铁剂)中铁元素的化合价。(已知:依地酸根是常见的配体,邻二氮菲可与 形成橙红色配合物)下列说法正确的是
形成橙红色配合物)下列说法正确的是
 形成橙红色配合物)下列说法正确的是
形成橙红色配合物)下列说法正确的是
| A.从现象②和③推测,依地酸铁钠中不含Fe(Ⅲ) |
| B.从现象②和⑤推测,依地酸铁钠中含Fe(Ⅱ) |
C.从现象①、②和③推测, 与 与 形成配合物的稳定性强于依地酸铁钠 形成配合物的稳定性强于依地酸铁钠 |
D.从现象①、④和⑤推测, 与邻二氮菲形成配合物的稳定性强于依地酸根 与邻二氮菲形成配合物的稳定性强于依地酸根 |
您最近一年使用:0次
2024-03-27更新
|
247次组卷
|
2卷引用:天津市第一中学2023-2024学年高二下学期期中考试化学试卷
名校
9 . 下列实验操作能达到其对应目的的是
| 实验目的 | 操作 | |
| A | 欲证明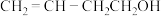 中含有碳碳双键 中含有碳碳双键 | 取该物质适量于试管,滴入酸性 溶液 溶液 |
| B | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,生成三溴苯酚白色沉淀,过滤 |
| C | 欲检验乙醇的消去反应产物 | 将乙醇与浓硫酸混合,迅速加热到170℃(务必迅速加热到170℃,140℃会有乙醚生成),将气体产物通过导气管直接通入酸性高锰酸钾 |
| D | 欲证明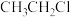 中含有氯原子 中含有氯原子 | 取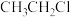 在碱性条件下的水解液适量于试管,加足量硝酸酸化,再加入 在碱性条件下的水解液适量于试管,加足量硝酸酸化,再加入 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-08更新
|
733次组卷
|
3卷引用:天津市双菱中学2023-2024学年高二下学期期中质量检测化学试卷
名校
解题方法
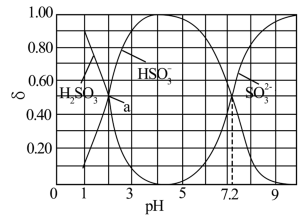
10 . 边搅拌边向 溶液中通入
溶液中通入 制备
制备 溶液,水溶液中
溶液,水溶液中 、
、 、
、 的分布系数δ随pH的变化关系如图所示。[比如
的分布系数δ随pH的变化关系如图所示。[比如 的分布系数:
的分布系数: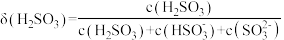 ]下列有关叙述错误的是
]下列有关叙述错误的是
 溶液中通入
溶液中通入 制备
制备 溶液,水溶液中
溶液,水溶液中 、
、 、
、 的分布系数δ随pH的变化关系如图所示。[比如
的分布系数δ随pH的变化关系如图所示。[比如 的分布系数:
的分布系数: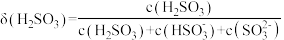 ]下列有关叙述错误的是
]下列有关叙述错误的是
| A.当溶液pH范围为4~5时,停止通入SO2 |
B.根据曲线数据计算可知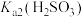 的数量级为 的数量级为 |
C.a点的溶液中 |
D. 的溶液中, 的溶液中,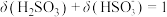 |
您最近一年使用:0次



