解题方法
1 . 亚硝酰氯的化学式为NOCl,主要用于合成洗涤剂、触媒,也可用作有机合成中间体。其熔点-64.5℃,沸点-5.5℃,易水解。某实验小组用以下实验来探究亚硝酰氯的制备。回答下列问题:
(1)文献中记载可利用浓盐酸和 浓溶液反应制取少量的NOCl,装置如下图所示,
浓溶液反应制取少量的NOCl,装置如下图所示,________ 。
②用仪器X代替分液漏斗的优点是________ 。
③装置B中盛放无水 的仪器名称为
的仪器名称为________ ,装置C的作用是________ 。
(2)亚硝酰氯也可以用NO与 混合制取。
混合制取。
①实验室用铜和稀硝酸反应来制备NO,标准状况下1.92gCu完全反应理论上可产生________ LNO。
②选用如下图所示的部分装置,用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为________ →d→c→g(气流方向从左至右,每组仪器最多使用一次)。实验室用二氧化锰制备氯气的离子方程式为________ 。 制取实验过程中“先通入
制取实验过程中“先通入 ,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是________ 。
(1)文献中记载可利用浓盐酸和
 浓溶液反应制取少量的NOCl,装置如下图所示,
浓溶液反应制取少量的NOCl,装置如下图所示,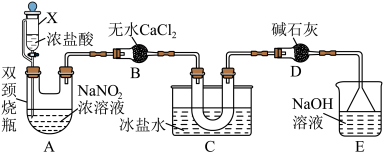
②用仪器X代替分液漏斗的优点是
③装置B中盛放无水
 的仪器名称为
的仪器名称为(2)亚硝酰氯也可以用NO与
 混合制取。
混合制取。①实验室用铜和稀硝酸反应来制备NO,标准状况下1.92gCu完全反应理论上可产生
②选用如下图所示的部分装置,用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为
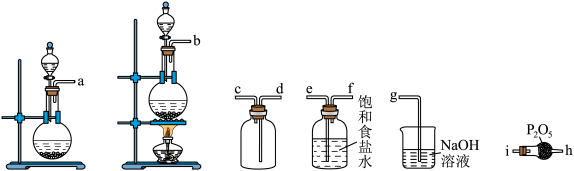
 制取实验过程中“先通入
制取实验过程中“先通入 ,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
您最近一年使用:0次
名校
2 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
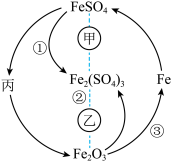
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近一年使用:0次
2024-04-21更新
|
168次组卷
|
2卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
名校
3 . 加兰他敏是一种天然生物碱,其中间体的合成路线如下。
(1)A中与卤代烃成醚活性高的羟基位于酯基的___________ 位(填“间”或“对”),A中碳原子的杂化方式为___________ 。
(2)C发生酸性水解,新产生的官能团为羟基和___________ (填名称)。
(3)用 代替PCC完成
代替PCC完成 的转化,化学方程式为
的转化,化学方程式为___________ 。
(4) 的同分异构体中,红外光谱显示有酚羟基、无
的同分异构体中,红外光谱显示有酚羟基、无 键的共有
键的共有___________ 种。
(5) 的反应类型为
的反应类型为___________ 。
(6)某药物中间体的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为___________ 和___________ 。
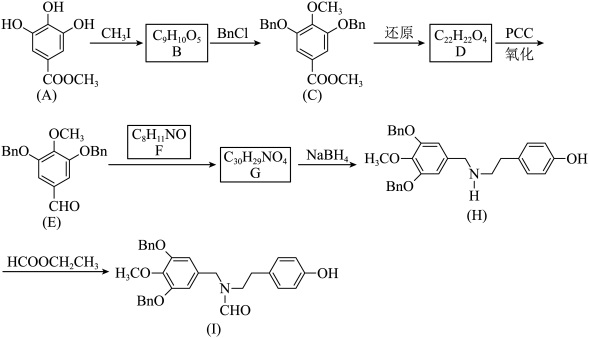
①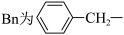
②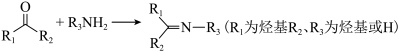
(1)A中与卤代烃成醚活性高的羟基位于酯基的
(2)C发生酸性水解,新产生的官能团为羟基和
(3)用
 代替PCC完成
代替PCC完成 的转化,化学方程式为
的转化,化学方程式为(4)
 的同分异构体中,红外光谱显示有酚羟基、无
的同分异构体中,红外光谱显示有酚羟基、无 键的共有
键的共有(5)
 的反应类型为
的反应类型为(6)某药物中间体的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为

您最近一年使用:0次
名校
解题方法
4 . 三氯化铬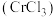 是常用的催化剂,易潮解,易升华,高温下易被氧化。某化学小组采用如下流程制备无水三氯化铬并探究三氯化铬六水合物的结构。
是常用的催化剂,易潮解,易升华,高温下易被氧化。某化学小组采用如下流程制备无水三氯化铬并探究三氯化铬六水合物的结构。 沸点为
沸点为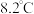 ,有毒,易水解。
,有毒,易水解。
(1)“热分解”发生反应的化学方程式为___________ 。
(2)“热反应”制无水 的实验装置如图所示(
的实验装置如图所示( 中加热装置略)。
中加热装置略)。 的目的是
的目的是___________ 。
②A中仪器X的名称是___________ ,其作用是___________ 。
③E中收集的物质含有___________ (写化学式)。
④尾气经___________ 处理后可循环使用。
(3)已知 配合物
配合物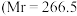 ,配位数为6)有多种异构体,不同条件下析出不同颜色的晶体,如
,配位数为6)有多种异构体,不同条件下析出不同颜色的晶体,如 晶体为淡绿色。将
晶体为淡绿色。将 溶于水,一定条件下结晶析出暗绿色晶体。称取
溶于水,一定条件下结晶析出暗绿色晶体。称取 该暗绿色晶体溶于水配成暗绿色溶液,加入足量的
该暗绿色晶体溶于水配成暗绿色溶液,加入足量的 溶液,得到2.
溶液,得到2. 白色沉淀。
白色沉淀。
① 中存在的化学键有
中存在的化学键有___________ (填序号)。
a.配位键 b.氢键 c.离子键 d.金属键
②该暗绿色晶体的化学式为___________ 。
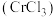 是常用的催化剂,易潮解,易升华,高温下易被氧化。某化学小组采用如下流程制备无水三氯化铬并探究三氯化铬六水合物的结构。
是常用的催化剂,易潮解,易升华,高温下易被氧化。某化学小组采用如下流程制备无水三氯化铬并探究三氯化铬六水合物的结构。
 沸点为
沸点为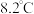 ,有毒,易水解。
,有毒,易水解。(1)“热分解”发生反应的化学方程式为
(2)“热反应”制无水
 的实验装置如图所示(
的实验装置如图所示( 中加热装置略)。
中加热装置略)。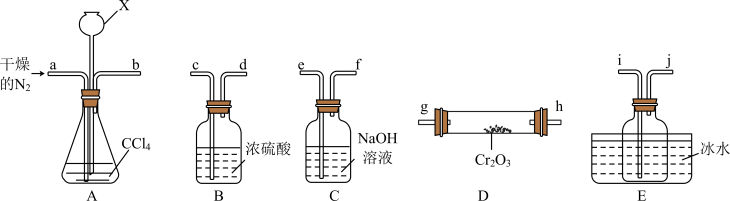
 的目的是
的目的是②A中仪器X的名称是
③E中收集的物质含有
④尾气经
(3)已知
 配合物
配合物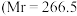 ,配位数为6)有多种异构体,不同条件下析出不同颜色的晶体,如
,配位数为6)有多种异构体,不同条件下析出不同颜色的晶体,如 晶体为淡绿色。将
晶体为淡绿色。将 溶于水,一定条件下结晶析出暗绿色晶体。称取
溶于水,一定条件下结晶析出暗绿色晶体。称取 该暗绿色晶体溶于水配成暗绿色溶液,加入足量的
该暗绿色晶体溶于水配成暗绿色溶液,加入足量的 溶液,得到2.
溶液,得到2. 白色沉淀。
白色沉淀。①
 中存在的化学键有
中存在的化学键有a.配位键 b.氢键 c.离子键 d.金属键
②该暗绿色晶体的化学式为
您最近一年使用:0次
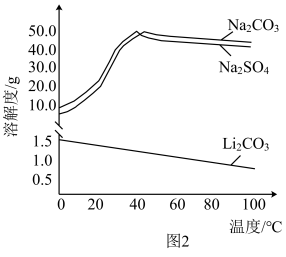
5 . 某温度下,两种难溶盐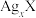 、
、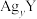 的饱和溶液中
的饱和溶液中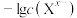 或
或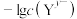 与
与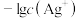 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
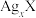 、
、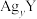 的饱和溶液中
的饱和溶液中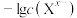 或
或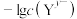 与
与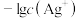 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.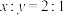 |
B.a点时, , ,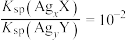 |
C. 平衡常数 平衡常数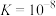 |
| D.向浓度均为0.1mol/L的NaxX、NayY混合溶液中滴加AgNO3溶液,先产生AgyY沉淀 |
您最近一年使用:0次
2024-04-17更新
|
426次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
6 . 将 催化转化成CO是实现
催化转化成CO是实现 资源化利用的关键步骤,发生的反应有
资源化利用的关键步骤,发生的反应有
反应Ⅰ:

反应Ⅱ: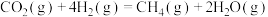

反应Ⅲ: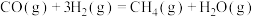
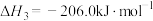 ,0.1MPa,在密闭容器中按
,0.1MPa,在密闭容器中按 投料,平衡时各组分的摩尔分数[物质i的摩尔分数:
投料,平衡时各组分的摩尔分数[物质i的摩尔分数: ,
, 未计入]随温度的变化如图。下列说法
未计入]随温度的变化如图。下列说法不正确 的是
 催化转化成CO是实现
催化转化成CO是实现 资源化利用的关键步骤,发生的反应有
资源化利用的关键步骤,发生的反应有反应Ⅰ:


反应Ⅱ:
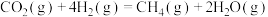

反应Ⅲ:
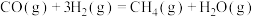
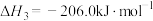 ,0.1MPa,在密闭容器中按
,0.1MPa,在密闭容器中按 投料,平衡时各组分的摩尔分数[物质i的摩尔分数:
投料,平衡时各组分的摩尔分数[物质i的摩尔分数: ,
, 未计入]随温度的变化如图。下列说法
未计入]随温度的变化如图。下列说法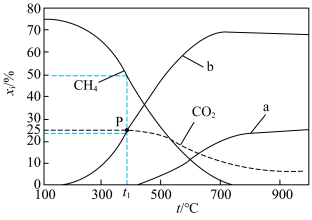
| A.低温下有利于反应Ⅱ正向进行 | B.曲线b为 |
C.P点时反应Ⅰ的 约为 约为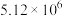 | D.900℃时,适当增大体系压强,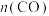 保持不变 保持不变 |
您最近一年使用:0次
2024-04-16更新
|
178次组卷
|
2卷引用:广西南宁市第二中学2024届高三下学期5月月考化学试题
名校
7 . 丙烯是三大合成材料的基本原料之一,可用于生产多种重要有机化工原料。由丙烷制丙烯的两种方法如下:
Ⅰ.丙烷无氧脱氢法:
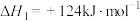
Ⅱ.丙烷氧化脱氢法: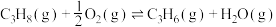

请回答下列问题:
(1)已知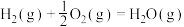
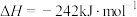 ,由此计算
,由此计算 =
=______  。
。
(2)某温度下,在恒容密闭容器中充入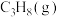 发生反应Ⅰ,下列能说明该反应达到平衡状态的是______(填字母)。
发生反应Ⅰ,下列能说明该反应达到平衡状态的是______(填字母)。
(3)不同压强下,在密闭容器中充入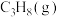 发生反应Ⅰ,丙烷平衡转化率随温度变化关系如图:
发生反应Ⅰ,丙烷平衡转化率随温度变化关系如图:_________ 。
② ,
, 压强下,若进料组成中加入惰性气体Ar,a点将
压强下,若进料组成中加入惰性气体Ar,a点将________ (填“上移”、“下移”或“不移动”)。
③ ,
, 时,a点对应的平衡常数
时,a点对应的平衡常数 =
=________  (精确到0.01)。
(精确到0.01)。
(4)反应Ⅱ制备丙烯时还会生成 、
、 等副产物,在催化剂的作用下,反应相同时间,
等副产物,在催化剂的作用下,反应相同时间, 的转化率和
的转化率和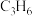 的产率随温度的变化关系如图所示:
的产率随温度的变化关系如图所示: 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是______________ 。
②575℃时,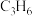 的选择性为
的选择性为______ ,(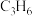 的选择性=
的选择性=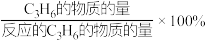
③基于上述研究结果,能提高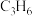 选择性的措施是
选择性的措施是______________ (任写一项)。
Ⅰ.丙烷无氧脱氢法:

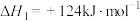
Ⅱ.丙烷氧化脱氢法:
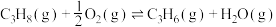

请回答下列问题:
(1)已知
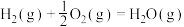
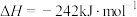 ,由此计算
,由此计算 =
= 。
。(2)某温度下,在恒容密闭容器中充入
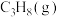 发生反应Ⅰ,下列能说明该反应达到平衡状态的是______(填字母)。
发生反应Ⅰ,下列能说明该反应达到平衡状态的是______(填字母)。A. |
| B.容器内混合气体的密度不再发生变化 |
| C.容器内混合气体的平均相对分子质量不再变化 |
| D.容器内的压强不再发生变化 |
(3)不同压强下,在密闭容器中充入
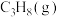 发生反应Ⅰ,丙烷平衡转化率随温度变化关系如图:
发生反应Ⅰ,丙烷平衡转化率随温度变化关系如图: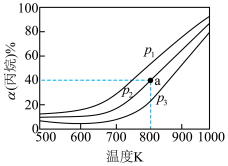
②
 ,
, 压强下,若进料组成中加入惰性气体Ar,a点将
压强下,若进料组成中加入惰性气体Ar,a点将③
 ,
, 时,a点对应的平衡常数
时,a点对应的平衡常数 =
= (精确到0.01)。
(精确到0.01)。(4)反应Ⅱ制备丙烯时还会生成
 、
、 等副产物,在催化剂的作用下,反应相同时间,
等副产物,在催化剂的作用下,反应相同时间, 的转化率和
的转化率和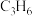 的产率随温度的变化关系如图所示:
的产率随温度的变化关系如图所示:
 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是②575℃时,
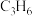 的选择性为
的选择性为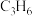 的选择性=
的选择性=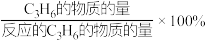
③基于上述研究结果,能提高
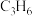 选择性的措施是
选择性的措施是
您最近一年使用:0次
名校
8 . 钴蓝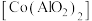 是一种重要的蓝色颜料。利用含钴废料主要成分为
是一种重要的蓝色颜料。利用含钴废料主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备钴蓝的一种工艺流程如图:
等杂质)制备钴蓝的一种工艺流程如图: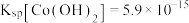 ;
;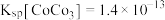 请回答以下问题:
请回答以下问题:
(1)“滤液”的主要成分是____________ ;
(2)“酸浸”中 的作用是
的作用是____________ ;
(3)萃取钴:P204【二(2-乙基已基)磷酸酯,难溶于水,用HA表示】是常用的 萃取剂,其结构简式如图1所示。萃取过程中发生反应:
萃取剂,其结构简式如图1所示。萃取过程中发生反应: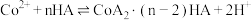 。能使用P204萃取剂萃取水溶液中
。能使用P204萃取剂萃取水溶液中 的原因是
的原因是____________ 。 的操作依次是
的操作依次是________ 、洗涤、干燥。
(5)常温下,若 溶液中
溶液中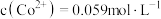 ,为防止沉钴过程中产生
,为防止沉钴过程中产生 沉淀,需控制溶液的pH不高于
沉淀,需控制溶液的pH不高于________ (保留一位小数)
(6)写出灼烧过程中主要反应的化学方程式________________ 。
(7)通过图3装置电解 溶液可以获得
溶液可以获得 单质,中间室获得盐酸。其中使用了阳离子交换膜的是
单质,中间室获得盐酸。其中使用了阳离子交换膜的是________ (填“a”或“b”),阳极的电极反应式为________________ 。
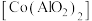 是一种重要的蓝色颜料。利用含钴废料主要成分为
是一种重要的蓝色颜料。利用含钴废料主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备钴蓝的一种工艺流程如图:
等杂质)制备钴蓝的一种工艺流程如图: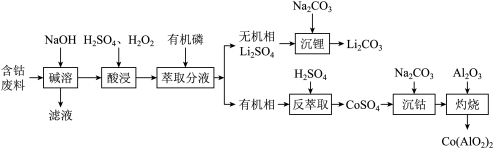
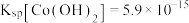 ;
;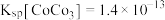 请回答以下问题:
请回答以下问题:(1)“滤液”的主要成分是
(2)“酸浸”中
 的作用是
的作用是(3)萃取钴:P204【二(2-乙基已基)磷酸酯,难溶于水,用HA表示】是常用的
 萃取剂,其结构简式如图1所示。萃取过程中发生反应:
萃取剂,其结构简式如图1所示。萃取过程中发生反应: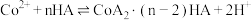 。能使用P204萃取剂萃取水溶液中
。能使用P204萃取剂萃取水溶液中 的原因是
的原因是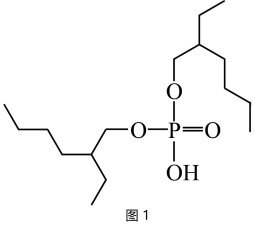
 的操作依次是
的操作依次是(5)常温下,若
 溶液中
溶液中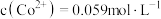 ,为防止沉钴过程中产生
,为防止沉钴过程中产生 沉淀,需控制溶液的pH不高于
沉淀,需控制溶液的pH不高于(6)写出灼烧过程中主要反应的化学方程式
(7)通过图3装置电解
 溶液可以获得
溶液可以获得 单质,中间室获得盐酸。其中使用了阳离子交换膜的是
单质,中间室获得盐酸。其中使用了阳离子交换膜的是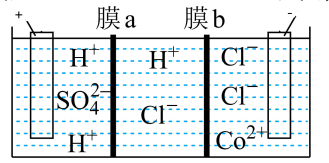
您最近一年使用:0次
名校
解题方法
9 . 离子液体被认为是21世纪最有希望的绿色溶液和功能材料之一,在诸多领域的用途已被研究开发。有几种离子液体由原子序数依次增大的短周期主族元素X、Y、Z、W、R、Q组成。请回答:
(1)基态Z原子的价电子排布式为________ ,基态Y原子占据最高能级的电子云轮廓图为________ 形。
(2)下列说法正确的是____。
(3)试解释 分子中X-W-X键角比
分子中X-W-X键角比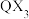 分子中X-Q-X键角大的原因
分子中X-Q-X键角大的原因________ 。
(4)化合物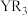 水解生成
水解生成 【也可写作
【也可写作 ,结构如图1】和
,结构如图1】和 。
。
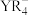 中Y原子的杂化方式为
中Y原子的杂化方式为________ , 晶体中含有
晶体中含有________  氢键。当
氢键。当 溶于水,
溶于水, 分子与水中
分子与水中 结合形成配位键,Y原子杂化方式由
结合形成配位键,Y原子杂化方式由 杂化变为
杂化变为 杂化,请用离子方程式解释
杂化,请用离子方程式解释 为一元弱酸原因
为一元弱酸原因________ 。 ,该晶体密度表达式为
,该晶体密度表达式为________  (YW的摩尔质量为
(YW的摩尔质量为 )。
)。
| 元素 | 元素性质或原子结构 |
| X | 电子只有一种自旋取向 |
| Y | 2p能级上有1个电子 |
| Z | 有6个不同运动状态的电子 |
| W | 2p轨道处于半充满状态,简单氢化物易液化,可用作制冷剂 |
| R | 仅有一个未成对电子,简单阴离子含10个电子 |
| Q | 与W位于同一主族 |
(1)基态Z原子的价电子排布式为
(2)下列说法正确的是____。
| A.氢化物的沸点:R>Z | B.分子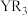 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.元素的电负性:R>X>Z | D.最高价含氧酸的酸性:W>Q |
(3)试解释
 分子中X-W-X键角比
分子中X-W-X键角比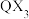 分子中X-Q-X键角大的原因
分子中X-Q-X键角大的原因(4)化合物
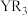 水解生成
水解生成 【也可写作
【也可写作 ,结构如图1】和
,结构如图1】和 。
。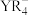 中Y原子的杂化方式为
中Y原子的杂化方式为 晶体中含有
晶体中含有 氢键。当
氢键。当 溶于水,
溶于水, 分子与水中
分子与水中 结合形成配位键,Y原子杂化方式由
结合形成配位键,Y原子杂化方式由 杂化变为
杂化变为 杂化,请用离子方程式解释
杂化,请用离子方程式解释 为一元弱酸原因
为一元弱酸原因 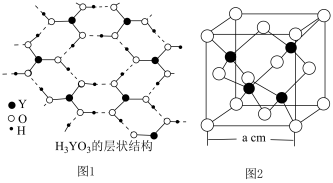
 ,该晶体密度表达式为
,该晶体密度表达式为 (YW的摩尔质量为
(YW的摩尔质量为 )。
)。
您最近一年使用:0次
名校
10 . 根据所学知识回答下列问题:
(1)化学反应中能量的变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。 和
和 反应生成
反应生成 过程中的能量变化如图所示:
过程中的能量变化如图所示:___________ (填标号)。
A.浓硫酸的稀释 B.二氧化碳与灼热的炭的反应
C.甲烷在氧气中燃烧 D.稀盐酸与碳酸氢钠的反应
②离子半径:
___________ (填“>”或“<”) ,判断的规律为
,判断的规律为___________ 。
③对于反应
 ,每转移0.4
,每转移0.4 电子,此时变化的热量为
电子,此时变化的热量为___________  。
。
(2)短周期主族元素a、b、c、d的原子序数依次增大,这四种元素形成的单质依次为m、n、p、q,x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;常温下,0.01 w溶液中
w溶液中 =1.0×10−10,这几种物质的转化关系如图:
=1.0×10−10,这几种物质的转化关系如图:___________ 个自旋平行的未成对电子。
②基态c原子的简化电子排布式为___________ 。
③过量的z通入w溶液中反应的离子方程式为___________ 。
(3)从能量角度来看, 比
比 的稳定性更
的稳定性更___________ (填“强”或“弱”),从原子结构角度分析其原因:___________ 。
(1)化学反应中能量的变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。
 和
和 反应生成
反应生成 过程中的能量变化如图所示:
过程中的能量变化如图所示: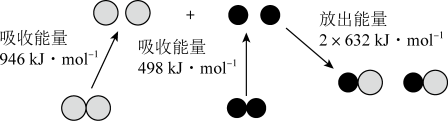
A.浓硫酸的稀释 B.二氧化碳与灼热的炭的反应
C.甲烷在氧气中燃烧 D.稀盐酸与碳酸氢钠的反应
②离子半径:

 ,判断的规律为
,判断的规律为③对于反应

 ,每转移0.4
,每转移0.4 电子,此时变化的热量为
电子,此时变化的热量为 。
。(2)短周期主族元素a、b、c、d的原子序数依次增大,这四种元素形成的单质依次为m、n、p、q,x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;常温下,0.01
 w溶液中
w溶液中 =1.0×10−10,这几种物质的转化关系如图:
=1.0×10−10,这几种物质的转化关系如图: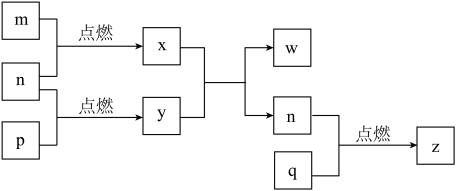
②基态c原子的简化电子排布式为
③过量的z通入w溶液中反应的离子方程式为
(3)从能量角度来看,
 比
比 的稳定性更
的稳定性更
您最近一年使用:0次



