一种绿色甲醇的生产方法是:通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制取甲醇。
主反应:
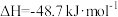
副反应:
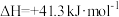
将 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=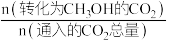 。下列说法错误的是
。下列说法错误的是
主反应:

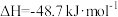
副反应:

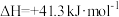
将
 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=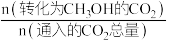 。下列说法错误的是
。下列说法错误的是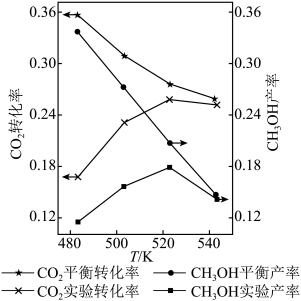
| A.由图可知,催化剂活性最好的温度大约在523K |
| B.483K升温到523K,主反应的反应速率受温度影响更大 |
C.温度由523K升到543K, 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 |
D.为了提高 的平衡转化率和 的平衡转化率和 的平衡产率,可以选择低温、低压条件 的平衡产率,可以选择低温、低压条件 |
更新时间:2024-05-16 11:29:36
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 分解生成
分解生成 和
和 可能的反应机理如图所示。下列说法不正确的是
可能的反应机理如图所示。下列说法不正确的是
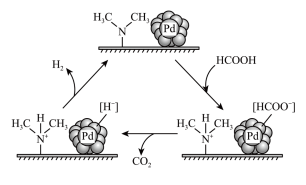
 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 分解生成
分解生成 和
和 可能的反应机理如图所示。下列说法不正确的是
可能的反应机理如图所示。下列说法不正确的是
A.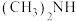 可以和盐酸反应 可以和盐酸反应 |
B.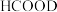 催化释氢反应除生成 催化释氢反应除生成 外,还生成了 外,还生成了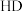 |
C.其他条件不变时,以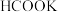 溶液代替 溶液代替 催化释氢的效果更佳 催化释氢的效果更佳 |
| D.该过程破坏了极性键和非极性键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列实验操作与现象和对应结论均正确的是
| 实验操作与现象 | 结论 | |
| A | 加热盛有少量 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝。 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝。 | 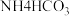 显碱性 显碱性 |
| B | 向某溶液中先加入氯化钡溶液,再滴入盐酸,先产生白色沉淀,后白色沉淀不消失。 | 该溶液中可能含有 |
| C | 其他条件相同的情况下,两只试管中均加入10ml,2mol/L的酸性 ,第一只试管中加入10ml,2mol/L的 ,第一只试管中加入10ml,2mol/L的 ,第二只试管中加入10ml,4mol/L的 ,第二只试管中加入10ml,4mol/L的 ,观察第二只试管褪色更快。 ,观察第二只试管褪色更快。 | 浓度越大,反应速率越大 |
| D | 向2支盛有2mL不同浓度 溶液的试管中同时加入1mL2% 溶液的试管中同时加入1mL2% 溶液,未观察到明显的实验现象差异。 溶液,未观察到明显的实验现象差异。 | 浓度对反应速率的影响不大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】2023年全球电动汽车销量预计超过1400万辆,为全球经济复苏和环境保护做出较大贡献。燃油汽车尾气中除大量CO2外,还含有NO和CO气体。某研究小组用新型催化剂对CO、NO催化转化进行研究,测得一段时间内, 条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。
条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。

反应Ⅱ:

下列叙述不正确 的是
 条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。
条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。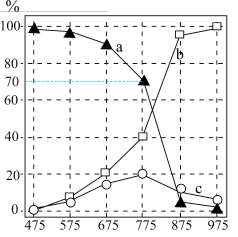


反应Ⅱ:


下列叙述
A.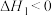 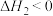 |
| B.曲线c表示:无CO时,NO直接分解为N2的转化率 |
C.775K, 时,不考虑其他反应,该时刻 时,不考虑其他反应,该时刻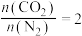 |
| D.温度在775K~875K时,催化剂活性较强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】以CO2和H2为原料,在催化剂作用下合成CH3OH的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
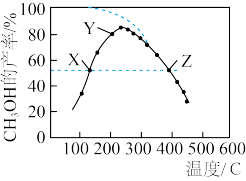
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
 CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
A.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H>0 CH3OH(g)+H2O(g) △H>0 |
| B.图中X点所示条件下,延长反应时间能提高CH3OH的产率 |
| C.图中X、Z点的正反应速率与其逆反应速率均相等 |
| D.选用合适的催化剂不可以减弱副反应的发生 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】工业上以1,4-丁二醇(BD)为原料催化脱氢制备γ-丁内酯(BL),其副反应产物为四氢呋喃( ,THF)、正丁醇(BuOH)以及其他四碳有机物。其他条件相同时,不同温度下,向1L容器中通入4×10-2molBD反应2h,测得BL、THF、BuOH在四碳有机产物中的物质的量分数如表:
,THF)、正丁醇(BuOH)以及其他四碳有机物。其他条件相同时,不同温度下,向1L容器中通入4×10-2molBD反应2h,测得BL、THF、BuOH在四碳有机产物中的物质的量分数如表:
| 温度/℃ | 220 | 240 | 250 | 255 |
| BL/% | 60.2 | 84.6 | 92.6 | 95.2 |
| THF/% | 1.2 | 1.8 | 1.9 | 2.1 |
| BuOH/% | 0.2 | 0.3 | 0.4 | 0.6 |
已知:HO(CH2)4OH(g,BD)
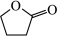 (g,BL)+2H2(g) △H>0
(g,BL)+2H2(g) △H>0
| A.255℃,2h时n(BL)=1.5×10-2mol,则0~2h内v(H2)主反应=1.5×10-2mol•L-1•h-1 |
| B.250℃,2h时n(BD)+n(BL)+n(THF)+n(BuOH)=4×10-2mol |
| C.220℃,2h时n(BL)=9.03×10-3mol,则BD的总转化率为37.5% |
| D.由表中数据可知:220~255℃,BL的选择性随着温度的升高而提高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】二氧化碳加氢制甲烷过程中的主要反应为
①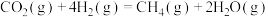
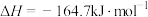
②
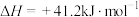
在密闭容器中, 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。

 的选择性
的选择性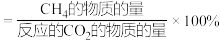 ,下列说法正确的是
,下列说法正确的是
①
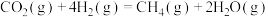
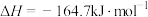
②

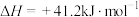
在密闭容器中,
 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。
 的选择性
的选择性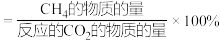 ,下列说法正确的是
,下列说法正确的是A.反应 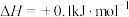 |
| B.该催化剂催化二氧化碳反应的最佳温度范围为350℃~400℃ |
C. 的平衡选择性随着温度的升高而增大 的平衡选择性随着温度的升高而增大 |
D.450℃时,延长反应的时间能使 平衡转化率达到X点的值 平衡转化率达到X点的值 |
您最近一年使用:0次
【推荐2】向相同容积的甲、乙两容器中分别充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)=2SO3(g) △H<0。若甲容器保持恒温恒容,乙容器保持恒温恒压,分别达到平衡。乙容器中平衡时生成SO3为1.6 mol,同时放出热量Q kJ。下列说法正确的是
| A.平衡时,反应放出的热量:甲>乙 |
| B.平衡时,O2的质量:甲<乙 |
| C.乙容器若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO2)大于2.4 mol |
| D.平衡时,向乙容器中再通入一定量的SO3气体,重新达到平衡时,SO2的百分含量升高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】合成氨工业涉及固体燃料的气化,需要研究 与
与 之间的转化。现将一定量的
之间的转化。现将一定量的 与足量碳在体积可变的密闭容器中发生反应:
与足量碳在体积可变的密闭容器中发生反应: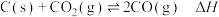 ,测得压强、温度对
,测得压强、温度对 、的平衡组成的影响如图所示。下列说法正确的是
、的平衡组成的影响如图所示。下列说法正确的是

 与
与 之间的转化。现将一定量的
之间的转化。现将一定量的 与足量碳在体积可变的密闭容器中发生反应:
与足量碳在体积可变的密闭容器中发生反应: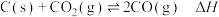 ,测得压强、温度对
,测得压强、温度对 、的平衡组成的影响如图所示。下列说法正确的是
、的平衡组成的影响如图所示。下列说法正确的是
A.平衡体系的压强: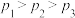 |
B.该反应的活化能: (正) (正) (逆) (逆) |
C.该反应的平衡常数: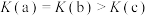 |
D.图中d点按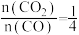 再通入混合气,平衡不移动 再通入混合气,平衡不移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式如下:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
反应Ⅲ:2CO(g)+2H2(g) CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化曲线如图所示。则图中曲线A表示的物质是
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1反应Ⅲ:2CO(g)+2H2(g)
 CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化曲线如图所示。则图中曲线A表示的物质是
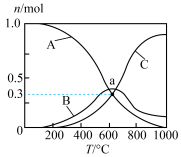
| A.CO | B.CH4 | C.CO2 | D.无法确定 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】T℃时,向两个等体积的恒容密闭容器中,均以n(NO):n(H2)=1:2充入NO与H2发生如下反应:
反应1:2NO(g)+2H2(g) N2(g)+2H2O(g)
N2(g)+2H2O(g)
反应2:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
甲为绝热过程、乙为恒温过程,反应体系的压强随时间变化曲线如图所示,Z点时NO的转化率为80%。
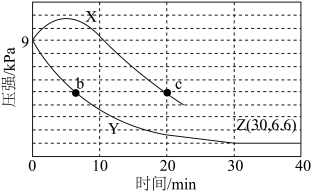
下列说法错误的是
反应1:2NO(g)+2H2(g)
 N2(g)+2H2O(g)
N2(g)+2H2O(g)反应2:N2(g)+3H2(g)
 2NH3(g)
2NH3(g)甲为绝热过程、乙为恒温过程,反应体系的压强随时间变化曲线如图所示,Z点时NO的转化率为80%。

下列说法错误的是
| A.曲线Y代表乙容器 |
| B.气体的总物质的量:nb>nc |
| C.若乙为恒温恒压过程,则平衡时NO的转化率小于80% |
| D.曲线Y从开始到Z点,用分压表示的H2消耗速率为0.14kPa•min-1 |
您最近一年使用:0次

 C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:
C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:
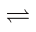 xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol,B:0.3mol,C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%。则x的值为(
xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol,B:0.3mol,C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%。则x的值为(

