名校
1 . NaHCO3溶液不仅在受热时能分解放出CO2,而且在室温时亦能分解。
请回答下列问题:
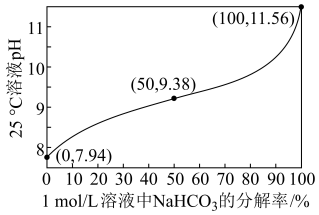
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。___________ 。
②等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性___________ (填“强”或“弱”)。
③0.5 mol·L-1 Na2CO3溶液的pH=___________ 。
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。___________ 。
②一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为___________ 。
③实验结果偏低的原因是___________ 。
请回答下列问题:
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。
②等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性
③0.5 mol·L-1 Na2CO3溶液的pH=
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。

②一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为
③实验结果偏低的原因是
您最近一年使用:0次
2024-01-17更新
|
131次组卷
|
2卷引用:四川省绵阳市东辰学校2022-2023学年高一上学期期末模拟化学试卷
名校
解题方法
2 . 研发二氧化碳的碳捕集和碳利用技术及合成氨是科学研究热点问题,回答下列问题:
(1)常温常压下,一些常见物质的燃烧热如表所示:
已知:
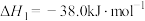
则

_____  ,该反应在
,该反应在______ (填“高温”“低温”或“任意温度”)下能自发进行。
(2) 催化加氢制取甲醇,反应如下:
催化加氢制取甲醇,反应如下:
主反应:

副反应:
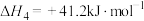
在一定条件下,向某 恒容密闭容器中充入
恒容密闭容器中充入 和
和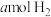 发生反应,起始总压强为
发生反应,起始总压强为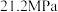 。实验测得
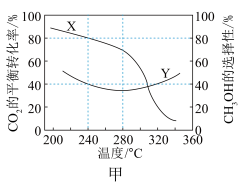
。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图所示:
的选择性随温度变化如图所示:
已知: 的选择性
的选择性 %。
%。
图中表示平衡时 的选择性的曲线为
的选择性的曲线为_____ (填“X”或“Y”),温度高于280℃时,曲线Y随温度升高而升高的原因是________ 。240℃时,反应 容器内达到平衡状态,副反应的
容器内达到平衡状态,副反应的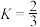 ,初始充入
,初始充入 的物质的量
的物质的量
_____ mol。
(3)工业利用 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含
催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。
①除去原料气中CO的理由是___________ 。
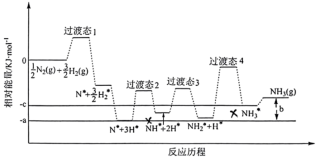
②研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。该反应历程中最大活化能对应步骤的化学方程式为______ 。
③铁催化合成氨时 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程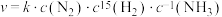 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是_____ 。
(1)常温常压下,一些常见物质的燃烧热如表所示:
| 名称 | 氢气 | 甲烷 | 一氧化碳 | 甲醇 |
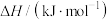 |  |  |  |  |

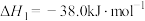
则


 ,该反应在
,该反应在(2)
 催化加氢制取甲醇,反应如下:
催化加氢制取甲醇,反应如下:主反应:


副反应:

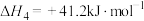
在一定条件下,向某
 恒容密闭容器中充入
恒容密闭容器中充入 和
和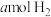 发生反应,起始总压强为
发生反应,起始总压强为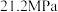 。实验测得
。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图所示:
的选择性随温度变化如图所示:
已知:
 的选择性
的选择性 %。
%。图中表示平衡时
 的选择性的曲线为
的选择性的曲线为 容器内达到平衡状态,副反应的
容器内达到平衡状态,副反应的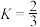 ,初始充入
,初始充入 的物质的量
的物质的量
(3)工业利用
 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含
催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。①除去原料气中CO的理由是
②研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。该反应历程中最大活化能对应步骤的化学方程式为

③铁催化合成氨时
 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程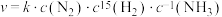 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是
您最近一年使用:0次
名校
解题方法
3 . 钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互熔,其固熔体为面心立方晶格。
(1)Co元素在周期表中属于_____ 区,其原子的简化电子排布式为________ 。
(2)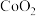 晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述
晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述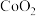 化学组成的是________(填序号)。
化学组成的是________(填序号)。
(3)二氯二吡啶合铂分子是一种铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。
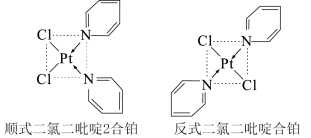
①顺式二氯二吡啶合铂分子中含有的化学键类型为___ (填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
②反式二氯二吡啶合铂分子是___ 分子(填“极性”或“非极性”)。
③常用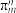 表示分子中的大
表示分子中的大 键,其中m代表参与形成大
键,其中m代表参与形成大 键的原子总数,n代表参与形成大
键的原子总数,n代表参与形成大 键的电子总数,如苯分子中存在
键的电子总数,如苯分子中存在 大
大 键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为
键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为___ ,吡啶分子中的大 键可表示为
键可表示为___ 。
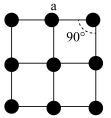
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y、z轴的投影图均为如下图所示,则铂原子采取的堆积方式为___ 。该堆积方式中的空间利用率为_______ 。若金属铂的密度为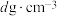 ,则晶胞参数
,则晶胞参数
______ nm(列出计算表达式)。
(1)Co元素在周期表中属于
(2)
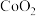 晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述
晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述 化学组成的是________(填序号)。
化学组成的是________(填序号)。A. | B.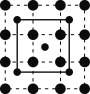 | C. | D. |
(3)二氯二吡啶合铂分子是一种铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。


①顺式二氯二吡啶合铂分子中含有的化学键类型为
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
②反式二氯二吡啶合铂分子是
③常用
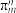 表示分子中的大
表示分子中的大 键,其中m代表参与形成大
键,其中m代表参与形成大 键的原子总数,n代表参与形成大
键的原子总数,n代表参与形成大 键的电子总数,如苯分子中存在
键的电子总数,如苯分子中存在 大
大 键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为
键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为 键可表示为
键可表示为(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y、z轴的投影图均为如下图所示,则铂原子采取的堆积方式为
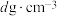 ,则晶胞参数
,则晶胞参数

您最近一年使用:0次
2023高三·全国·专题练习
名校
解题方法
4 . 工业上利用石煤矿粉(主要含 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:

已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为 、
、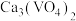 、
、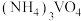 ;
;
②不同pH下,V元素在溶液中的主要存在形式见下表:
③25℃时,
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(2)滤渣Ⅰ的成分为_________ (填化学式)。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到________ 操作单元中循环使用。
(4)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①_________ 。②________ ;25℃时,测得“转化”后,滤液中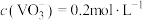 为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少______  。
。
(5)“煅烧”的, 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为
,反应中氧化剂与还原剂物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:
已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为
 、
、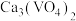 、
、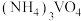 ;
;②不同pH下,V元素在溶液中的主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |

回答下列问题:
(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤渣Ⅰ的成分为
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到
(4)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①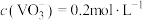 为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少 。
。(5)“煅烧”的,
 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为
,反应中氧化剂与还原剂物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
2024-01-11更新
|
148次组卷
|
5卷引用:四川省绵阳中学2022-2023学年高三上学期高考适应性考试(三)理综试题
四川省绵阳中学2022-2023学年高三上学期高考适应性考试(三)理综试题(已下线)预测卷03-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)先机卷 01 -【热题狂飙】2023年高考化学样卷(全国卷专用)山东省聊城市2022-2023学年高三下学期开学考试化学试题辽宁省葫芦岛市2024届高三一模化学试题
名校
解题方法
5 . H2O2为绿色氧化剂,用途广泛。工业上可用乙基蒽醌EAQ(C16H12O2)法制备:
①C16H12O2(EAQ)+H2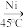 H16H14O2 (EHAQ)
H16H14O2 (EHAQ)
②C16H14O2(EHAQ)+O2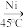 C16H12O2(EAQ)+H2O2
C16H12O2(EAQ)+H2O2
(1)该制备的总反应方程式为___________ 。
(2)某实验小组选用如图所示仪器模拟工业法制备H2O2:(夹持装置和加热装置略)
已知:H2O、HX会造成Ni催化剂中毒;制备H2的反应为:Zn+2HCl=ZnCl2+H2↑。
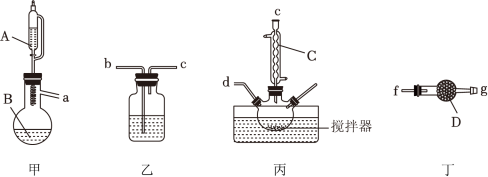
①检查气密性后,向三颈烧瓶中加入乙基蒽醌(EAQ)、CCl4和镍,通入H2控温45℃。用题中小写字母表示的接口连接顺序为a→___________ →f(仪器D使用一次,其余仪器可重复使用),仪器D的作用为 ___________ 。
②一段时间后,丙装置中改通入由亚硝酸钠溶液和氯化铵溶液反应生成的N2该反应的离子方程式为___________ ,略去该步的危害为 ___________ 。
③然后再向丙装置中通入O2,继续反应一段时间,仍维持45℃的原因为___________ 。
④过滤三颈烧瓶中混合物,加___________ (填试剂名称)萃取、分液、减压蒸馏,得产品。
(3)测定产品纯度:取10.00mL产品配成100.00mL溶液,取20.00mL于锥形瓶中,用0.1000mol/L酸性KMnO4标准溶液滴定,平行滴定三次,分别消耗KMnO4溶液体积为41.98mL、42.02mL、42.57mL,产品中H2O2的浓度为___________ mol/L。
①C16H12O2(EAQ)+H2
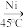 H16H14O2 (EHAQ)
H16H14O2 (EHAQ)②C16H14O2(EHAQ)+O2
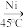 C16H12O2(EAQ)+H2O2
C16H12O2(EAQ)+H2O2(1)该制备的总反应方程式为
(2)某实验小组选用如图所示仪器模拟工业法制备H2O2:(夹持装置和加热装置略)
已知:H2O、HX会造成Ni催化剂中毒;制备H2的反应为:Zn+2HCl=ZnCl2+H2↑。

①检查气密性后,向三颈烧瓶中加入乙基蒽醌(EAQ)、CCl4和镍,通入H2控温45℃。用题中小写字母表示的接口连接顺序为a→
②一段时间后,丙装置中改通入由亚硝酸钠溶液和氯化铵溶液反应生成的N2该反应的离子方程式为
③然后再向丙装置中通入O2,继续反应一段时间,仍维持45℃的原因为
④过滤三颈烧瓶中混合物,加
(3)测定产品纯度:取10.00mL产品配成100.00mL溶液,取20.00mL于锥形瓶中,用0.1000mol/L酸性KMnO4标准溶液滴定,平行滴定三次,分别消耗KMnO4溶液体积为41.98mL、42.02mL、42.57mL,产品中H2O2的浓度为
您最近一年使用:0次
名校
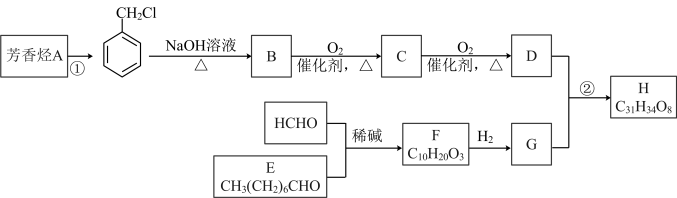
6 . 一种用于治疗高血脂的新药H的合成路线如图:
已知: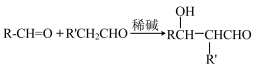
回答下列问题:
(1)反应①的反应类型为___________ ,B的化学名称为 ___________ 。
(2)下列关于C的说法正确的是 ___________(填序号)。
(3)F中所含官能团的名称是___________ 。
(4)写出D与G反应的化学方程式___________ 。
(5)化合物Ⅰ的相对分子质量比化合物D大14,且满足下列条件的Ⅰ的同分异构体有___________ 种。其中核磁共振氢谱图中有4组峰,峰面积比为1:2:2:3的结构简式为 ___________ 。
①属于芳香族化合物;
②能发生水解反应;
③能发生银镜反应。
(6)参照上述路线,设计由B和乙醛制备肉桂醛(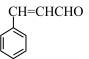 )的合成路线
)的合成路线 ___________ (无机试剂任选)。

已知:

回答下列问题:
(1)反应①的反应类型为
(2)下列关于C的说法正确的是 ___________(填序号)。
| A.能与Na反应生成H2 |
| B.能与新制Cu(OH)2悬浊液反应 |
| C.能使溴水褪色 |
| D.1molC最多能与3molH2发生加成反应 |
(3)F中所含官能团的名称是
(4)写出D与G反应的化学方程式
(5)化合物Ⅰ的相对分子质量比化合物D大14,且满足下列条件的Ⅰ的同分异构体有
①属于芳香族化合物;
②能发生水解反应;
③能发生银镜反应。
(6)参照上述路线,设计由B和乙醛制备肉桂醛(
 )的合成路线
)的合成路线
您最近一年使用:0次
7 . 乙烯是重要的工业原料,可用下列方法制备。
Ⅰ、CO2催化加氢法制CH2=CH2:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g)ΔH
已知:H2、CH2=CH2的燃烧热分别为285.8kJ/mol、1411.0kJ/mol;
H2O(l)=H2O(g) ΔH1=+44.0kJ/mol
(1)该反应ΔH=___________ kJ/mol。
(2)在0.1MPa,将CO2和H2按个数比为2:3充入刚性容器中,分别在不同催化剂条件下发生反应,测得相同时间CO2的转化率与温度的关系如图所示:

①一定温度下,下列有关说法不正确的是___________ 。
A.向反应体系中加入少量无水CaCl2固体,可提高CH2=CH2的产率
B.达平衡时,c(CO2):c(H2)一定为2:3
C.当体系中压强不再改变时,反应一定达到平衡
D.使用合适的催化剂可以得到更多的CH2=CH2
②230℃时,Kp=___________ (列出计算式即可)
Ⅱ.乙醇消去法制CH2=CH2:C2H5OH(1)=CH2=CH2(g)+H2O(g) ΔH=+44.2kJ/mol。浓硫酸催化下,用C2H5OH制备CH2=CH2,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙醇进料量的关系如图所示(保持其他条件相同)。
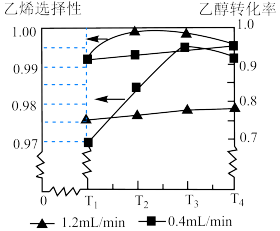
(3)当乙醇进料量一定时,温度升高,乙醇的转化率___________ 。该制备反应的最佳条件为 ___________ ,T3之后,乙烯选择性降低可能的原因为 ___________ 。
Ⅲ.电化学法制CH2=CH2:
(4)工业上用电解原理制备乙烯,装置如图所示:
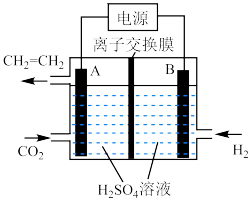
①该电解池最好选___________ (填“阳”或“阴”)离子交换膜;
②阴极的电极反应为___________ 。
Ⅰ、CO2催化加氢法制CH2=CH2:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g)ΔH
已知:H2、CH2=CH2的燃烧热分别为285.8kJ/mol、1411.0kJ/mol;
H2O(l)=H2O(g) ΔH1=+44.0kJ/mol
(1)该反应ΔH=
(2)在0.1MPa,将CO2和H2按个数比为2:3充入刚性容器中,分别在不同催化剂条件下发生反应,测得相同时间CO2的转化率与温度的关系如图所示:

①一定温度下,下列有关说法不正确的是
A.向反应体系中加入少量无水CaCl2固体,可提高CH2=CH2的产率
B.达平衡时,c(CO2):c(H2)一定为2:3
C.当体系中压强不再改变时,反应一定达到平衡
D.使用合适的催化剂可以得到更多的CH2=CH2
②230℃时,Kp=
Ⅱ.乙醇消去法制CH2=CH2:C2H5OH(1)=CH2=CH2(g)+H2O(g) ΔH=+44.2kJ/mol。浓硫酸催化下,用C2H5OH制备CH2=CH2,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙醇进料量的关系如图所示(保持其他条件相同)。

(3)当乙醇进料量一定时,温度升高,乙醇的转化率
Ⅲ.电化学法制CH2=CH2:
(4)工业上用电解原理制备乙烯,装置如图所示:

①该电解池最好选
②阴极的电极反应为
您最近一年使用:0次
2022·北京·高考真题
8 . 某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。
ⅱ、浓碱条件下,MnO 可被OH-还原为MnO
可被OH-还原为MnO 。
。
ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
(1)B中试剂是_____ 。
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为_____ 。
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是_____ 。
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO 氧化为MnO
氧化为MnO 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:_____ ,但通过实验测定溶液的碱性变化很小。
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_____ ,溶液绿色缓慢加深,原因是MnO2被_____ (填化学式)氧化,可证明实验Ⅲ的悬浊液中氧化剂过量。
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是_____ 。
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:_____ 。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO
 (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。ⅱ、浓碱条件下,MnO
 可被OH-还原为MnO
可被OH-还原为MnO 。
。ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
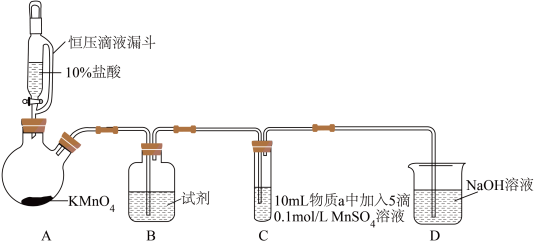
| 实验 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO
 氧化为MnO
氧化为MnO 。
。①用化学方程式表示可能导致溶液碱性减弱的原因:
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:
您最近一年使用:0次
2023-11-29更新
|
877次组卷
|
29卷引用:四川省成都市树德中学2022-2023学年高三上学期入学考试理综化学试题
四川省成都市树德中学2022-2023学年高三上学期入学考试理综化学试题(已下线)2022年北京市高考真题化学试题(部分试题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)2022年北京市高考真题化学试题(已下线)第28讲 定性、定量实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)2022年北京高考真题变式题1-14(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)专题三 离子反应-实战高考·二轮复习核心突破(已下线)2022年北京高考真题化学试题变式题(实验探究题)新疆乌鲁木齐市第101中学2022-2023学年高一上学期12月月考化学试题突破超重点 高效突破综合实验 实验4 创新探究实验角度1控制变量法探究(已下线)题型46 实验原理探究型综合实验(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 氯气和卤族元素(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)北京一零一中学2023-2024学年高三上学期11月统练五化学试题(已下线)微专题 物质性质综合实验探究北京市日坛中学2023-2024学年高三上学期10月检测化学试题北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题江苏省苏州市工业园区星海实验高级中学2023-2024学年高一上学期12月调研化学试题山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
名校
解题方法
9 . 某温度下,恒容密闭容器内发生反应:H2(g)+I2 g)  2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
 2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是| A.混合气体颜色变深 | B.混合气体密度变大 |
| C.容器内压强变小 | D.氢气的体积分数变小 |
您最近一年使用:0次
2023-10-21更新
|
689次组卷
|
25卷引用:四川省南充市2021-2022学年高二下学期期末考试化学试题
四川省南充市2021-2022学年高二下学期期末考试化学试题北京市海淀区2021~2022学年高二上学期期末化学试题(已下线)第04练 化学平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)安徽省舒城中学2021-2022学年高二下学期第一次月考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期末检测化学试题北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题湖北省宜昌英杰学校2022-2023学年高二上学期10月测试化学试题北京市第三十五中学2022-2023学年高二上学期10月月考化学试题甘肃省兰州第一中学2022-2023学年高二上学期期末考试化学试题陕西省洛南中学2022-2023学年高二上学期10月月考化学试题北京市海淀区2020届高三上学期期末考试化学试题天津市河北区2020届高三年级“停课不停学”期间线上测试化学试题吉林省汪清县汪清四中2021-2022学年高二上学期第一次阶段考试化学试题 陕西省咸阳市武功县2021--2022学年高二上学期质量调研化学试题天津市南开区2023届高三下学期质量监测 ( 二 ) 化学试题(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)天津市第一中学2023-2024学年高二上学期10月月考化学试题北京市海淀区2023-2024学年高二上学期期中考试化学试题北京市和平街第一中学2023-2024学年高二上学期10月阶段性练习化学试题北京市第五十中学2023-2024学年高二上学期期中考试化学试题北京市广渠门中学2023-2024学年高二上学期期中考试化学试题 北京市第一六一中学2023-2024学年高二上学期10月月考化学试题安徽省合肥卓越中学2023-2024学年高二上学期期中考试化学试题北京市北京师范大学附属中学平谷第一分校2023-2024学年高二上学期期中考试化学试题天津市南开中学2023-2024学年高三下学期第四次月考化学试卷
10 . 下面有关晶体的叙述中,不正确的是
A.氯化钠晶体中,每个 周围距离相等的 周围距离相等的 共有6个 共有6个 |
| B.金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
C.氯化铯晶体中,每个 周围紧邻8个 周围紧邻8个 |
D.干冰晶体中,每个 分子周围紧邻12个 分子周围紧邻12个 分子 分子 |
您最近一年使用:0次
2023-10-09更新
|
190次组卷
|
2卷引用:四川省盐亭中学2022-2023学年高二上学期期中教学质量监测(理科)化学试题



