NaHCO3溶液不仅在受热时能分解放出CO2,而且在室温时亦能分解。
请回答下列问题:
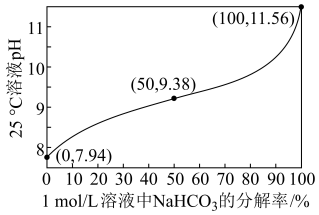
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。___________ 。
②等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性___________ (填“强”或“弱”)。
③0.5 mol·L-1 Na2CO3溶液的pH=___________ 。
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。___________ 。
②一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为___________ 。
③实验结果偏低的原因是___________ 。
请回答下列问题:
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。
②等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性
③0.5 mol·L-1 Na2CO3溶液的pH=
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。

②一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为
③实验结果偏低的原因是
更新时间:2024-01-17 15:58:00
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】向盛有300mLNaHCO3和Na2CO3混合溶液的烧杯中逐滴加入0.40mol·L-1的Ba(OH)2溶液,加入500mL恰好完全反应,溶液中c(OH-)为0.35mol·L-1。请回答:(忽略溶液混合时体积的变化)
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=___________ 。
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=___________ 。
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】Ⅰ.铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是____________________ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是______________ 。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
Ⅱ.工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解3.00 g K2FeO4样品,调节pH值使高铁酸根全部被还原成铁离子,再调节pH为3~4,用1.0 mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,滴定终点时,消耗Na2S2O3标准溶液18.00mL。
①滴定终点的现象是_______________________________________ 。
②原样品中高铁酸钾的质量分数为______________ 。
Ⅲ.A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行):A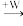 B
B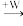 C。A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
C。A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
(1)若将标准状况下2.24 L的W通入150 mL 1 mol·L-1的A溶液中,充分反应。总反应的离子方程式为______________________________________________ 。
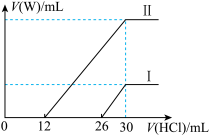
(2)向两份30 mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.2 mol·L-1盐酸,如图所示,Ⅰ和Ⅱ分别为向M、N溶液中加入盐酸的体积V(HCl)与产生W气体的体积V(W)的关系。则M、N两溶液中相同溶质的物质的量之比为__________ 。
Ⅳ.简述检验某液态卤代烃中是否含有氯元素的方法:_______________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
Ⅱ.工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解3.00 g K2FeO4样品,调节pH值使高铁酸根全部被还原成铁离子,再调节pH为3~4,用1.0 mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,滴定终点时,消耗Na2S2O3标准溶液18.00mL。
①滴定终点的现象是
②原样品中高铁酸钾的质量分数为
Ⅲ.A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行):A
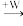 B
B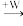 C。A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
C。A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。(1)若将标准状况下2.24 L的W通入150 mL 1 mol·L-1的A溶液中,充分反应。总反应的离子方程式为
(2)向两份30 mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.2 mol·L-1盐酸,如图所示,Ⅰ和Ⅱ分别为向M、N溶液中加入盐酸的体积V(HCl)与产生W气体的体积V(W)的关系。则M、N两溶液中相同溶质的物质的量之比为

Ⅳ.简述检验某液态卤代烃中是否含有氯元素的方法:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】许多钠的化合物的水溶液呈碱性,这些化合物之间往往可以相互转化。
(1)写出 的电子式
的电子式___________ ; 所含化学键的类型有
所含化学键的类型有___________ (填写下列字母)。
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2) 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
___________  (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
(3)该固体样品应在___________ (填仪器名称)中加热至恒重。该过程主要发生的化学方程式为___________ 。
(4)对某一样品做四组平行实验,数据结果如下:
则该样品中 质量分数为
质量分数为___________ (表示成百分数,精确到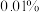 )。
)。
(5)若 质量分数标准值为
质量分数标准值为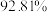 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有___________ (填写下列字母)
a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
(1)写出
 的电子式
的电子式 所含化学键的类型有
所含化学键的类型有a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2)
 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
 (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。(3)该固体样品应在
(4)对某一样品做四组平行实验,数据结果如下:
| 所测物理量 | 第一组 | 第二组 | 第三组 | 第四组 |
| 容器质量/g | 17.221 | 18.565 | 18.652 | 17.094 |
| 加热前容器与样品质量/g | 24.864 | 26.800 | 26.935 | 24.338 |
| 恒重后容器与样品质量/g | 22.209 | 23.936 | 23.992 | 21.823 |
 质量分数为
质量分数为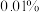 )。
)。(5)若
 质量分数标准值为
质量分数标准值为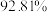 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】A、 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系
是中学常见的无机物,存在如图转化关系 部分生成物和反应条件略去
部分生成物和反应条件略去 。
。
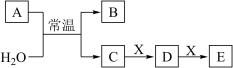
(1)若A的焰色反应为黄色,且A为化合物,回答下列问题:
①A与H2O反应的离子方程式为_______ 。
②若X为具有较强还原性的非金属单质,通常为黑色粉末,写出E的化学式_______ 。
③若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为_______ 。
a.NaCl溶液 b.BaCl2 溶液 c.Ca(OH)2溶液 d.NaOH溶液
(2)若A为黄绿色气体,具有很强的氧化性,若 溶液显强酸性,则
溶液显强酸性,则 的化学式为
的化学式为_______ 。
 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系
是中学常见的无机物,存在如图转化关系 部分生成物和反应条件略去
部分生成物和反应条件略去 。
。
(1)若A的焰色反应为黄色,且A为化合物,回答下列问题:
①A与H2O反应的离子方程式为
②若X为具有较强还原性的非金属单质,通常为黑色粉末,写出E的化学式
③若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为
a.NaCl溶液 b.BaCl2 溶液 c.Ca(OH)2溶液 d.NaOH溶液
(2)若A为黄绿色气体,具有很强的氧化性,若
 溶液显强酸性,则
溶液显强酸性,则 的化学式为
的化学式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】根据所学知识回答下列问题:
(1)A 与NaOH 溶液反应,有如下转化关系(若产物中有水生成则省略,未表示出来)。
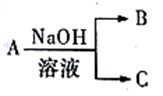
①若A 为常见金属单质,C 为气体,写出向B溶液中通入过量CO2 反应的离子方程式:_______________ ;
②若A 为空气的成分之一,能造成温室效应,当向100 mL1mol/L NaOH 溶液中通入1.344 L 气体(标准状况下)充分反应后,生成B和C 的物质的量之比为______ (B的摩尔质量大于C);
③若A 为AlCl3,写出A 与NaOH 按物质的量之比3 :10 混合时发生反应的离子方程式:______________ 。
(2)氯化铁溶液可用于腐蚀印刷铜电路板,请写出相关的离子方程式:______________ ,如何检验溶液中的铁离子已经完全反应: ______________ 。
(3)现有AlCl3 和FeCl3 混合溶液,其中A13+ 和Fe3+ 的物质的量之和为0.1mol,向此溶液中加入80 mL浓度为4mol/L 的NaOH 溶液,使其充分反应,设原混合溶液中A13+ 的物质的量与A13+ 和Fe3+ 的总物质的量的比值为x。当最终生成的沉淀中只有Fe(OH)3时,x 的取值范围是______ ,请在图中画出沉淀总量(mol)随x(0→1.0)变化的曲线:______________

(1)A 与NaOH 溶液反应,有如下转化关系(若产物中有水生成则省略,未表示出来)。

①若A 为常见金属单质,C 为气体,写出向B溶液中通入过量CO2 反应的离子方程式:
②若A 为空气的成分之一,能造成温室效应,当向100 mL1mol/L NaOH 溶液中通入1.344 L 气体(标准状况下)充分反应后,生成B和C 的物质的量之比为
③若A 为AlCl3,写出A 与NaOH 按物质的量之比3 :10 混合时发生反应的离子方程式:
(2)氯化铁溶液可用于腐蚀印刷铜电路板,请写出相关的离子方程式:
(3)现有AlCl3 和FeCl3 混合溶液,其中A13+ 和Fe3+ 的物质的量之和为0.1mol,向此溶液中加入80 mL浓度为4mol/L 的NaOH 溶液,使其充分反应,设原混合溶液中A13+ 的物质的量与A13+ 和Fe3+ 的总物质的量的比值为x。当最终生成的沉淀中只有Fe(OH)3时,x 的取值范围是

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再产生CO2气体为止,在此过程中,溶液中的碳酸氢根离子浓度的变化是___ 。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为___ 。
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有___ 种。若固体混合物A的质量m(A)为定值,生成气体的量为定值,则A的可能组成是(填写化学式):___ 、___ ;___ 、___ 。(可以不填满)
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是___ mol。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是
您最近一年使用:0次



