许多钠的化合物的水溶液呈碱性,这些化合物之间往往可以相互转化。
(1)写出 的电子式
的电子式___________ ; 所含化学键的类型有
所含化学键的类型有___________ (填写下列字母)。
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2) 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
___________  (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
(3)该固体样品应在___________ (填仪器名称)中加热至恒重。该过程主要发生的化学方程式为___________ 。
(4)对某一样品做四组平行实验,数据结果如下:
则该样品中 质量分数为
质量分数为___________ (表示成百分数,精确到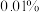 )。
)。
(5)若 质量分数标准值为
质量分数标准值为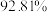 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有___________ (填写下列字母)
a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
(1)写出
 的电子式
的电子式 所含化学键的类型有
所含化学键的类型有a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2)
 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
 (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。(3)该固体样品应在
(4)对某一样品做四组平行实验,数据结果如下:
| 所测物理量 | 第一组 | 第二组 | 第三组 | 第四组 |
| 容器质量/g | 17.221 | 18.565 | 18.652 | 17.094 |
| 加热前容器与样品质量/g | 24.864 | 26.800 | 26.935 | 24.338 |
| 恒重后容器与样品质量/g | 22.209 | 23.936 | 23.992 | 21.823 |
 质量分数为
质量分数为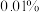 )。
)。(5)若
 质量分数标准值为
质量分数标准值为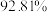 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
21-22高一下·上海宝山·期末 查看更多[2]
上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题(已下线)专题02 反应热的测量和计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
更新时间:2022-06-29 11:53:22
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】Ⅰ.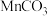 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。
可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。
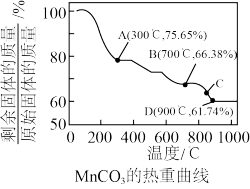
(1)300℃时,剩余固体中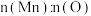 为
为_______ 。
(2)图中C点对应固体的成分为_______ (填化学式)。
Ⅱ. 是常见温室气体,将一定量的气体
是常见温室气体,将一定量的气体 通入100mL某浓度的NaOH溶液得F溶液,向F溶液中逐滴加入
通入100mL某浓度的NaOH溶液得F溶液,向F溶液中逐滴加入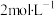 的盐酸,产生
的盐酸,产生 的体积与所加盐酸体积之间的关系如图所示。
的体积与所加盐酸体积之间的关系如图所示。
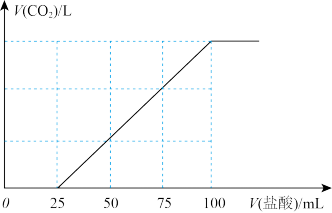
(3)F溶质与足量石灰水发生反应最多可得沉淀的质量为_______ 。
Ⅲ.完成问题
(4)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[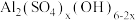 ]溶液。若溶液的pH偏高,则碱式硫酸铝产率下降且有气体C产生,用化学方程式表示其原因:
]溶液。若溶液的pH偏高,则碱式硫酸铝产率下降且有气体C产生,用化学方程式表示其原因:_______ 。
 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。
可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。
(1)300℃时,剩余固体中
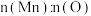 为
为(2)图中C点对应固体的成分为
Ⅱ.
 是常见温室气体,将一定量的气体
是常见温室气体,将一定量的气体 通入100mL某浓度的NaOH溶液得F溶液,向F溶液中逐滴加入
通入100mL某浓度的NaOH溶液得F溶液,向F溶液中逐滴加入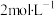 的盐酸,产生
的盐酸,产生 的体积与所加盐酸体积之间的关系如图所示。
的体积与所加盐酸体积之间的关系如图所示。
(3)F溶质与足量石灰水发生反应最多可得沉淀的质量为
Ⅲ.完成问题
(4)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[
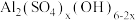 ]溶液。若溶液的pH偏高,则碱式硫酸铝产率下降且有气体C产生,用化学方程式表示其原因:
]溶液。若溶液的pH偏高,则碱式硫酸铝产率下降且有气体C产生,用化学方程式表示其原因:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】向盛有300mLNaHCO3和Na2CO3混合溶液的烧杯中逐滴加入0.40mol·L-1的Ba(OH)2溶液,加入500mL恰好完全反应,溶液中c(OH-)为0.35mol·L-1。请回答:(忽略溶液混合时体积的变化)
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=___________ 。
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=___________ 。
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】取一定质量NaHCO3和Na2O的固体混合物溶于适量的水,向所得溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生的气体体积与所加盐酸体积之间的关系如图所示。试回答下列问题:

(1)盐酸的物质的量浓度为_____ 。
(2)固体混合物中NaHCO3与Na2O物质的量之比_____ 。

(1)盐酸的物质的量浓度为
(2)固体混合物中NaHCO3与Na2O物质的量之比
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g) CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g) CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
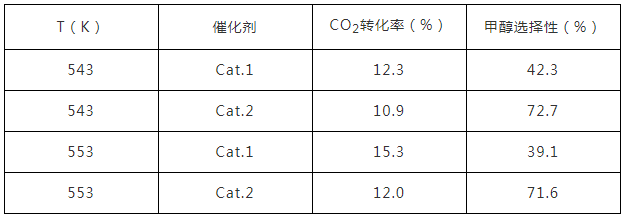
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l) H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=_____________ ;反应II的ΔH2=______________ kJ·mol-1。
(2)在图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图 。_________

CO2(g)+3 H2(g)
 CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 ICO2(g)+ H2(g)
 CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)
 H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=
(2)在图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】铜及其化合物应用广泛。回答下列问题:
(1)目前铜可采用如下方法制备:
方法1:火法炼铜: ;
;
方法2:湿法炼铜: 。
。
上述两种方法中,方法2比方法1更好,其原因是_______ (写出一条原因即可)。上述两种方法冶炼铜中,若转移的电子数相同,则方法1和方法2冶炼出的铜的质量之比为_______ 。
(2)黄铜矿的含铜成分为 ,常采用
,常采用 溶液浸取,生成
溶液浸取,生成 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为_______ 。
(3)将 、
、 和
和 组成的混合物加入
组成的混合物加入 溶液恰好使混合物完全溶解,同时收集到2.24L(标准状况)
溶液恰好使混合物完全溶解,同时收集到2.24L(标准状况) 气体。若将此混合物用足量的
气体。若将此混合物用足量的 加热还原,所得固体的质量为
加热还原,所得固体的质量为_______ g。
(4) 和
和 的燃烧热分别为
的燃烧热分别为 、
、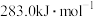 ,已知
,已知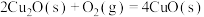
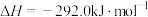 ;则
;则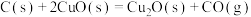 的
的
_______  。
。
(5)某同学利用下图装置进行铁上电镀铜的实验探究。
①实验ⅰ中气体减少的原因是_______ 。
②实验ⅰ中,推测产生 ,可能发生的反应有
,可能发生的反应有 、
、_______ 。
③随着阴极析出 ,实验ⅱ中
,实验ⅱ中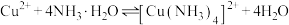 平衡不移动,理由是
平衡不移动,理由是_______ 。
(1)目前铜可采用如下方法制备:
方法1:火法炼铜:
 ;
;方法2:湿法炼铜:
 。
。上述两种方法中,方法2比方法1更好,其原因是
(2)黄铜矿的含铜成分为
 ,常采用
,常采用 溶液浸取,生成
溶液浸取,生成 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为(3)将
 、
、 和
和 组成的混合物加入
组成的混合物加入 溶液恰好使混合物完全溶解,同时收集到2.24L(标准状况)
溶液恰好使混合物完全溶解,同时收集到2.24L(标准状况) 气体。若将此混合物用足量的
气体。若将此混合物用足量的 加热还原,所得固体的质量为
加热还原,所得固体的质量为(4)
 和
和 的燃烧热分别为
的燃烧热分别为 、
、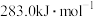 ,已知
,已知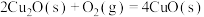
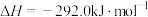 ;则
;则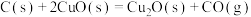 的
的
 。
。(5)某同学利用下图装置进行铁上电镀铜的实验探究。
| 实验序号 | 装置示意图 | 实验现象 |
| 1 | 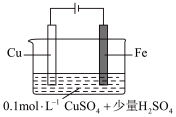 | 阴极表面有无色气体,一段时间后阴极表面有红色固体,气体减少。经检验电解液中有 |
| 2 | 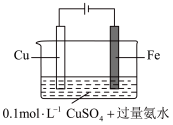 | 阴极表面未观察到气体,一段时间后阴极表面有致密红色固体。经检验电解液中无 元素 元素 |
②实验ⅰ中,推测产生
 ,可能发生的反应有
,可能发生的反应有 、
、③随着阴极析出
 ,实验ⅱ中
,实验ⅱ中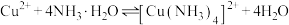 平衡不移动,理由是
平衡不移动,理由是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g);ΔH1=+489.0 kJ·mol-1
C(s)+CO2(g)=2CO(g);ΔH2=+172.5 kJ·mol-1。
则CO还原Fe2O3的热化学方程式为______________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CH3OH的物质的量随时间的变化如图所示,请回答下列问题:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CH3OH的物质的量随时间的变化如图所示,请回答下列问题:
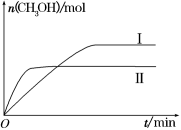
①该反应的平衡常数的表达式为K=_______________ 。
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ_____ KⅡ(填“大于” 、“等于”或“小于”)。
③在下图a、b、c三点中,H2的转化率由高到低的顺序是__________ (填字母)。
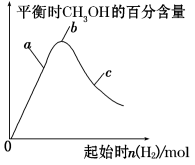
(3)在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是______________ 。
a.氢气的浓度减小
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时n(H2)/n(CH3OH)增大
(4)在恒温恒容条件下,起始加入的反应物不变,要增大CH3OH 的产率,可以采取的有效措施是______________
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g);ΔH1=+489.0 kJ·mol-1
C(s)+CO2(g)=2CO(g);ΔH2=+172.5 kJ·mol-1。
则CO还原Fe2O3的热化学方程式为
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同条件下发生反应:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CH3OH的物质的量随时间的变化如图所示,请回答下列问题:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CH3OH的物质的量随时间的变化如图所示,请回答下列问题:
①该反应的平衡常数的表达式为K=
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ
③在下图a、b、c三点中,H2的转化率由高到低的顺序是

(3)在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是
a.氢气的浓度减小
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时n(H2)/n(CH3OH)增大
(4)在恒温恒容条件下,起始加入的反应物不变,要增大CH3OH 的产率,可以采取的有效措施是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】汽车安全气囊中的填充物有NaN3 (叠氮酸钠)、 、
、 等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
(1)写出N2的电子式:_______ 。
(2)NaN3是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。NaN3晶体中存在的化学键类型是_______ 。
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是_______ (填写化学式),所涉及的5种元素中,原子半径最大的是_______ (填写元素符号)。
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: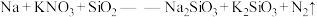 (未配平)。
(未配平)。
(4)写出配平后完整的化学方程式,并用单线桥法标出电子转移的方向和数目_______ 。
(5)结合金属钠的化学性质,说明汽车安全气囊中填充 、
、 的目的
的目的_______ 。
(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是_______ 。
 、
、 等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:(1)写出N2的电子式:
(2)NaN3是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。NaN3晶体中存在的化学键类型是
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: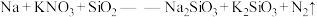 (未配平)。
(未配平)。(4)写出配平后完整的化学方程式,并用单线桥法标出电子转移的方向和数目
(5)结合金属钠的化学性质,说明汽车安全气囊中填充
 、
、 的目的
的目的(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】已知氯化铝的熔点为190℃(2.02×105Pa),但它在180℃即开始升华。
(1)氯化铝是________________ (填“离子化合物”或“共价化合物”)。
(2)在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g·L-1,且已知它的结构中有配位键,氯化铝的化学式为________ ,结构式为________ 。
(3)无水氯化铝在空气中强烈地“发烟”,其原因是______________________ 。
(4)设计一个更可靠的实验,判别氯化铝是离子化合物还是共价化合物。你设计的实验是________________ 。
(1)氯化铝是
(2)在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g·L-1,且已知它的结构中有配位键,氯化铝的化学式为
(3)无水氯化铝在空气中强烈地“发烟”,其原因是
(4)设计一个更可靠的实验,判别氯化铝是离子化合物还是共价化合物。你设计的实验是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)X原子有两个电子层,它能与最活泼的金属Y形成 的化合物,X是
的化合物,X是_______ 元素(写元素符号)。
(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是_______ 元素(写元素符号),n=_______ 。
(3)下表是元素周期表的一部分,回答有关问题:
①在这些元素中,最不活泼的元素的结构示意图是______________
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为___________ ;碱性最强的与呈两性的发生反应的离子方程式__________
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有___________
④用电子式表示由元素(8)和(10)形成化合物的过程:_________________
 的化合物,X是
的化合物,X是(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是
(3)下表是元素周期表的一部分,回答有关问题:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
①在这些元素中,最不活泼的元素的结构示意图是
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有
④用电子式表示由元素(8)和(10)形成化合物的过程:
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】锡是一种银白色金属,在生产、生活中有着重要的用途,在化合物中主要呈现+2和+4价。
(l)我国云南个旧锡矿闻名于世,其主要成分为SnO2。用焦炭作还原剂,在高温下用该矿石可制得粗锡,该反应的化学方程式为___________ 。
(2)马口铁是在铁皮表面镀一层金属锡。马口铁破损后,负极上的电极反应是_______ 。
(3)锡的氯化物有SnCl2和SnCl4。SnCl2是生产和化学实验中常用的还原剂,易发生水解;SnCl4常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃。
① 若实验室中以SnCl2固体配制SnCl2溶液,试简述操作方法________ 。
②SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为_______ 。
(4)Sn(OH)2具有明显的两性,在碱性条件下以Sn(OH)3的形式存在。写出Sn(OH)2发生酸式电离的电离方程式____________ 。
(5)SnS2是黄色固体,俗称“金粉”,将H2S通入SnCl4溶液中可得SnS2沉淀,写出该反应的离子方程式__________ 。
(6)某同学对微电子器件生产的锡粉设计如下方法进行纯度测定:① 取试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;② 加入过量的Fe2(SO4)3溶液;③ 用0.10mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价);④ 根据数据计算出锡粉的纯度。步骤② 中加入Fe2(SO4)3的作用是_______ ;用离子方程式表示K2Cr2O7溶液进行滴定实验的原理__________ 。
(l)我国云南个旧锡矿闻名于世,其主要成分为SnO2。用焦炭作还原剂,在高温下用该矿石可制得粗锡,该反应的化学方程式为
(2)马口铁是在铁皮表面镀一层金属锡。马口铁破损后,负极上的电极反应是
(3)锡的氯化物有SnCl2和SnCl4。SnCl2是生产和化学实验中常用的还原剂,易发生水解;SnCl4常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃。
① 若实验室中以SnCl2固体配制SnCl2溶液,试简述操作方法
②SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为
(4)Sn(OH)2具有明显的两性,在碱性条件下以Sn(OH)3的形式存在。写出Sn(OH)2发生酸式电离的电离方程式
(5)SnS2是黄色固体,俗称“金粉”,将H2S通入SnCl4溶液中可得SnS2沉淀,写出该反应的离子方程式
(6)某同学对微电子器件生产的锡粉设计如下方法进行纯度测定:① 取试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;② 加入过量的Fe2(SO4)3溶液;③ 用0.10mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价);④ 根据数据计算出锡粉的纯度。步骤② 中加入Fe2(SO4)3的作用是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:
(1)写出 在周期表中的位置
在周期表中的位置___________ 。
(2)将 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为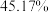 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式___________ (已知:固体残留率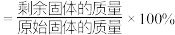 )。
)。
(3)将固体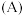 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比___________ 。
(4)该正极材料充电一段时间后变为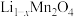 ,为测定
,为测定 的值。称取
的值。称取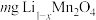 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为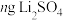 ,写出
,写出 的表达式
的表达式___________ 。
 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:(1)写出
 在周期表中的位置
在周期表中的位置(2)将
 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为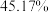 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式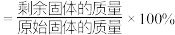 )。
)。(3)将固体
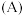 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比(4)该正极材料充电一段时间后变为
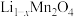 ,为测定
,为测定 的值。称取
的值。称取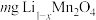 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为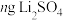 ,写出
,写出 的表达式
的表达式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】工业废水中的氨氮(以 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。
(1)微生物法:酸性废水中的部分 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。
① 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
② 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为_______ 。
(2)次氯酸钠氧化法:向氨氮废水中加入 ,氨氮转化为
,氨氮转化为 而除去。
而除去。
① 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
②一定 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。 :
: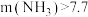 时,总氮的去除率随
时,总氮的去除率随 :
: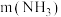 的增大不升反降的原因是
的增大不升反降的原因是_______ 。
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,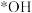 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。_______ 。
②其它条件不变调节废水的 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是_______ 。 晶体进行纯度测定:
晶体进行纯度测定:
a.称取 样品,将其配成
样品,将其配成 溶液。
溶液。
b.先向锥形瓶内加入一定浓度的 溶液,加热至
溶液,加热至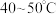 。冷却后再向其中加入
。冷却后再向其中加入
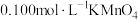 溶液,充分混合。
溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液 。
。
(NaNO2与 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)
通过计算,该样品中 的质量分数是
的质量分数是_______ 。(写出计算过程)
 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。(1)微生物法:酸性废水中的部分
 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。①
 转化为
转化为 的离子方程式为
的离子方程式为②
 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为(2)次氯酸钠氧化法:向氨氮废水中加入
 ,氨氮转化为
,氨氮转化为 而除去。
而除去。①
 氧化
氧化 的离子方程式为
的离子方程式为②一定
 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。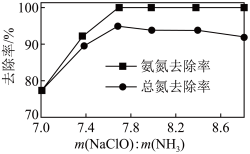
 :
: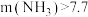 时,总氮的去除率随
时,总氮的去除率随 :
: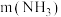 的增大不升反降的原因是
的增大不升反降的原因是(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,
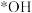 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。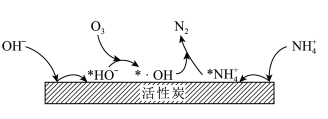
②其它条件不变调节废水的
 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是
 晶体进行纯度测定:
晶体进行纯度测定:a.称取
 样品,将其配成
样品,将其配成 溶液。
溶液。b.先向锥形瓶内加入一定浓度的
 溶液,加热至
溶液,加热至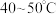 。冷却后再向其中加入
。冷却后再向其中加入
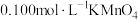 溶液,充分混合。
溶液,充分混合。c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液
 。
。(NaNO2与
 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)通过计算,该样品中
 的质量分数是
的质量分数是
您最近一年使用:0次



