向盛有300mLNaHCO3和Na2CO3混合溶液的烧杯中逐滴加入0.40mol·L-1的Ba(OH)2溶液,加入500mL恰好完全反应,溶液中c(OH-)为0.35mol·L-1。请回答:(忽略溶液混合时体积的变化)
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=___________ 。
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=___________ 。
(1)当NaHCO3溶液完全转化为BaCO3时,消耗Ba(OH)2溶液的体积V=
(2)原混合溶液中n(NaHCO3):n(Na2CO3)=
更新时间:2021-11-25 21:13:10
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】取四份不同质量的(NH4)2SO4和NH4HSO4的混合物样品,分别加入到200mL1 mol/L的NaOH溶液中,充分反应,加热,再将逸出气体干燥后用浓H2SO4吸收,测定结果如下表:
回答下列问题:
(1)分析上表中的数据,求m的值。
(2)在研究时发现,浓硫酸增加的质量(g)与样品的质量(g)之间满足一定的函数关系。假设样品的质量为x,浓硫酸增加的质量为y,写出当x在不同范围时y与x的函数关系。
| 实验编号 | I | II | III | IV |
| 样品的质量(g) | 9.88 | 19.76 | 29.64 | 49.40 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
(1)分析上表中的数据,求m的值。
(2)在研究时发现,浓硫酸增加的质量(g)与样品的质量(g)之间满足一定的函数关系。假设样品的质量为x,浓硫酸增加的质量为y,写出当x在不同范围时y与x的函数关系。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】次氯酸钾,是一种强氧化剂,极易溶于冷水,遇热水则分解。主要用作氧化剂、漂白剂、消毒剂、杀菌剂。已知氯气与 反应放热,反应温度较高时有副反应发生。
反应放热,反应温度较高时有副反应发生。
Ⅰ.配制

 溶液
溶液
(1)配制溶液时,必须用到的玻璃仪器有烧杯、胶头滴管、_______ 。需要称量氢氧化钾的质量为:_______ g。
Ⅱ.制备

(2)盛放浓盐酸的仪器名称是_______ ,A中发生反应的化学方程式为_______ 。
(3)B中盛放的试剂是_______ ,D中反应的离子方程式为_______ 。
(4)根据题给信息,分析该实验装置中存在的不足并提出改进措施:_______ 。
(5)加热

 溶液和
溶液和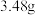
 粉末的混合物,若反应充分进行,则理论上可产生的
粉末的混合物,若反应充分进行,则理论上可产生的 在标准状况下的体积为
在标准状况下的体积为_______  。
。
 反应放热,反应温度较高时有副反应发生。
反应放热,反应温度较高时有副反应发生。Ⅰ.配制


 溶液
溶液(1)配制溶液时,必须用到的玻璃仪器有烧杯、胶头滴管、
Ⅱ.制备


(2)盛放浓盐酸的仪器名称是
(3)B中盛放的试剂是
(4)根据题给信息,分析该实验装置中存在的不足并提出改进措施:
(5)加热


 溶液和
溶液和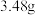
 粉末的混合物,若反应充分进行,则理论上可产生的
粉末的混合物,若反应充分进行,则理论上可产生的 在标准状况下的体积为
在标准状况下的体积为 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】钛是继铁、铝后的第三金属,二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.用钛铁矿制取二氧化钛,(钛铁矿主要成分为FeTiO3,其中Ti元素化合价为+4价,含有Fe2O3杂质。)主要流程如下:
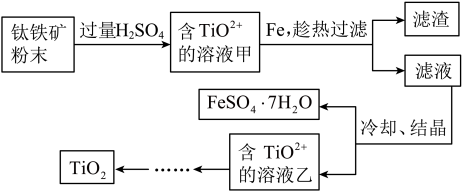
(1)Fe2O3与H2SO4反应的离子方程式_________________ 。
(2)加Fe的作用是______________________ 。
Ⅱ.由金红石(含TiO2大于96%)为原料生产钛的流程如下:

(3)反应②的方程式是____________ ,该反应需要在Ar气氛中进行的原因是________ 。
Ⅲ.科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。
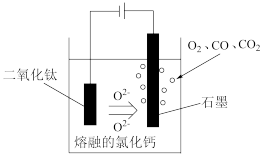
(4)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氧化钙,原理如右图所示 该方法阴极获得钛的电极反应为___________________ 。
(5)阳极产生的CO2经常用氢氧化钠溶液来吸收,现有0.4mol CO2用200ml 3mol/L的NaOH溶液将其完全吸收,溶液中的离子浓度由大到小的顺序为_______________ 。
Ⅰ.用钛铁矿制取二氧化钛,(钛铁矿主要成分为FeTiO3,其中Ti元素化合价为+4价,含有Fe2O3杂质。)主要流程如下:

(1)Fe2O3与H2SO4反应的离子方程式
(2)加Fe的作用是
Ⅱ.由金红石(含TiO2大于96%)为原料生产钛的流程如下:

(3)反应②的方程式是
Ⅲ.科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。
(4)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氧化钙,原理如右图所示 该方法阴极获得钛的电极反应为

(5)阳极产生的CO2经常用氢氧化钠溶液来吸收,现有0.4mol CO2用200ml 3mol/L的NaOH溶液将其完全吸收,溶液中的离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:_____ ,若是改加氢氧化钡溶液至中性,离子反应方程式为:______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:__ 。
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:____ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为___ 。
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为____ 。
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】Ⅰ.煤炭中以FeS2形式存在的硫,在有水和空气及在脱硫微生物存在下发生生物氧化还原反应,有关反应的离子方程式依次为:
①2FeS2+7O2+2H2O 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;
②Fe2++O2+H+ Fe3++________;
Fe3++________;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2SO
4H++2SO 。
。
已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整_______ 。
(2)反应③的还原剂是__________________ 。
(3)观察上述反应,硫元素最终转化为____________ 从煤炭中分离出来。
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是____________________________ 。在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是_______________________ 。(提示:碘元素被氧化成IO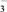 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO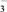 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是________________ 。
Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是________ (填元素符号)。当生成0.8 mol 铜时,此反应转移的电子数目是________ 。
①2FeS2+7O2+2H2O
 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;②Fe2++O2+H+
 Fe3++________;
Fe3++________;③FeS2+2Fe3+
 3Fe2++2S;
3Fe2++2S;④2S+3O2+2H2O
 4H++2SO
4H++2SO 。
。已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整
(2)反应③的还原剂是
(3)观察上述反应,硫元素最终转化为
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是
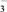 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO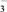 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再产生CO2气体为止,在此过程中,溶液中的碳酸氢根离子浓度的变化是___ 。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为___ 。
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有___ 种。若固体混合物A的质量m(A)为定值,生成气体的量为定值,则A的可能组成是(填写化学式):___ 、___ ;___ 、___ 。(可以不填满)
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是___ mol。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。

(1)A-B段的离子反应方程式为__________________________ 。
(2)原NaOH溶液的浓度为__________ mol/L。
(3)通入CO2在标准状况下的体积为_______ mL。
(4)所得溶液的溶质成分是_______________ ,其物质的量之比为_________ 。

(1)A-B段的离子反应方程式为
(2)原NaOH溶液的浓度为
(3)通入CO2在标准状况下的体积为
(4)所得溶液的溶质成分是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】许多钠的化合物的水溶液呈碱性,这些化合物之间往往可以相互转化。
(1)写出 的电子式
的电子式___________ ; 所含化学键的类型有
所含化学键的类型有___________ (填写下列字母)。
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2) 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
___________  (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
(3)该固体样品应在___________ (填仪器名称)中加热至恒重。该过程主要发生的化学方程式为___________ 。
(4)对某一样品做四组平行实验,数据结果如下:
则该样品中 质量分数为
质量分数为___________ (表示成百分数,精确到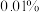 )。
)。
(5)若 质量分数标准值为
质量分数标准值为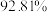 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有___________ (填写下列字母)
a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
(1)写出
 的电子式
的电子式 所含化学键的类型有
所含化学键的类型有a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(2)
 金属钠完全氧化为
金属钠完全氧化为 的焓变为
的焓变为 ,而完全氧化为
,而完全氧化为 的焓变为
的焓变为 ,则
,则
 (填“>”、“<”或“=”)。如果以
(填“>”、“<”或“=”)。如果以 为原料制备
为原料制备 固体,样品往往混有一定量的
固体,样品往往混有一定量的 。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。
。可以通过测定固体样品加热前后的质量差来测定该样品的纯度。(3)该固体样品应在
(4)对某一样品做四组平行实验,数据结果如下:
| 所测物理量 | 第一组 | 第二组 | 第三组 | 第四组 |
| 容器质量/g | 17.221 | 18.565 | 18.652 | 17.094 |
| 加热前容器与样品质量/g | 24.864 | 26.800 | 26.935 | 24.338 |
| 恒重后容器与样品质量/g | 22.209 | 23.936 | 23.992 | 21.823 |
 质量分数为
质量分数为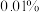 )。
)。(5)若
 质量分数标准值为
质量分数标准值为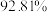 ,则上述实验中可能存在的问题有
,则上述实验中可能存在的问题有a.盛放样品的容器有受热分解杂质 b.盛放样品的容器有热稳定杂质
c.加热前洗净的容器未完全干燥 d.样品在加热后冷却时未放置于干燥器
e.加热时有样品溅出 f.固体样品未充分受热,反应进行不完全
您最近一年使用:0次




