1 . 硫酸的消费量常用来衡量一个国家工业发展水平,其中 的催化氧化是重要的一步。
的催化氧化是重要的一步。
I.科研人员使用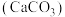 为基础固硫材料,复合不同的催化剂(
为基础固硫材料,复合不同的催化剂(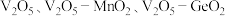 )催化
)催化 向
向 的转化,同时研究了不同温度下使用三种催化剂对
的转化,同时研究了不同温度下使用三种催化剂对 固硫效率(用单位时间
固硫效率(用单位时间 转化率表示)的影响如下图:
转化率表示)的影响如下图:
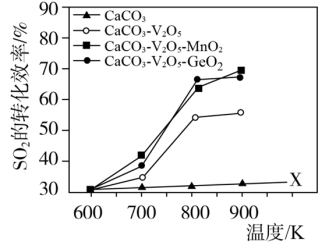
(1)仅使用 而不使用催化剂获得X线的实验目的是
而不使用催化剂获得X线的实验目的是_______ ﹔
(2)下列有关说法正确的是_______
a.三种催化剂中 催化剂效率最低
催化剂效率最低
b.同温同压下,使用复合催化剂有利于提高 的平衡产率
的平衡产率
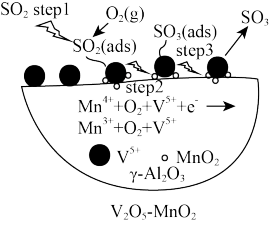
c.如上图为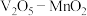 为催化剂时的反应机理,由图可知
为催化剂时的反应机理,由图可知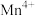 比
比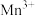 更易获得电子
更易获得电子
d.温度越高一定越有利于催化剂催化效率的提升
(3)某 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: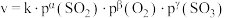 ,根据表中数据可得:
,根据表中数据可得:
_______ 、
_______ 、
_______ 。
Ⅱ.在恒温恒压下,向密闭容器中充入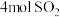 和
和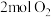 混合气体,
混合气体, 后,反应达到平衡,生成
后,反应达到平衡,生成 气体
气体 ,同时放出热量
,同时放出热量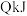 。请回答下列问题:
。请回答下列问题:
(4)该反应的热化学方程式为_______ 。
(5)在该条件下,反应前后容器的体积之比为_______ 。
(6)若把“恒温恒压”改为“恒压绝热条件”反应,平衡后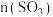
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 的催化氧化是重要的一步。
的催化氧化是重要的一步。I.科研人员使用
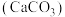 为基础固硫材料,复合不同的催化剂(
为基础固硫材料,复合不同的催化剂(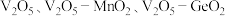 )催化
)催化 向
向 的转化,同时研究了不同温度下使用三种催化剂对
的转化,同时研究了不同温度下使用三种催化剂对 固硫效率(用单位时间
固硫效率(用单位时间 转化率表示)的影响如下图:
转化率表示)的影响如下图:
(1)仅使用
 而不使用催化剂获得X线的实验目的是
而不使用催化剂获得X线的实验目的是(2)下列有关说法正确的是

a.三种催化剂中
 催化剂效率最低
催化剂效率最低b.同温同压下,使用复合催化剂有利于提高
 的平衡产率
的平衡产率c.如上图为
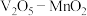 为催化剂时的反应机理,由图可知
为催化剂时的反应机理,由图可知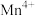 比
比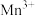 更易获得电子
更易获得电子d.温度越高一定越有利于催化剂催化效率的提升
(3)某
 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: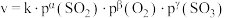 ,根据表中数据可得:
,根据表中数据可得:


| 实验 | 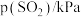 | 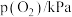 | 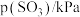 | 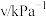 |
| 1 | m | n | p | q |
| 2 | 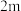 | n | p |  |
| 3 | m | n |  | 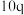 |
| 4 | m |  | p | 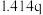 |
Ⅱ.在恒温恒压下,向密闭容器中充入
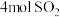 和
和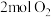 混合气体,
混合气体, 后,反应达到平衡,生成
后,反应达到平衡,生成 气体
气体 ,同时放出热量
,同时放出热量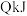 。请回答下列问题:
。请回答下列问题:(4)该反应的热化学方程式为
(5)在该条件下,反应前后容器的体积之比为
(6)若把“恒温恒压”改为“恒压绝热条件”反应,平衡后
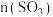
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2022-11-14更新
|
235次组卷
|
4卷引用:青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题
2 . 室温下,向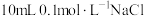 溶液和
溶液和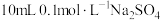 溶液中分别滴加
溶液中分别滴加 的
的 溶液,
溶液, [
[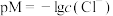 或
或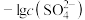 ]与
]与 溶液体积的关系如图所示。下列说法错误的是
溶液体积的关系如图所示。下列说法错误的是

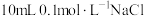 溶液和
溶液和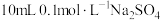 溶液中分别滴加
溶液中分别滴加 的
的 溶液,
溶液, [
[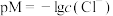 或
或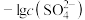 ]与
]与 溶液体积的关系如图所示。下列说法错误的是
溶液体积的关系如图所示。下列说法错误的是
A.室温下,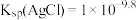 |
B.A、C、D点对应溶液中,C点对应的 最大 最大 |
C.若用 的 的 溶液滴定,则A点向B点移动 溶液滴定,则A点向B点移动 |
D.室温下,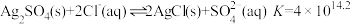 |
您最近一年使用:0次
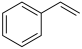
3 . 苯乙烯是合成树脂、离子交换树脂及合成橡胶等的重要单体,常用乙苯为原料合成。
(1)逆水煤气变换耦合反应(二步法):CO2和乙苯为原料制备苯乙烯的机理如下:
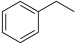 ⇌
⇌
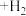
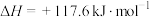
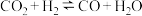
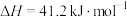
“一步法”: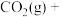
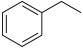

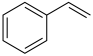
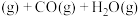 的
的 为
为_______ 。
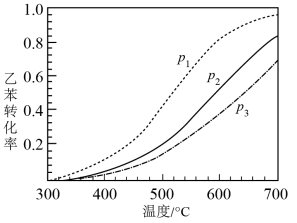
(2)乙苯直接脱氢制苯乙烯,反应原理如下:


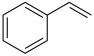
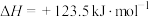
①不同压强下,实验测得乙苯的平衡转化率随温度( )的变化关系如图所示,压强(
)的变化关系如图所示,压强( 、
、 、
、 )由大到小的顺序为
)由大到小的顺序为_______ ,理由是_______ 。
②实际过程中,通常向乙苯中掺入水蒸气,保持体系总压为 。乙苯平衡转化率与温度、投料比
。乙苯平衡转化率与温度、投料比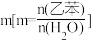 的关系如图。则投料比
的关系如图。则投料比 、
、 、
、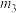 由大到小的顺序为
由大到小的顺序为_______ 。
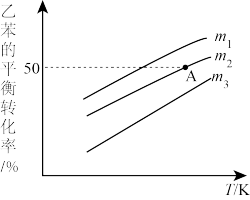
③若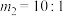 ,则A点温度下,该反应的平衡常数
,则A点温度下,该反应的平衡常数
_______ 。
(3)含苯乙烯的废水肆意排放会对环境造成严重的污染,现采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水, )。已知:∙OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
)。已知:∙OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
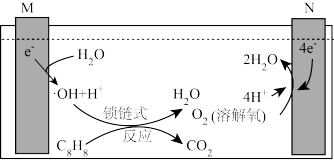
M连接电源的_______ (填“正极”或“负极”),若电路中通过10mol电子,则有_______ g苯乙烯被羟基自由基完全氧化成CO2和H2O。
(1)逆水煤气变换耦合反应(二步法):CO2和乙苯为原料制备苯乙烯的机理如下:
 ⇌
⇌
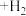
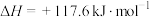
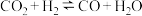
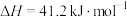
“一步法”:
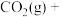



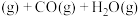 的
的 为
为(2)乙苯直接脱氢制苯乙烯,反应原理如下:



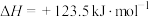
①不同压强下,实验测得乙苯的平衡转化率随温度(
 )的变化关系如图所示,压强(
)的变化关系如图所示,压强( 、
、 、
、 )由大到小的顺序为
)由大到小的顺序为
②实际过程中,通常向乙苯中掺入水蒸气,保持体系总压为
 。乙苯平衡转化率与温度、投料比
。乙苯平衡转化率与温度、投料比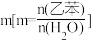 的关系如图。则投料比
的关系如图。则投料比 、
、 、
、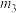 由大到小的顺序为
由大到小的顺序为
③若
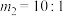 ,则A点温度下,该反应的平衡常数
,则A点温度下,该反应的平衡常数
(3)含苯乙烯的废水肆意排放会对环境造成严重的污染,现采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,
 )。已知:∙OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
)。已知:∙OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
M连接电源的
您最近一年使用:0次
解题方法
4 . 五硫代碳酸钠(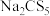 ,
,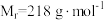 )是一种针状固体,易溶于水和乙醚,溶液呈深黄色,难溶于丙酮,是一种优良的还原剂,工业上常用于重金属废水的处理。实验室用
)是一种针状固体,易溶于水和乙醚,溶液呈深黄色,难溶于丙酮,是一种优良的还原剂,工业上常用于重金属废水的处理。实验室用 、
、 和硫粉在水溶液中制备
和硫粉在水溶液中制备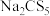 并测定其浓度(加热装置均已略去)。
并测定其浓度(加热装置均已略去)。
已知:① 有毒、易挥发、难溶于水,化学性质与CO2相似;②在非极性溶剂
有毒、易挥发、难溶于水,化学性质与CO2相似;②在非极性溶剂 中,会有副产物
中,会有副产物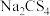 生成,
生成,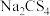 难溶于乙醚。
难溶于乙醚。
实验一:制备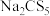

实验步骤:
i.取2g硫粉和2mL离子液体{1-丁基-3-甲基咪唑四氟硼酸盐,简称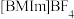 }与
}与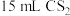 (过量)混合液于
(过量)混合液于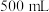 三颈圆底烧瓶中,往a中加入
三颈圆底烧瓶中,往a中加入 。
。
ii.打开仪器a开关,水浴加热三颈烧瓶至40℃,在电磁搅拌器下反应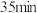 。
。
iii.反应结束后,将溶液转入烧杯中,经进一步操作得到干燥的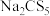 样品。
样品。
(1)仪器a的名称为_______ ;仪器 的作用是
的作用是_______ 。
(2)已知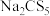 中硫的化合价为-1和-2,1个
中硫的化合价为-1和-2,1个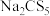 中过硫键(
中过硫键( )的数目为
)的数目为_______ 。
(3)装置c中盛放的药品可以是____ (填字母),写出该物质与 反应的化学方程式:
反应的化学方程式:____ 。
a.无水 b.
b. 固体 c.硅胶
固体 c.硅胶
(4)生成副产物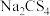 的离子方程式为
的离子方程式为_______ 。
实验二:测定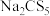 样品纯度
样品纯度
为测定生成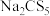 样品的纯度,取干燥后样品3.5g,加水溶解并稀释至
样品的纯度,取干燥后样品3.5g,加水溶解并稀释至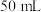 ,每次取出
,每次取出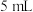 用无色的二硫化二异丙基黄原酸酯(
用无色的二硫化二异丙基黄原酸酯(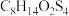 )的乙腈溶液为标准液(
)的乙腈溶液为标准液(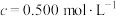 )进行滴定,反应原理为
)进行滴定,反应原理为 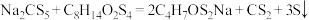 (黄原酸盐为无色),平均消耗
(黄原酸盐为无色),平均消耗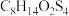 的乙腈标准液体积是
的乙腈标准液体积是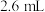 。
。
(5)滴定终点现象是_______ ;样品纯度为_______ (保留小数点后1位)。
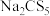 ,
,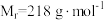 )是一种针状固体,易溶于水和乙醚,溶液呈深黄色,难溶于丙酮,是一种优良的还原剂,工业上常用于重金属废水的处理。实验室用
)是一种针状固体,易溶于水和乙醚,溶液呈深黄色,难溶于丙酮,是一种优良的还原剂,工业上常用于重金属废水的处理。实验室用 、
、 和硫粉在水溶液中制备
和硫粉在水溶液中制备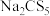 并测定其浓度(加热装置均已略去)。
并测定其浓度(加热装置均已略去)。已知:①
 有毒、易挥发、难溶于水,化学性质与CO2相似;②在非极性溶剂
有毒、易挥发、难溶于水,化学性质与CO2相似;②在非极性溶剂 中,会有副产物
中,会有副产物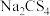 生成,
生成,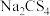 难溶于乙醚。
难溶于乙醚。实验一:制备
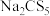

图1
实验步骤:
i.取2g硫粉和2mL离子液体{1-丁基-3-甲基咪唑四氟硼酸盐,简称
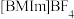 }与
}与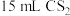 (过量)混合液于
(过量)混合液于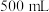 三颈圆底烧瓶中,往a中加入
三颈圆底烧瓶中,往a中加入 。
。ii.打开仪器a开关,水浴加热三颈烧瓶至40℃,在电磁搅拌器下反应
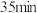 。
。iii.反应结束后,将溶液转入烧杯中,经进一步操作得到干燥的
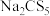 样品。
样品。(1)仪器a的名称为
 的作用是
的作用是(2)已知
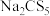 中硫的化合价为-1和-2,1个
中硫的化合价为-1和-2,1个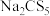 中过硫键(
中过硫键( )的数目为
)的数目为(3)装置c中盛放的药品可以是
 反应的化学方程式:
反应的化学方程式:a.无水
 b.
b. 固体 c.硅胶
固体 c.硅胶(4)生成副产物
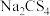 的离子方程式为
的离子方程式为实验二:测定
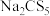 样品纯度
样品纯度为测定生成
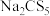 样品的纯度,取干燥后样品3.5g,加水溶解并稀释至
样品的纯度,取干燥后样品3.5g,加水溶解并稀释至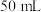 ,每次取出
,每次取出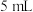 用无色的二硫化二异丙基黄原酸酯(
用无色的二硫化二异丙基黄原酸酯(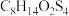 )的乙腈溶液为标准液(
)的乙腈溶液为标准液(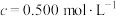 )进行滴定,反应原理为
)进行滴定,反应原理为 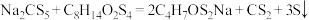 (黄原酸盐为无色),平均消耗
(黄原酸盐为无色),平均消耗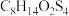 的乙腈标准液体积是
的乙腈标准液体积是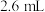 。
。(5)滴定终点现象是
您最近一年使用:0次
5 . 25℃时,已知弱酸H3RO3溶液中含R物种的浓度之和为0.1 mol·L-1,溶液中所有含R物种的lgc-pOH的关系如图所示,下列说法错误的是

已知: pOH表示OH-浓度的负对数[pOH = -lgc(OH- )]。

已知: pOH表示OH-浓度的负对数[pOH = -lgc(OH- )]。
| A.H3RO3 为二元弱酸 |
| B.曲线③表示lgc(H3RO3)随pOH的变化 |
C.pH=6.7 的溶液中: c(H3RO3)+ 2c( )=0.1mol·L-1 )=0.1mol·L-1 |
D.反应H3RO3+   2 2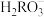 的平衡常数K=1.0 × 105 的平衡常数K=1.0 × 105 |
您最近一年使用:0次
2022-07-13更新
|
1530次组卷
|
11卷引用:青海省海东市2022届高考一模理科综合化学试题
青海省海东市2022届高考一模理科综合化学试题黑龙江省大庆市2021-2022学年高三上学期第二次教学质量检测理科综合化学试题山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题安徽省“皖南八校”2022届高三下学期第三次联考理综化学试题广东省四校(华附,省实,深中,广雅)2021-2022学年高二下学期期末联考化学试题四川省北大成都附属实验学校2021-2022学年高三下学期第四次模拟考试理科综合化学试题河北省保定市部分学校2021-2022学年高三12月联考化学试题河北省邢台市“五岳联盟”部分重点学校2021-2022学年高三12月联考化学试题河南省新乡市2021-2022学年高三上学期第一次模拟考试理综化学试题 山东省济南市历城第二中学2023届高三上学期一轮复习验收考试化学试题江西省吉水中学2023届高三下学期一模考试化学试题
解题方法
6 . 化合物K是一种有机光电材料的中间体。实验室由芳香化合物A制备K的一种合成路线如下:
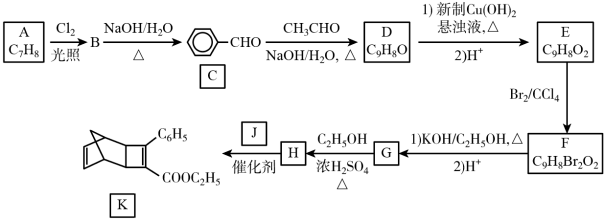
已知:①在一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
②RCHO+CH3CHO RCH=CHCHO+H2O
RCH=CHCHO+H2O
③
回答下列问题:
(1)B的分子式为_______ ;E中官能团的名称为_______
(2)D→E第一步的化学反应方程式为_______ 。
(3)F→G第一步的反应类型为_______ 。
(4)J的结构简式为_______ 。
(5)芳香化合物X是E的同分异构体,X具有以下特点:①只有一个环状结构;②具有两个相同的官能团;③能发生银镜反应,X共有_______ 种(不考虑立体异构)。其中核磁共振氢谱有四种不同化学环境的氢,且峰面积之比为3:2:2:1,写出2种符合要求的X的结构简式_______ 。
(6)根据上述路线中的相关知识,以乙醇为原料设计合成1-丁醇,写出合成路线(要求:反应不超过三步,其它无机试剂任选)_______ 。

已知:①在一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
②RCHO+CH3CHO
 RCH=CHCHO+H2O
RCH=CHCHO+H2O③

回答下列问题:
(1)B的分子式为
(2)D→E第一步的化学反应方程式为
(3)F→G第一步的反应类型为
(4)J的结构简式为
(5)芳香化合物X是E的同分异构体,X具有以下特点:①只有一个环状结构;②具有两个相同的官能团;③能发生银镜反应,X共有
(6)根据上述路线中的相关知识,以乙醇为原料设计合成1-丁醇,写出合成路线(要求:反应不超过三步,其它无机试剂任选)
您最近一年使用:0次
7 . 自2021年美国央行的大量放水,大宗原材料价格猛涨,企业十分重视提高原材料的利用率。某大型企业以工业烧渣(主要含ZnO,还含少量Fe3O4、Al2O3、CuO及SiO2等)为原料制取有机高分子材料的阻燃剂一磷酸锌[Zn3(PO4)2]的工艺流程如图所示。
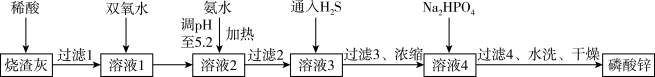
已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
(1)在180 °C对“烧渣灰”进行酸溶最适合的酸是_______ (填“盐酸”、“硫酸”或“硝酸”)。
(2)加入双氧水的作用是作氧化剂,则发生反应的化学方程式为_______ ;可用NaClO代替双氧水,两者相比,_______ (填化学式)的氧化效率更高。(氧化效率以单位质量的氧化剂得到的电子数表示)
(3)加氨水过程中加热的目的是_______ ;“过滤2”得到的滤渣的主要成分为_______ (填化学式)。
(4)通入H2S的目的是_______ ;加入Na2 HPO4发生反应的离子方程式为_______ 。
(5)确认磷酸锌洗涤干净的操作是_______ 。
(6)在通入H2S之前,“溶液3”中A13+的浓度为_______ mol·L-1。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.7 | 2.2 | 5.2 | 6.5 |
| 沉淀完全(c=1.0×10-5mol· L-1)的pH | 4.7 | 3.2 | 6.7 | 8.0 |
(2)加入双氧水的作用是作氧化剂,则发生反应的化学方程式为
(3)加氨水过程中加热的目的是
(4)通入H2S的目的是
(5)确认磷酸锌洗涤干净的操作是
(6)在通入H2S之前,“溶液3”中A13+的浓度为
您最近一年使用:0次
名校
8 . 某温度下,饱和溶液中-lgc(Cl-)、- lgc(I-)与-lgc(Ag+)的关系如图所示。已知同温下,Ksp (AgCl)>Ksp (AgI)。下列说法错误的是
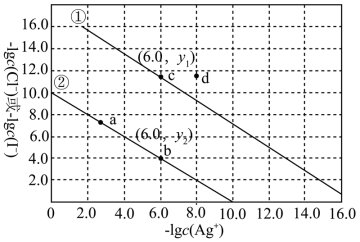
| A.线①代表AgI的沉淀溶解曲线 |
B.c(Ag+)= 10-6 mol·L-1时,两溶液中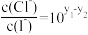 |
| C.加入AgNO3(s)可使溶液由d点变到c点 |
| D.逐渐降低温度,线①平行地移向线② |
您最近一年使用:0次
2022-05-19更新
|
1217次组卷
|
3卷引用:青海省西宁市大通回族土族自治县2022届高三第二次模拟考试理科综合化学试题
青海省西宁市大通回族土族自治县2022届高三第二次模拟考试理科综合化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)浙江省海宁市高级中学2023-2024学年高二下学期3月月考化学试题
9 . 铅蓄电池的拆解、回收和利用可以减少其对环境的污染,具有重要的可持续发展意义。利用废铅蓄电池的铅膏(主要成分为PbSO4、PbO2),还有少重Pb、Fe2O3、Al2O3)制备PbO的流程如图:
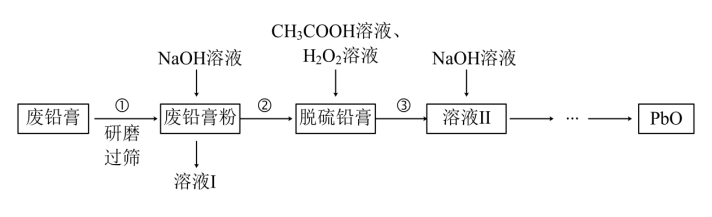
回答下列问题:
(1)步骤①将废铅膏研磨过筛的目的是____ 。
(2)向废铅膏粉中加入NaOH溶液可将PbSO4转化为PbO,反应的离子方程式是____ 。
(3)溶液Ⅰ中主要含有的阴离子有OH-、____ 。
(4)加入CH3COOH溶液和H2O2溶液可将脱硫铅膏中的含铅物质转化为(CH3COO)2Pb。PbO2转化为(CH2COO)2Pb的化学方程式是____ 。
(5)为使Pb2+完全沉淀并获得纯净的PbO,需向溶液Ⅱ中分两次加入NaOH溶液。第一次加入的目的是____ ,过滤后,第二次加入NaOH溶液调节溶液的pH至少为____ (已知:25℃,Ksp[Fe(OH)3]=4×10-38,Ksp[Pb(OH)2]=1×10-16)。
(6)若废铅膏中铅元素的质量分数为69%,用上述流程对1kg废铅膏进行处理,得到669gPbO,则铅的回收率为____ %。

回答下列问题:
(1)步骤①将废铅膏研磨过筛的目的是
(2)向废铅膏粉中加入NaOH溶液可将PbSO4转化为PbO,反应的离子方程式是
(3)溶液Ⅰ中主要含有的阴离子有OH-、
(4)加入CH3COOH溶液和H2O2溶液可将脱硫铅膏中的含铅物质转化为(CH3COO)2Pb。PbO2转化为(CH2COO)2Pb的化学方程式是
(5)为使Pb2+完全沉淀并获得纯净的PbO,需向溶液Ⅱ中分两次加入NaOH溶液。第一次加入的目的是
(6)若废铅膏中铅元素的质量分数为69%,用上述流程对1kg废铅膏进行处理,得到669gPbO,则铅的回收率为
您最近一年使用:0次
10 . 常温下,在含有0.10mol·L-1H3PO3的溶液中含磷元素的微粒pc随pOH的变化关系如图所示已知pc=-lgc,pOH=-lgc(OH-),H3PO3为二元弱酸,下列有关说法中不正确的是


| A.m=10.00 |
| B.曲线③对应的微粒是H3PO3 |
| C.Na2HPO3溶液显碱性 |
D.c点对应的溶液中c(H+)>c(H2PO )+c(OH-)+2c(HPO )+c(OH-)+2c(HPO ) ) |
您最近一年使用:0次
2022-04-02更新
|
444次组卷
|
2卷引用:青海省西宁市2021-2022学年高三高考二模理科综合化学试题



