名校
解题方法
1 . 按要求回答问题。
(1)NaH能与水剧烈反应生成氢气,生成的 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目___________ 。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为___________  ,该样品中含杂质碳
,该样品中含杂质碳___________ g。
(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于___________ g,消耗NaOH溶液的体积是___________ mL。
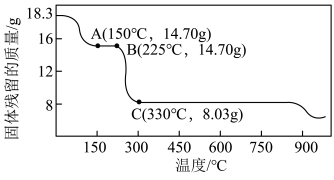
(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴( )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为___________ (填化学式),取C点固体用足量的浓盐酸完全溶解可得到黄绿色气体,写出以上反应的离子反应方程式___________ 。
(1)NaH能与水剧烈反应生成氢气,生成的
 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的
 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为 ,该样品中含杂质碳
,该样品中含杂质碳(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的
 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴(
 )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
您最近一年使用:0次
名校
解题方法
2 . 按要求进行计算。
(1)0.5mol C2H6O的质量是_______ 克,与_______ g H2O分子中的氢的原子数目相同。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量_______ 。
(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为_______ L。
(4)某溶液中仅含有H+、Al3+、Cl-、 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是_______ mol·L-1。
(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为_______ 。
(1)0.5mol C2H6O的质量是
(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为
(4)某溶液中仅含有H+、Al3+、Cl-、
 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为
您最近一年使用:0次
名校
解题方法
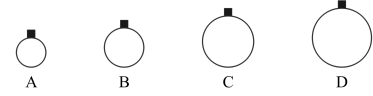
3 . (1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_________ (填选项序号)。
(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为_______ 。
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7mol•L﹣1,c(Zn2+)=0.1mol•L﹣1,c(Cl﹣)=0.3mol•L﹣1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为_________ 。
(4)0.3mol的甲烷与_________ g氨气中所含氢原子数相等。
(5)在同温同压下,2g二氧化碳的体积为120ml,而2gA气体的体积为165ml,则气体A的摩尔质量_________________ ;
(6)标准状况下,11.2L二氧化碳和一氧化碳混合气体的质量为18g,则其中二氧化碳的质量为_________ ,一氧化碳的体积为_________ 。
(7)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100mol•L﹣1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl﹣,则S2O32﹣将转化成____________ 。
A.S2﹣ B.S C.SO32﹣ D.SO42﹣
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移0.6mole﹣,则被氧化的HCl的物质的量为_____________ 。

(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7mol•L﹣1,c(Zn2+)=0.1mol•L﹣1,c(Cl﹣)=0.3mol•L﹣1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为
(4)0.3mol的甲烷与
(5)在同温同压下,2g二氧化碳的体积为120ml,而2gA气体的体积为165ml,则气体A的摩尔质量
(6)标准状况下,11.2L二氧化碳和一氧化碳混合气体的质量为18g,则其中二氧化碳的质量为
(7)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100mol•L﹣1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl﹣,则S2O32﹣将转化成
A.S2﹣ B.S C.SO32﹣ D.SO42﹣
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移0.6mole﹣,则被氧化的HCl的物质的量为
您最近一年使用:0次
名校
4 . 标准状况下,容积为VmL的烧瓶充满NH3,设NA为阿伏加 德罗常数的值。
(1)集满空气时,该烧瓶总质量为a g,则集满NH3时该烧瓶总质量为____________
(2)烧瓶中气体原子的总数是______________
(3)已知NH3的密度比空气小,极易溶于水,氨溶于水形成的溶液称为氨水。用烧瓶中的NH3做喷泉实验,水充满烧瓶,所得溶液的密度为ρg/mL,假设NH3没有损失,该溶液中溶质的质量分数为______ ,物质的量浓度为_______ mol/l
(1)集满空气时,该烧瓶总质量为a g,则集满NH3时该烧瓶总质量为
(2)烧瓶中气体原子的总数是
(3)已知NH3的密度比空气小,极易溶于水,氨溶于水形成的溶液称为氨水。用烧瓶中的NH3做喷泉实验,水充满烧瓶,所得溶液的密度为ρg/mL,假设NH3没有损失,该溶液中溶质的质量分数为
您最近一年使用:0次
2019-10-16更新
|
419次组卷
|
3卷引用:宁夏石嘴山市第三中学2019-2020学年高一10月月考化学试题
名校
5 . 硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18g某种硬铝恰好与10mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448mL氧气(标准状况)混合,恰好能被水完全吸收。
① 计算该硝酸的物质的量浓度。
② 计算并确定此种硬铝的化学式。
① 计算该硝酸的物质的量浓度。
② 计算并确定此种硬铝的化学式。
您最近一年使用:0次
名校
6 . 现有0.270kg质量分数为10%的CuCl2,计算:
(1)溶液中CuCl2的物质的量;
(2)溶液中Cu2+和Cl-的物质的量;
(3)若溶液的密度为1.35g/cm3,计算该溶液中溶质的物质的量浓度。
(1)溶液中CuCl2的物质的量;
(2)溶液中Cu2+和Cl-的物质的量;
(3)若溶液的密度为1.35g/cm3,计算该溶液中溶质的物质的量浓度。
您最近一年使用:0次
名校
7 . 有关物质的量的计算是中学化学的重要内容,完成以下填空:
(1)0.5 mol CH4的质量是_______ g,在标准状况下的体积为________ L;含有_____ mol电子。
(2)相同物质的量的SO2和SO3,质量之比为_________ 所含O的物质的量之比为_______ 。
(3)用58.5g无水氯化钠配制成1 L溶液,其物质的量浓度为______ mol/L;若从中取出500 mL,其物质的量浓度为________ mol/L;
(4) 标准状况下,33.6 L的HCl气体所具有的物质的量为_____________ ,将其溶解于水配成3 L的溶液,所得盐酸的物质的量浓度为__________ 。
(5)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为________ mL。
(1)0.5 mol CH4的质量是
(2)相同物质的量的SO2和SO3,质量之比为
(3)用58.5g无水氯化钠配制成1 L溶液,其物质的量浓度为
(4) 标准状况下,33.6 L的HCl气体所具有的物质的量为
(5)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为
您最近一年使用:0次
名校
8 . 常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答下列问题:
(1)混合溶液pH=8的原因是______________ (用离子方程式表示)
(2)混合溶液中由水电离出的c(OH-)___________ (填“大于”、“等于”或“小于”)0.1mol/LNaOH溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=____________ mol/L, c(OH-)- c(HA)=____________ mol/L
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH_________ 7 (填“大于”、“等于”或“小于”)
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH___________ 7(填“大于”、“等于”或“小于”)。
(1)混合溶液pH=8的原因是
(2)混合溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH
您最近一年使用:0次
2017-03-06更新
|
967次组卷
|
2卷引用:宁夏青铜峡市高级中学2019-2020学年高二上学期期中考试化学试题
解题方法
9 . 有机物A是烃的含氧衍生物,在同温同压下,A蒸气与乙醇蒸气的相对密度是2。1.38g A完全燃烧后,若将燃烧的产物通过碱石灰,碱石灰的质量会增加3.06g;若将燃烧产物通过浓硫酸,浓硫酸的质量会增加1.08g;通过计算确定A的分子式(写出必要的文字说明、计算过程)
您最近一年使用:0次
11-12高二上·浙江杭州·期末
10 . 有机物A由碳、氢、氧三种元素组成,现取3g A与 4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余),将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g,回答下列问题:
(1)3g A中所含氢原子、碳原子的物质的量各是多少?________
(2)通过计算确定该有机物的分子式。________
(3)已知A能和金属钠发生反应,则写出A可能的结构简式。________
(1)3g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
(3)已知A能和金属钠发生反应,则写出A可能的结构简式。
您最近一年使用:0次
2017-02-17更新
|
391次组卷
|
3卷引用:2016-2017学年宁夏石嘴山三中高二上期中化学卷



