名校
解题方法
1 . 为测定某铝镁铜合金中铝、镁的质量分数,进行如下实验(忽略反应中水的蒸发):①向30.0g合金粉末中加入200g 30.0% NaOH溶液,充分反应后,称得固液混合物质量为227.0g。②再向混合液中加入过量稀硫酸,充分反应后剩余固体洗涤干燥后称得质量为0.6g。(计算结果保留一位小数)
(1)查得室温下30.0% NaOH溶液密度为1.33g/mL,则该NaOH溶液的物质的量浓度为___________ mol/L。
(2)30.0g合金中Al的质量为___________ g。
(3)合金中Mg元素的质量分数为___________ 。
(1)查得室温下30.0% NaOH溶液密度为1.33g/mL,则该NaOH溶液的物质的量浓度为
(2)30.0g合金中Al的质量为
(3)合金中Mg元素的质量分数为
您最近一年使用:0次
2 .  可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):
Ⅰ.取0.68000 g 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。
Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为___________ mol。
(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为___________ mol。
(3)产品中硫化氢的质量分数为___________ 。
 可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):Ⅰ.取0.68000 g
 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L
 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为
(3)产品中硫化氢的质量分数为
您最近一年使用:0次
名校
3 . 聚合氯化铝的化学式为 ,其中的铝含量可使用
,其中的铝含量可使用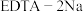 (化学式可简写为
(化学式可简写为 )标准溶液与锌(
)标准溶液与锌( )标准溶液测定,测定过程涉及到的化学方程式为:
)标准溶液测定,测定过程涉及到的化学方程式为: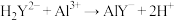 ;
; 。取11.58g某聚合氯化铝样品完全溶于160
。取11.58g某聚合氯化铝样品完全溶于160 5.0
5.0 盐酸后将溶液分为两等份:其中一份稀释到100
盐酸后将溶液分为两等份:其中一份稀释到100 后取10
后取10 溶液移入锥形瓶中,加入80
溶液移入锥形瓶中,加入80 0.10
0.10
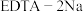 标准溶液,充分反应后剩余的
标准溶液,充分反应后剩余的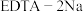 恰好与10
恰好与10 0.20
0.20 锌标准溶液反应;另一份加入足量硝酸酸化的
锌标准溶液反应;另一份加入足量硝酸酸化的 溶液,过滤、洗涤、干燥后得到0.46
溶液,过滤、洗涤、干燥后得到0.46
 固体。
固体。
(1)该聚合氯化铝样品中含Al元素的物质的量为_______ mol。
(2)该聚合氯化铝样品的化学式中a:b=_______ 。
 ,其中的铝含量可使用
,其中的铝含量可使用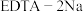 (化学式可简写为
(化学式可简写为 )标准溶液与锌(
)标准溶液与锌( )标准溶液测定,测定过程涉及到的化学方程式为:
)标准溶液测定,测定过程涉及到的化学方程式为: ;
; 。取11.58g某聚合氯化铝样品完全溶于160
。取11.58g某聚合氯化铝样品完全溶于160 5.0
5.0 盐酸后将溶液分为两等份:其中一份稀释到100
盐酸后将溶液分为两等份:其中一份稀释到100 后取10
后取10 溶液移入锥形瓶中,加入80
溶液移入锥形瓶中,加入80 0.10
0.10
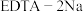 标准溶液,充分反应后剩余的
标准溶液,充分反应后剩余的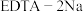 恰好与10
恰好与10 0.20
0.20 锌标准溶液反应;另一份加入足量硝酸酸化的
锌标准溶液反应;另一份加入足量硝酸酸化的 溶液,过滤、洗涤、干燥后得到0.46
溶液,过滤、洗涤、干燥后得到0.46
 固体。
固体。(1)该聚合氯化铝样品中含Al元素的物质的量为
(2)该聚合氯化铝样品的化学式中a:b=
您最近一年使用:0次
名校
解题方法
4 . 把1L 1.0mol/L 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
(1)溶液混合前 的物质的量是
的物质的量是___________ mol。
(2)反应后 的物质的量浓度是
的物质的量浓度是___________ mol/L。
(3)反应中消耗铁粉的质量是___________ g。
 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:(1)溶液混合前
 的物质的量是
的物质的量是(2)反应后
 的物质的量浓度是
的物质的量浓度是(3)反应中消耗铁粉的质量是
您最近一年使用:0次
解题方法
5 . 现有一份部分被氧化的铜片(氧化产物为CuO),称取4.32g铜片,溶于一定体积1.00mol•L-1稀硝酸中,反应恰好完全进行,收集到无色气体448mL(已折算为标准状况)。
(1)该稀硝酸中所含HNO3的物质的量为___________ ;
(2)该铜片被氧化的百分数为___________ 。
(1)该稀硝酸中所含HNO3的物质的量为
(2)该铜片被氧化的百分数为
您最近一年使用:0次
名校
解题方法
6 .  在不同温度下失水和分解,随着温度升高分别生成
在不同温度下失水和分解,随着温度升高分别生成 ,现称取10.000g
,现称取10.000g 在敞口容器加热一定时间后,气体全部逸出,冷却后得到含两种成分的固体共2.720g,测得生成的
在敞口容器加热一定时间后,气体全部逸出,冷却后得到含两种成分的固体共2.720g,测得生成的 的体积为0.448L(已折算为标准标况),求:
的体积为0.448L(已折算为标准标况),求:
(1)固体的成分______ ,其物质的量之比______ 。
(2)标准状况下生成 的体积
的体积______ 。
 在不同温度下失水和分解,随着温度升高分别生成
在不同温度下失水和分解,随着温度升高分别生成 ,现称取10.000g
,现称取10.000g 在敞口容器加热一定时间后,气体全部逸出,冷却后得到含两种成分的固体共2.720g,测得生成的
在敞口容器加热一定时间后,气体全部逸出,冷却后得到含两种成分的固体共2.720g,测得生成的 的体积为0.448L(已折算为标准标况),求:
的体积为0.448L(已折算为标准标况),求:(1)固体的成分
(2)标准状况下生成
 的体积
的体积
您最近一年使用:0次
7 . 某 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
(1)样品中物质的量之比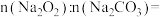
___________ 。
(2)盐酸的物质的量浓度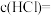
___________ 。
 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积/mL | 100.0 | 100.0 | 100.0 | 100.0 |
| 样品质量/g | 2.62 | 3.93 | 5.24 | 6.55 |
| 气体总体积/mL | 448 | 560 | 448 | 560 |
(1)样品中物质的量之比
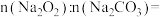
(2)盐酸的物质的量浓度
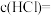
您最近一年使用:0次
8 . 在100mL稀盐酸中加入混合均匀的 和
和 固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生
固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生 (该状况下,气体的密度为
(该状况下,气体的密度为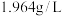 )体积的关系。请计算:
)体积的关系。请计算:
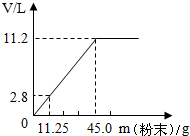
(1)该盐酸中HCl的质量为___________ 。
(2)若该盐酸为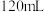 时,加入粉末为
时,加入粉末为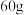 ,产生
,产生 的体积为
的体积为___________ 。
(3)若粉末的质量为 ,该盐酸的体积为
,该盐酸的体积为 ,产生的
,产生的 体积为
体积为 。试写出粉末质量
。试写出粉末质量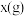 与产生
与产生 体积
体积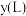 之间的关系:
之间的关系:___________ 。
 和
和 固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生
固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生 (该状况下,气体的密度为
(该状况下,气体的密度为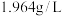 )体积的关系。请计算:
)体积的关系。请计算:
(1)该盐酸中HCl的质量为
(2)若该盐酸为
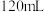 时,加入粉末为
时,加入粉末为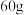 ,产生
,产生 的体积为
的体积为(3)若粉末的质量为
 ,该盐酸的体积为
,该盐酸的体积为 ,产生的
,产生的 体积为
体积为 。试写出粉末质量
。试写出粉末质量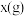 与产生
与产生 体积
体积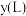 之间的关系:
之间的关系:
您最近一年使用:0次
9 . 取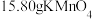 ,加热分解后剩余固体
,加热分解后剩余固体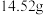 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:
(1)写出 受热分解的化学方程式
受热分解的化学方程式__________ 。
(2) 的分解率
的分解率__________ 。
(3)气体A的物质的量_________ 。
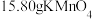 ,加热分解后剩余固体
,加热分解后剩余固体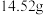 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:(1)写出
 受热分解的化学方程式
受热分解的化学方程式(2)
 的分解率
的分解率(3)气体A的物质的量
您最近一年使用:0次
解题方法
10 . 常温下,将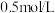 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以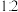 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与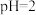 的某一元弱酸溶液
的某一元弱酸溶液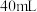 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液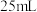 ,试求:
,试求:
(1) 溶液的物质的量浓度为
溶液的物质的量浓度为______  。
。
(2)该一元弱酸的物质的量浓度为______  。
。
(3)此条件下该一元弱酸的电离度为______ 。
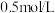 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以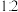 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与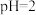 的某一元弱酸溶液
的某一元弱酸溶液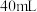 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液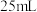 ,试求:
,试求:(1)
 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)该一元弱酸的物质的量浓度为
 。
。(3)此条件下该一元弱酸的电离度为
您最近一年使用:0次



