解题方法
1 . 金属钛用途广泛。从海水中提取Mg和 ,并联合用以钛铁矿(主要含
,并联合用以钛铁矿(主要含 和
和 、
、 、
、 等杂质)为原料冶炼钛单质,其主要工艺流程如下:
等杂质)为原料冶炼钛单质,其主要工艺流程如下: 的形式存在于溶液中,
的形式存在于溶液中, 易水解为偏钛酸
易水解为偏钛酸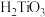 ,
,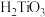 可写作
可写作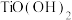 。
。
(1)试剂①通常选煅烧的贝壳粉而不用 的原因是
的原因是_____ 。
(2)试剂②为_____ 。
(3)“沉降分离”出的滤渣成分有_____ 。
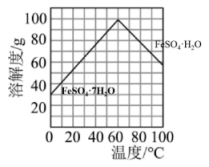
(4)已知绿矾的溶解度随温度变化的曲线如图所示,从溶液Ⅰ获得绿矾的操作方法为_____ 、_____ ,过滤、洗涤、干燥。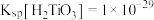 ,若要让
,若要让 水解完全(离子浓度小于
水解完全(离子浓度小于 ),应控制
),应控制 不低于
不低于_____ 。
(6)反应①除生成 外还生成一种可燃性气体,该反应的化学方程式为
外还生成一种可燃性气体,该反应的化学方程式为_____ ,“高温氯化”反应理论计算结果显示,在200℃条件下达到平衡时, 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于200℃,其原因是
,但实际生产中反应温度却远高于200℃,其原因是_____ (写一种)。
(7)该工艺流程中可以循环使用的物质有_____ 。
 ,并联合用以钛铁矿(主要含
,并联合用以钛铁矿(主要含 和
和 、
、 、
、 等杂质)为原料冶炼钛单质,其主要工艺流程如下:
等杂质)为原料冶炼钛单质,其主要工艺流程如下: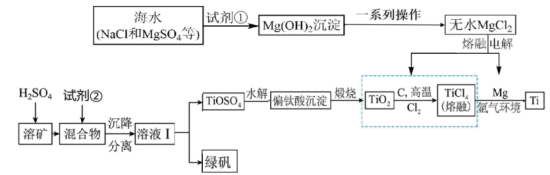
 的形式存在于溶液中,
的形式存在于溶液中, 易水解为偏钛酸
易水解为偏钛酸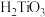 ,
,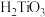 可写作
可写作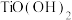 。
。(1)试剂①通常选煅烧的贝壳粉而不用
 的原因是
的原因是(2)试剂②为
(3)“沉降分离”出的滤渣成分有
(4)已知绿矾的溶解度随温度变化的曲线如图所示,从溶液Ⅰ获得绿矾的操作方法为
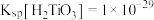 ,若要让
,若要让 水解完全(离子浓度小于
水解完全(离子浓度小于 ),应控制
),应控制 不低于
不低于(6)反应①除生成
 外还生成一种可燃性气体,该反应的化学方程式为
外还生成一种可燃性气体,该反应的化学方程式为 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于200℃,其原因是
,但实际生产中反应温度却远高于200℃,其原因是(7)该工艺流程中可以循环使用的物质有
您最近一年使用:0次
解题方法
2 . 计算并填空
(1)5.75g Na与水反应,得到200mL溶液。在标准状况下,生成的氢气的体积为__________ ;得到溶液的物质的量浓度为__________ 。
(2)已知,11.6g CO和 的混合物的总物质的量为0.3mol。
的混合物的总物质的量为0.3mol。
①计算混合气体的平均摩尔质量为__________ (小数点后保留一位有效数字);
②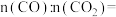
__________ 。
③将此混合气体通入 溶液中,若恰好得到
溶液中,若恰好得到 溶液,需要的NaOH溶液体积为
溶液,需要的NaOH溶液体积为__________ L。
(1)5.75g Na与水反应,得到200mL溶液。在标准状况下,生成的氢气的体积为
(2)已知,11.6g CO和
 的混合物的总物质的量为0.3mol。
的混合物的总物质的量为0.3mol。①计算混合气体的平均摩尔质量为
②
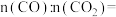
③将此混合气体通入
 溶液中,若恰好得到
溶液中,若恰好得到 溶液,需要的NaOH溶液体积为
溶液,需要的NaOH溶液体积为
您最近一年使用:0次
3 . 把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)13gZn的物质的量_______ (写出计算过程,下同);
(2)参加反应的HCl的物质的量_______ 。
(3)反应后ZnCl2的物质的量浓度_______ ;
(4)生成H2的体积(标准状况)_______ 。
(1)13gZn的物质的量
(2)参加反应的HCl的物质的量
(3)反应后ZnCl2的物质的量浓度
(4)生成H2的体积(标准状况)
您最近一年使用:0次
名校
解题方法
4 . 化学反应与能量
(1)已知



设有氢气和丙烷的混合气体5mol,完全燃烧时放出热量为3847kJ,则混合气体中氢气与丙烷的体积比是_______ 。
(2)甲醇( )广泛用作燃料电池的燃料,可由天然气来合成,已知:
)广泛用作燃料电池的燃料,可由天然气来合成,已知:
①

②
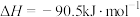
③
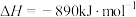
则甲醇的燃烧热为_______ 。
(3)向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量是5.12kJ。向足量的
溶液,放出的热量是5.12kJ。向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量为2.2kJ。则
溶液,放出的热量为2.2kJ。则 溶液与
溶液与 溶液反应的热化学方程式为
溶液反应的热化学方程式为


_______ 。
(4)已知:
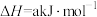

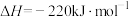
 、
、 和
和 键的键能分别为436、496和
键的键能分别为436、496和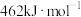 ,则a为
,则a为_______ 。
(1)已知




设有氢气和丙烷的混合气体5mol,完全燃烧时放出热量为3847kJ,则混合气体中氢气与丙烷的体积比是
(2)甲醇(
 )广泛用作燃料电池的燃料,可由天然气来合成,已知:
)广泛用作燃料电池的燃料,可由天然气来合成,已知:①


②

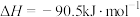
③

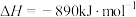
则甲醇的燃烧热为
(3)向足量的
 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量是5.12kJ。向足量的
溶液,放出的热量是5.12kJ。向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量为2.2kJ。则
溶液,放出的热量为2.2kJ。则 溶液与
溶液与 溶液反应的热化学方程式为
溶液反应的热化学方程式为

(4)已知:

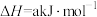

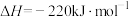
 、
、 和
和 键的键能分别为436、496和
键的键能分别为436、496和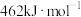 ,则a为
,则a为
您最近一年使用:0次
名校
解题方法
5 . 化学平衡常数和化学平衡计算
(1)已知在448℃时,反应 的平衡常数K为49,则该温度下反应
的平衡常数K为49,则该温度下反应 的平衡常数K′为
的平衡常数K′为_______ 。(用分数表示)
(2)某温度下,若把10mol 与30mol
与30mol 置于体积为10L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的
置于体积为10L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的
_______ 。(用分数表示)
(3)恒温恒压下,在一容积可变的容器中, 达到平衡状态时,
达到平衡状态时, 、
、 、
、 各1mol,若此时再充入3mol
各1mol,若此时再充入3mol ,则平衡
,则平衡_______ 移动(填“正向”、“逆向”或“不”)
(4)以水煤气为原料合成甲醇: ,容器为恒温、恒压
,容器为恒温、恒压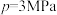 ,充入1mol
,充入1mol 和2mol
和2mol 达到平衡时
达到平衡时 的转化率为75%,平衡常数Kp=
的转化率为75%,平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(5)在1L真空密闭容器中加入amol 固体,t℃时发生如下反应:
固体,t℃时发生如下反应:
 ①
①
 ②
②
 ③
③
达平衡时,体系中 ,
, ,
, ,则t°C时反应①的平衡常数K值为
,则t°C时反应①的平衡常数K值为_______ (用字母表示)
(6)查阅资料知 的反应历程分两步:
的反应历程分两步:
Ⅰ.
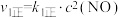 ;
;
Ⅱ. ;
; ;
;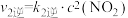
一定温度下,反应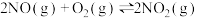 达到平衡状态,请写出用
达到平衡状态,请写出用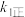 、
、 、
、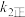 、
、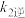 表示的平衡常数表达式
表示的平衡常数表达式
_______ 。
(1)已知在448℃时,反应
 的平衡常数K为49,则该温度下反应
的平衡常数K为49,则该温度下反应 的平衡常数K′为
的平衡常数K′为(2)某温度下,若把10mol
 与30mol
与30mol 置于体积为10L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的
置于体积为10L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的
(3)恒温恒压下,在一容积可变的容器中,
 达到平衡状态时,
达到平衡状态时, 、
、 、
、 各1mol,若此时再充入3mol
各1mol,若此时再充入3mol ,则平衡
,则平衡(4)以水煤气为原料合成甲醇:
 ,容器为恒温、恒压
,容器为恒温、恒压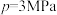 ,充入1mol
,充入1mol 和2mol
和2mol 达到平衡时
达到平衡时 的转化率为75%,平衡常数Kp=
的转化率为75%,平衡常数Kp=(5)在1L真空密闭容器中加入amol
 固体,t℃时发生如下反应:
固体,t℃时发生如下反应: ①
① ②
② ③
③达平衡时,体系中
 ,
, ,
, ,则t°C时反应①的平衡常数K值为
,则t°C时反应①的平衡常数K值为(6)查阅资料知
 的反应历程分两步:
的反应历程分两步:Ⅰ.

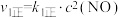 ;
;
Ⅱ.
 ;
; ;
;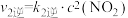
一定温度下,反应
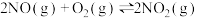 达到平衡状态,请写出用
达到平衡状态,请写出用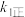 、
、 、
、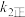 、
、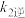 表示的平衡常数表达式
表示的平衡常数表达式
您最近一年使用:0次
22-23高二上·全国·课时练习
名校
解题方法
6 . 反应aA(g)+bB(g) cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
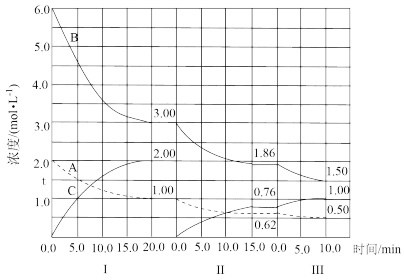
问题:
(1)反应的化学方程式中a∶b∶c为____ 。
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为____ 。
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是____ ,其值是____ 。
(4)由第一次平衡到第二次平衡,平衡向____ 移动,采取的措施是____ 。
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低;T2____ T3(填“<”“>”“=”),判断的理由是____ 。
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
问题:
(1)反应的化学方程式中a∶b∶c为
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡向
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低;T2
您最近一年使用:0次
2022-10-18更新
|
1095次组卷
|
4卷引用:内蒙古包钢第一中学2022-2023学年高二上学期月考化学试题
内蒙古包钢第一中学2022-2023学年高二上学期月考化学试题(已下线)2.2.3 化学反应速率和化学平衡图像——同步学习必备知识江西省赣州市十校协作2022-2023学年高二上学期期中联考化学试题河南省郑州中学2023-2024学年高三上学期第二次月考化学试题
名校
解题方法
7 . 3.84g铜溶于100mL的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变)。计算下列问题:
(1)产生气体的体积_________ (标准状况下)。
(2)生成的硝酸铜的物质的量浓度________ 。
(1)产生气体的体积
(2)生成的硝酸铜的物质的量浓度
您最近一年使用:0次
2022-12-14更新
|
920次组卷
|
3卷引用:内蒙古自治区第二地质中学2020-2021学年高一下学期第一次阶段检测化学试题
内蒙古自治区第二地质中学2020-2021学年高一下学期第一次阶段检测化学试题(已下线)【知识图鉴】单元讲练测必修第二册第五单元 02基础练上海市实验学校2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100mL硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,向反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。
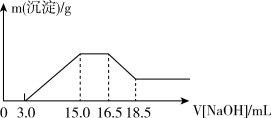
回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:_______ 。
(2)参加反应硝酸根离子物质的量为_______ mol。
(3)参加反应的铝与镁的物质的量之比为_______ 。
(4)混合液中硫酸的物质的量的浓度为_______ mol/L。

回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:
(2)参加反应硝酸根离子物质的量为
(3)参加反应的铝与镁的物质的量之比为
(4)混合液中硫酸的物质的量的浓度为
您最近一年使用:0次
解题方法
9 . 化学计量在化学中占有重要地位,回答下列问题:
(1)0.3molNH3分子中所含原子数约与___ 个H2O分子中所含原子数相等。
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO 的物质的量是
的物质的量是___ 。
(3)16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为___ 。
(4)在一定温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积气态化合物,则该化合物的化学式是___ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=___ 。
(1)0.3molNH3分子中所含原子数约与
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO
 的物质的量是
的物质的量是(3)16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)在一定温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积气态化合物,则该化合物的化学式是
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=
您最近一年使用:0次
名校
解题方法
10 . 在一密闭的2L容器中装有4molSO2和2molO2,在一定条件下开始反应2SO2(g)+O2(g) 2SO3(g)。2min末测得容器中有1.6molSO2,请计算:
2SO3(g)。2min末测得容器中有1.6molSO2,请计算:
(1)2min末SO3的浓度;___________
(2)2min内SO2的平均反应速率。___________
(3)2min末SO2的转化率。___________
(4)反应前后的压强之比。___________
 2SO3(g)。2min末测得容器中有1.6molSO2,请计算:
2SO3(g)。2min末测得容器中有1.6molSO2,请计算:(1)2min末SO3的浓度;
(2)2min内SO2的平均反应速率。
(3)2min末SO2的转化率。
(4)反应前后的压强之比。
您最近一年使用:0次



