1 . 随着科学技术的进步,科学家研究出了种类繁多的合金来满足各行各业的需求。称取某镁铝合金 放入过量氢氧化钠溶液中,制得
放入过量氢氧化钠溶液中,制得 (标准状况下),试回答:
(标准状况下),试回答:
(1)目前用量最大的合金是__________ ;常见的一些合金硬度比其成分金属的__________ 。
(2)该合金中镁铝的物质的量之比是多少_______ (写出计算过程)。
 放入过量氢氧化钠溶液中,制得
放入过量氢氧化钠溶液中,制得 (标准状况下),试回答:
(标准状况下),试回答:(1)目前用量最大的合金是
(2)该合金中镁铝的物质的量之比是多少
您最近一年使用:0次
解题方法
2 . 铝是典型的两性金属,既能与酸反应,又能与强碱溶液反应。回答下列问题:
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是___________ (升高/降低),还原剂都是___________ 。
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为___________ ,消耗氯化氢和氢氧化钠的物质的量之比为___________ 。
甲、乙两个烧杯中分别盛有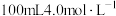 的盐酸和
的盐酸和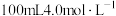 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为___________ 。反应中消耗的NaOH与HCl的物质的量之比为___________ 。
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为
甲、乙两个烧杯中分别盛有
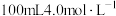 的盐酸和
的盐酸和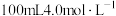 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
您最近一年使用:0次
解题方法
3 . 工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。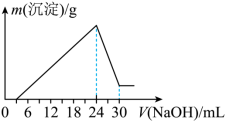
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
4 . 镁铝合金(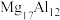 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为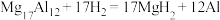 。得到的混合物Y(
。得到的混合物Y( )在一定条件下释放出氢气。在
)在一定条件下释放出氢气。在 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量?
的物质的量?___________ (请写出简要的计算过程,必须列出关系式)
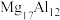 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为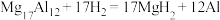 。得到的混合物Y(
。得到的混合物Y( )在一定条件下释放出氢气。在
)在一定条件下释放出氢气。在 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量?
的物质的量?
您最近一年使用:0次
解题方法
5 . 某同学在研究钠及其化合物的性质时,将一块纯净的金属钠置于氧气流中充分加热进行反应,最终得到淡黄色固体。冷却后称量固体的质量为7.8g,将该固体放入适量水中得到溶液500mL,且放出气体。请计算(写出计算过程):
(1)反应中生成气体的体积是多少(标准状况下)________ ?
(2)所得溶液中溶质的物质的量浓度是多少________ ?
(1)反应中生成气体的体积是多少(标准状况下)
(2)所得溶液中溶质的物质的量浓度是多少
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
(1)用20 g NaOH 配制成500 mL溶液,其物质的量浓度为_______ mol/L,从中取出1 mL,其物质的量浓度为_______ mol/L,含溶质_______ g。若将这1 mL溶液用水稀释到100 mL,所得溶液中溶质的物质的量浓度为_______ moI/L。
(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为_______ 。
(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为_______ 。
(4)标准状况下,1.7g NH3与_______ LH2S气体含有的氢原子数相同。
(1)用20 g NaOH 配制成500 mL溶液,其物质的量浓度为
(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为
(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
(4)标准状况下,1.7g NH3与
您最近一年使用:0次
2023-11-26更新
|
251次组卷
|
2卷引用:山西省实验中学2023-2024学年高一上学期期中考试化学试题
解题方法
7 . 已知常温下部分弱电解质的电离常数如表:
回答下列问题:
(1)常温下,物质的量浓度相同的三种溶液:① ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时, 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为_______ 。
(3) 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为_______ (用离子浓度表示) 。
(4)热的 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是_______ °
(5)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为_______ 。
(6)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: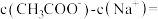
_______ mol/L(列出计算式即可,不需要计算准确值)。
| 弱电解质 | HClO |  |  |  |
| 电离常数 | 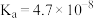 | 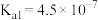 、 、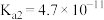 | 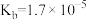 | 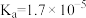 |
(1)常温下,物质的量浓度相同的三种溶液:①
 ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是(2)25℃时,
 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为(3)
 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为(4)热的
 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是(5)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为(6)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: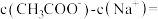
您最近一年使用:0次
解题方法
8 . 某稀硫酸和稀硝酸的混合溶液500mL,平均分成两等份。向第一份中逐渐加入铜粉,最多能溶解9.6g铜粉。向第二份中逐渐加入铁粉,产生气体的量随加入铁粉质量的变化如图所示(假设硝酸只被还原为 气体)。
气体)。

已知:不考虑溶液混合时体积和温度变化。
回答下列问题:
(1)在第一份溶液中,反应进行时:
①发生反应的离子方程式为_______ 。
②被消耗完全的离子为_______ (填离子符号)。
(2)在第二份溶液中:
①从反应开始至反应结束的过程中,产生的气体有_______ (填化学式),所得气体的总体积为_______ L(标准状况下)。
②检验a点溶液中金属离子的方法为_______ 。
③a→b的化学方程式为_______ 。
④c点溶液中,
_______  。
。
(3)原混合溶液中,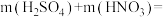
_______ g。
 气体)。
气体)。
已知:不考虑溶液混合时体积和温度变化。
回答下列问题:
(1)在第一份溶液中,反应进行时:
①发生反应的离子方程式为
②被消耗完全的离子为
(2)在第二份溶液中:
①从反应开始至反应结束的过程中,产生的气体有
②检验a点溶液中金属离子的方法为
③a→b的化学方程式为
④c点溶液中,

 。
。(3)原混合溶液中,
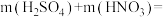
您最近一年使用:0次
2023-03-20更新
|
732次组卷
|
2卷引用:山西省2022-2023学年高一下学期3月联合考试化学试题
解题方法
9 . 向一瓶500 mL 0.4 mol/L的KI溶液中通入过量氯气后,将溶液蒸干并充分灼烧,试计算剩余固体的质量_______ 。
您最近一年使用:0次
解题方法
10 . 将18g铁铝合金投入足量NaOH溶液中,完全反应后生成2.24L氢气(标准状况),请计算此铁铝合金中铝的质量分数。(假设合金中其他成分不与NaOH反应)_______
您最近一年使用:0次



