名校
解题方法
1 . 回答下列问题
(1)0.5 mol水中含有___________ 个氢原子。
(2)9g水与___________ g硫酸所含的分子数相等。
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液___________ mL。
(4)标准状况下,和4mol 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为___________ 。
(5) 个
个 与
与___________ mol  质量相等。
质量相等。
(1)0.5 mol水中含有
(2)9g水与
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液
(4)标准状况下,和4mol
 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为(5)
 个
个 与
与 质量相等。
质量相等。
您最近一年使用:0次
名校
解题方法
2 . 移取20.00 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。
已知:
① 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;
② 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化
(1)加入 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为_______ 。
(2)酸化后 歧化发生离子反应方程式为
歧化发生离子反应方程式为_______ 。
(3)加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(4)则溶液中的 的浓度为
的浓度为_______ ; 的浓度为
的浓度为_______ 。
(5)若溶液酸化后将 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将_______ (填“偏大”、“偏小”或“不变”)。
 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。已知:
①
 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;②
 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化(1)加入
 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为(2)酸化后
 歧化发生离子反应方程式为
歧化发生离子反应方程式为(3)加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(4)则溶液中的
 的浓度为
的浓度为 的浓度为
的浓度为(5)若溶液酸化后将
 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将
您最近一年使用:0次
名校
解题方法
3 . 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。_______ 。硝酸所表现出的化学性质主要有_______
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是_______ g。
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则
①反应结束后的溶液中 、
、 的物质的量之比
的物质的量之比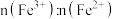 为
为_______ 。
②标准状况下,计算生成NO气体的体积_______ 。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。
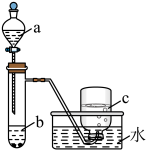
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol
 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则①反应结束后的溶液中
 、
、 的物质的量之比
的物质的量之比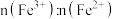 为
为②标准状况下,计算生成NO气体的体积
您最近一年使用:0次
2023-04-19更新
|
169次组卷
|
2卷引用:吉林省长春市第八中学2022-2023学年高一下学期4月考试化学试题
解题方法
4 . 把10.2g镁铝合金的粉末放入过量的盐酸中,得到11.2LH2(标准状况下)。试计算:
(1)该合金中镁的质量分数为_______ 。
(2)该合金中镁与铝的物质的量之比为_______ 。
(3)该合金溶于足量的烧碱溶液中,产生H2的体积(标准状况下)用是_______ ;
(1)该合金中镁的质量分数为
(2)该合金中镁与铝的物质的量之比为
(3)该合金溶于足量的烧碱溶液中,产生H2的体积(标准状况下)用是
您最近一年使用:0次
解题方法
5 . 在100mL含有0.3mol氯化氢的盐酸溶液中放入5.6g铁粉,经过2min收集到干燥纯净的氢气1.12L(标准状况下)。在这2min内用盐酸表示的该反应速率为_______ ,用氯化亚铁表示的反应速率为_______ 。在此之后又经过4min,铁粉恰好完全溶解,在此之后4min内,用盐酸表示的平均反应速率为_______ 。从反应开始至铁粉完全溶解的6min内,用氯化亚铁表示的平均反应速率为_______ 。整个反应过程前2min内的平均反应速率比后4min内平均反应速率快的原因是_______ 。
您最近一年使用:0次
解题方法
6 . 在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为物质的化学计量数。在0~3 min内,各物质的物质的量变化如表所示:
pZ(g)+qQ(g),式中m、n、p、q为物质的化学计量数。在0~3 min内,各物质的物质的量变化如表所示:
已知2 min内v(Q)=0.075 mol•L-1•min-1,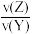 =
= 。
。
(1)试确定以下物质的相关量:起始时n(Y)=_____ ,n(Q)=____ 。
(2)化学方程式中m=_____ ,n=____ ,p=____ ,q=____ 。
(3)用Z表示2 min内的反应速率:_____ 。
(4)2 min末Q的转化率为_____ 。
 pZ(g)+qQ(g),式中m、n、p、q为物质的化学计量数。在0~3 min内,各物质的物质的量变化如表所示:
pZ(g)+qQ(g),式中m、n、p、q为物质的化学计量数。在0~3 min内,各物质的物质的量变化如表所示:| 物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | 0.8 |
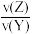 =
= 。
。(1)试确定以下物质的相关量:起始时n(Y)=
(2)化学方程式中m=
(3)用Z表示2 min内的反应速率:
(4)2 min末Q的转化率为
您最近一年使用:0次
2022-09-30更新
|
458次组卷
|
3卷引用:吉林省白城市通榆县毓才高级中学2022-2023学年高二上学期第一次月考化学试题
解题方法
7 . 常温下,1mLpH=13的Ba(OH)2溶液,其c(OH-)是_________ 。Ba(OH)2物质的量浓度是_________ 。0.01 mol·L-1的NaOH溶液的pH是_________ 。
您最近一年使用:0次
解题方法
8 . 某潜水艇上有50人,如果每人每分钟消耗的O2在标准状况下体积为0.08L(标准状况下O2的密度为1.429g/L),假设所需要的O2全部由Na2O2来提供,则该潜水艇一天所需要的Na2O2质量是_____ 千克。
您最近一年使用:0次
9 . 将一定量的CO2气体通入2 L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发)。

(1)O点溶液中所含溶质的化学式为_______ ,
(2)O到a点发生反应的离子方程式:_______ 。
(3)标准状况下通入CO2气体的体积为_______ L, NaOH溶液的物质的量浓度为_______ mol·L-1。

(1)O点溶液中所含溶质的化学式为
(2)O到a点发生反应的离子方程式:
(3)标准状况下通入CO2气体的体积为
您最近一年使用:0次
10 . 化学计量在化学中占有重要地位,请回答下列问题:
(1)青蒿素C15H22O5的摩尔质量为_______ 。
(2)在标准状况下,22.4 L由O2和N2组成的混合气体中,含有的分子总数约为_______ 。
(3)在标准状况下,含有 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为_______ 。
(4)某消毒小组人员用17 mol/L的浓硫酸配制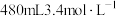 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为_______  ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为_______ 。
(5)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。标准状况下,向Ⅰ中充入8 g SO2,Ⅱ中充入8 g O2,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______ 。

(6)把7.8克镁铝合金的粉末放入过量的盐酸中,得到8.96 LH2 (标准状况)。该合金中铝和镁的物质的量之比_______ 。
(1)青蒿素C15H22O5的摩尔质量为
(2)在标准状况下,22.4 L由O2和N2组成的混合气体中,含有的分子总数约为
(3)在标准状况下,含有
 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为(4)某消毒小组人员用17 mol/L的浓硫酸配制
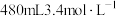 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为 ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为(5)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。标准状况下,向Ⅰ中充入8 g SO2,Ⅱ中充入8 g O2,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为

(6)把7.8克镁铝合金的粉末放入过量的盐酸中,得到8.96 LH2 (标准状况)。该合金中铝和镁的物质的量之比
您最近一年使用:0次



