解题方法
1 . 将硝酸钠(NaNO3)和硝酸钡[Ba(NO3)2]的混合物29.1g放入烧杯,加入100.0g水使其完全溶解,再加入94.2g硫酸钠溶液恰好完全反应,过滤(忽略溶液的损失),称得滤液的质量为200.0g。请计算:
(1)恰好完全反应后产生的沉淀质量为______ g。
(2)所得滤液的溶质质量分数(写出完整的解题过程)________ 。
(1)恰好完全反应后产生的沉淀质量为
(2)所得滤液的溶质质量分数(写出完整的解题过程)
您最近一年使用:0次
2 . 现有2g质量H2,计算:
(1)氢原子是_______ 个;
(2)H2的摩尔质量为_______ ;
(3)氢分子是_______ 个;
(4)在标况下,体积是_______ 升;
(5)H2_______ (填“是”或“不是”)我们的理想能源,常用_______ 方法或_______ 方法收集;
(1)氢原子是
(2)H2的摩尔质量为
(3)氢分子是
(4)在标况下,体积是
(5)H2
您最近一年使用:0次
解题方法
3 . 计算题
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为:_______ 。
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl(g)+HCl(g) ΔH1>0
SiHCl(g)+HCl(g) ΔH1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g) 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3
反应③的ΔH3=_______ (用ΔH1、ΔH2表示)。
(3)实现反应 对减少温室气体排放和减缓燃料危机具有重要意义。
对减少温室气体排放和减缓燃料危机具有重要意义。
已知:

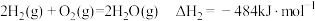

则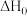 =
=_______  。
。
(4)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法高炉内可能发生的反应:
①C(s) +O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s) + CO2(g)= 2CO(g) △H2=+172.5 kJ/mol
③4CO(g) + Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol
则:3Fe(s)+2O2(g)= Fe3O4(s) △H=_______ 。
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为:
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)
 SiHCl(g)+HCl(g) ΔH1>0
SiHCl(g)+HCl(g) ΔH1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)
 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3反应③的ΔH3=
(3)实现反应
 对减少温室气体排放和减缓燃料危机具有重要意义。
对减少温室气体排放和减缓燃料危机具有重要意义。已知:

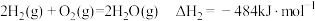

则
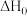 =
= 。
。(4)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法高炉内可能发生的反应:
①C(s) +O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s) + CO2(g)= 2CO(g) △H2=+172.5 kJ/mol
③4CO(g) + Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol
则:3Fe(s)+2O2(g)= Fe3O4(s) △H=
您最近一年使用:0次
解题方法
4 . 回答下列问题
(1)填写关于物质的量计算的四个恒等式:n=___________ =___________ =___________ =___________ 。
(2)0.5molO3(臭氧)中含有的分子数是___________ 个、原子数是___________ 个。
(3)0.5mol的Fe含___________ 个铁原子,质量是___________ g;2.107×1024个铁原子是___________ molFe,质量为___________ g。
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。
(1)填写关于物质的量计算的四个恒等式:n=
(2)0.5molO3(臭氧)中含有的分子数是
(3)0.5mol的Fe含
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
您最近一年使用:0次
名校
5 . 将一定质量的镁、铝合金投入100mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5mol·L-1NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液的体积的关系如图,回答下列问题:
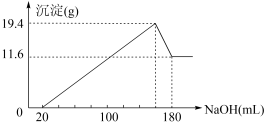
(1)写出Al与NaOH溶液反应的离子方程式:____ 。
(2)计算原合金中镁、铝的质量____ (请写出具体的计算过程,计算结果保留一位小数)。

(1)写出Al与NaOH溶液反应的离子方程式:
(2)计算原合金中镁、铝的质量
您最近一年使用:0次
6 . 为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
(1)有机物A的相对分子质量是_______ ;
(2)有机物A的最简式分子式是_______ ,分子式是_______
(3)写出有机物A的结构简式:_______ 。
(4)写出有机物A的一种同分异构体结构简式:_______ 。
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。

(1)有机物A的相对分子质量是
(2)有机物A的最简式分子式是
(3)写出有机物A的结构简式:
(4)写出有机物A的一种同分异构体结构简式:
您最近一年使用:0次
2021-05-11更新
|
342次组卷
|
3卷引用:西藏自治区山南市第二高级中学2020-2021学年高二下学期期中考试化学试题
西藏自治区山南市第二高级中学2020-2021学年高二下学期期中考试化学试题(已下线)专题一 有机化合物的结构特点与研究方法-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修3)6月刊 (期末复习必刷题)河北省石家庄北华中学2023-2024学年高三上学期10月月考考试化学试题
7 . (1)1.5mol氧气中含有的O2的个数为___________ ,标准状况下体积为___________ L,与___________ gH2O所含的原子总数相等。
(2)在标准状况下,体积为6.72L的NO和NO2混合气,质量为11.88g,则NO和NO2的体积比为___________ 。
(3)某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO 的物质的量是
的物质的量是___________ 。
(2)在标准状况下,体积为6.72L的NO和NO2混合气,质量为11.88g,则NO和NO2的体积比为
(3)某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO
 的物质的量是
的物质的量是
您最近一年使用:0次
解题方法
8 . (1)等质量的CO和CO2,物质的量之比为_____ ,氧原子个数之比为____ 。
(2)1.5molH2SO4的质量是___ g,其中含有___ molH,含有____ g氧原子。
(3)18.06×1023个氨分子(NH3)的物质的量为____ mol,含有__ mol氢原子、____ mol电子。
(2)1.5molH2SO4的质量是
(3)18.06×1023个氨分子(NH3)的物质的量为
您最近一年使用:0次
名校
解题方法
9 . (1)一定温度下,在密闭容器中通入一定量的NO2,发生反应:2NO2(g) 2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
则:①该可逆反应的平衡常数K=___ (请用数字计算式表达)。
②此时NO2的转化率____ 。
(2)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
计算:①5min末A的物质的量浓度为___ ;
②前5min内用B表示的化学反应速率v(B)为___ ;
③化学方程式中n值为___ 。
 2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。则:①该可逆反应的平衡常数K=
②此时NO2的转化率
(2)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)
 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算:①5min末A的物质的量浓度为
②前5min内用B表示的化学反应速率v(B)为
③化学方程式中n值为
您最近一年使用:0次
名校
10 . (1)1.5molH2SO4的质量是__ g,其中含有__ molH,含有__ g氧原子。
(2)等质量的CO和CO2,物质的量之比为__ ,氧原子个数之比为__ 。
(3)9.03×1023个氨分子(NH3)的物质的量为__ mol,含有__ mol氢原子,__ mol电子。
(2)等质量的CO和CO2,物质的量之比为
(3)9.03×1023个氨分子(NH3)的物质的量为
您最近一年使用:0次



