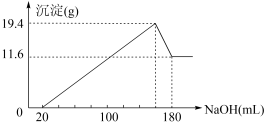
将一定质量的镁、铝合金投入100mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5mol·L-1NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液的体积的关系如图,回答下列问题:
(1)写出Al与NaOH溶液反应的离子方程式:____ 。
(2)计算原合金中镁、铝的质量____ (请写出具体的计算过程,计算结果保留一位小数)。

(1)写出Al与NaOH溶液反应的离子方程式:
(2)计算原合金中镁、铝的质量
更新时间:2022-04-13 17:11:57
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)在标准状况下,①4g氢气②33.6L甲烷③3.01×1023个H2S分子,含分子数最多的是______ (填序号,下同),质量最大的是______ ,体积最小的是______ ;
(2)同温同压下,质量相同的CO和CO2气体的体积之比为______ ;
(3)用1L0.1mol/LBaCl2溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸钠三种溶液中的SO42-完全转化为BaSO4沉淀,则三种溶液中溶质的物质的量浓度之比依次是______ 。
(2)同温同压下,质量相同的CO和CO2气体的体积之比为
(3)用1L0.1mol/LBaCl2溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸钠三种溶液中的SO42-完全转化为BaSO4沉淀,则三种溶液中溶质的物质的量浓度之比依次是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6升,再在此溶液中加入过量NaOH溶液,最终得到沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少?________
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积?________ 。
(1)Mg、Al的物质的量各为多少?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在标准状况下,进行甲、乙、丙三组实验,三组实验各取30mL同浓度的盐酸,加入同一种镁、铝混合物粉末,产生气体,有关数据列表如下:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 1020 |
| 气体体积/mL | 560 | 672 | 672 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)等质量的两份铝分别和足量的盐酸、氢氧化钠溶液反应,所得H2的体积比为___________ ;
(2)足量的两份铝分别和等体积、等物质的量浓度的盐酸和氢氧化钠溶液反应,产生H2的体积比为___________ ;
(3)甲、乙两个烧杯,各盛有100mL、3mol/L的盐酸和氢氧化钠溶液,向两烧杯分别加入等质量的铝粉,反应后,测得甲、乙两烧杯中产生气体体积比为1:2,则加入铝粉的质量为____ g;
(4)现有100mL、2mol/L的NaOH溶液,欲制Na2CO3,若直接通入CO2,则不容易掌握CO2的用量。因为CO2通得过少,则会有NaOH剩余;若通入过量CO2,则又会有___________ 产生。于是小强同学设计了下列方案:(请补充完整后面步骤)
①先将100mL NaOH溶液分为两等份;
②_______
③_______
则可得到Na2CO3溶液。
(2)足量的两份铝分别和等体积、等物质的量浓度的盐酸和氢氧化钠溶液反应,产生H2的体积比为
(3)甲、乙两个烧杯,各盛有100mL、3mol/L的盐酸和氢氧化钠溶液,向两烧杯分别加入等质量的铝粉,反应后,测得甲、乙两烧杯中产生气体体积比为1:2,则加入铝粉的质量为
(4)现有100mL、2mol/L的NaOH溶液,欲制Na2CO3,若直接通入CO2,则不容易掌握CO2的用量。因为CO2通得过少,则会有NaOH剩余;若通入过量CO2,则又会有
①先将100mL NaOH溶液分为两等份;
②
③
则可得到Na2CO3溶液。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将一定质量的镁和铝的合金投入100 mL,一定物质的量浓度的盐酸中,恰好反应,共产生气体5.6 L(标准状况下),向所得溶液中滴加5mol·L-1NaOH溶液至过量,最终产生白色沉淀13.6 g。请计算:
(1)原合金中镁和铝的质量分别是________ 。
(2)原盐酸溶液的物质的量浓度________ 。
(1)原合金中镁和铝的质量分别是
(2)原盐酸溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】计算题
(1)含0.4 mol Al3+ 的Al2 (SO4 )3中所含的SO 的物质的量是
的物质的量是_______ 。
(2)_______ mol H2O2所含原子数与0.2mol H3PO4所含原子数相等。
(3)把10.2 g镁铝合金的粉末放入过量的烧碱中,得到6.72 L标准状况下的H2。
分别进行下列相关计算(要求写出必要的计算过程)。
① 该合金中铝的质量分数为_______ ;
② 该合金中镁与铝的物质的量之比为_______ ;
③ 该合金溶于足量的盐酸溶液中,产生H2的体积(标准状况下)为_______ 。
(1)含0.4 mol Al3+ 的Al2 (SO4 )3中所含的SO
 的物质的量是
的物质的量是(2)
(3)把10.2 g镁铝合金的粉末放入过量的烧碱中,得到6.72 L标准状况下的H2。
分别进行下列相关计算(要求写出必要的计算过程)。
① 该合金中铝的质量分数为
② 该合金中镁与铝的物质的量之比为
③ 该合金溶于足量的盐酸溶液中,产生H2的体积(标准状况下)为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气相对分子质量为29,则A的相对分子质量是_______________
(2)把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为___________
(3)已知铜和稀硝酸反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则被氧化的物质与被还原的物质质量比为___________
(4)A、B两个烧瓶中分别装80mL 3.0 mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体的体积比为A:B=2:5,则加入铝粉的质量为___________
(2)把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为
(3)已知铜和稀硝酸反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则被氧化的物质与被还原的物质质量比为
(4)A、B两个烧瓶中分别装80mL 3.0 mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体的体积比为A:B=2:5,则加入铝粉的质量为
您最近一年使用:0次

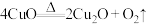 。计算:
。计算:

