在标准状况下,进行甲、乙、丙三组实验,三组实验各取30mL同浓度的盐酸,加入同一种镁、铝混合物粉末,产生气体,有关数据列表如下:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 1020 |
| 气体体积/mL | 560 | 672 | 672 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
更新时间:2016-04-07 17:36:33
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000mol•L﹣1的K2Cr2O7标准溶液240mL,应准确称取K2Cr2O7的质量是 ___________ g[保留4位有效数字,已知M(K2Cr2O7)=294.0g•mol﹣1]。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)1mol H2SO4中约含有______ 个H2SO4,______ mol H ,______ mol O;
(2)9.03×1023个CO2的物质的量是______ mol,在标准状况下的体积______ L,质量是是______ 克。
(3)在100mL2mol/LH2SO4溶液中,H2SO4的质量是______ 克。H+的物质的量浓度为____________ 。
(4)质量分数为36.5%、密度为1.18g/cm3的浓盐酸中HCl的物质的量浓度为_____________ 。
(2)9.03×1023个CO2的物质的量是
(3)在100mL2mol/LH2SO4溶液中,H2SO4的质量是
(4)质量分数为36.5%、密度为1.18g/cm3的浓盐酸中HCl的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
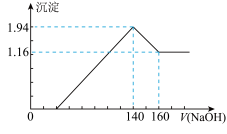
求:(1)合金中Mg,Al的质量_______________ ;
(2)所用HCl的物质的量浓度_______________ 。

求:(1)合金中Mg,Al的质量
(2)所用HCl的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将0.1mol的镁铝混合物溶于100mL 2 mol·L-1的H2SO4中,然后再滴加1 mol·L-1的NaOH溶液。请回答:

(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示。当V1=160mL时,则金属粉末中,n(Mg)=_______ mol
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V (NaOH)=_______ mL

(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示。当V1=160mL时,则金属粉末中,n(Mg)=
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V (NaOH)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如表(气体体积均为标准状况下测得):
(1)甲组实验中,盐酸_____ ;乙组实验中,盐酸_____ (填“过量“、“适量“或“不足“)。
(2)该盐酸的物质的量浓度_____ 。
(3)合金中Mg、Al的物质的量之比为____ 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为 ,并使Mg2+刚好沉淀完全,则溶液中
,并使Mg2+刚好沉淀完全,则溶液中 的物质的量为
的物质的量为_____ mol;溶液中Na+的物质的量为______ mol。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 0.255 | 0.385 | 0.459 |
| 生成气体/ml | 280 | 336 | 336 |
(1)甲组实验中,盐酸
(2)该盐酸的物质的量浓度
(3)合金中Mg、Al的物质的量之比为
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为
 ,并使Mg2+刚好沉淀完全,则溶液中
,并使Mg2+刚好沉淀完全,则溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】把3.06 g铝和镁的混合物粉末放入100 mL盐酸中,恰好完全反应,并得到标准状况下3.36 LH2 计算:(要有过程)
(1)该合金中铝的物质的量_____ 。
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)____ 。
(1)该合金中铝的物质的量
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】由于镁合金具有硬度大、密度小、散热性好、抗震性好等优异性能它被用于制笔记本电脑外壳、竞赛自行车车架等。现称取一定质量的镁铝合金样品放入500mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH 溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

试计算:
(1)合金中Al的质量______ 。
(2)NaOH溶液的物质的量浓度_____

试计算:
(1)合金中Al的质量
(2)NaOH溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。求原混合物中单质铁的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】5.00g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示:
请回答下列问题:
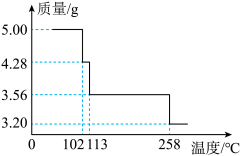
(1)试确定110℃时固体物质的化学式___________ ;
(2)取200℃所得样品,加热至280℃,该反应的化学方程式为:__________________________________
(3)将280℃所得产物在570℃下灼烧得到的主要产物是1.60g黑色粉末和一种氧化性气体,黑色粉末的化学式为______________ 。
请回答下列问题:

(1)试确定110℃时固体物质的化学式
(2)取200℃所得样品,加热至280℃,该反应的化学方程式为:
(3)将280℃所得产物在570℃下灼烧得到的主要产物是1.60g黑色粉末和一种氧化性气体,黑色粉末的化学式为
您最近一年使用:0次




