解题方法
1 . 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)计算H2S的平衡转化率a=_____ (写出计算过程)。
(2)计算浓度平衡常数K=_____ 。(写出计算过程)。
 COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)计算H2S的平衡转化率a=
(2)计算浓度平衡常数K=
您最近一年使用:0次
2 . 将标准状况下 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度_____ (忽略溶液体积的变化)。
 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度
您最近一年使用:0次
解题方法
3 . 为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为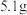 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少_____ 。
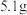 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少
您最近一年使用:0次
名校
解题方法
4 . 利用所学化学反应原理知识进行计算:
(1)某温度下,纯水中的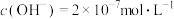 ,若温度不变,滴入稀硫酸使
,若温度不变,滴入稀硫酸使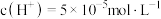 ,则由水电离出的
,则由水电离出的
___________ 。
(2)将99mLpH=2盐酸与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至25℃时溶液的
___________ 。
(3)0.2mol/L的 和0.1mol/L NaOH溶液等体积混合后的溶液中:
和0.1mol/L NaOH溶液等体积混合后的溶液中: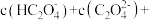
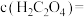
___________ mol/L。
(4)常温下,向100mL0.2mol/L的 溶液中加入200mL0.15mol/L的盐酸(混合后溶液的体积变化忽略不计),已知25℃时,
溶液中加入200mL0.15mol/L的盐酸(混合后溶液的体积变化忽略不计),已知25℃时, ,混合后溶液中
,混合后溶液中
___________ mol/L。
(1)某温度下,纯水中的
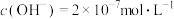 ,若温度不变,滴入稀硫酸使
,若温度不变,滴入稀硫酸使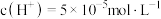 ,则由水电离出的
,则由水电离出的
(2)将99mLpH=2盐酸与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至25℃时溶液的

(3)0.2mol/L的
 和0.1mol/L NaOH溶液等体积混合后的溶液中:
和0.1mol/L NaOH溶液等体积混合后的溶液中: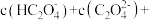
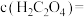
(4)常温下,向100mL0.2mol/L的
 溶液中加入200mL0.15mol/L的盐酸(混合后溶液的体积变化忽略不计),已知25℃时,
溶液中加入200mL0.15mol/L的盐酸(混合后溶液的体积变化忽略不计),已知25℃时, ,混合后溶液中
,混合后溶液中
您最近一年使用:0次
名校
解题方法
5 . 某兴趣小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

(1)向饱和NaCl溶液中通入 和氨气时,应先通入
和氨气时,应先通入___________ (填化学式)。操作①的名称为___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)该流程中可循环利用的物质是___________ (填化学式)。
(4)现将 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)下列选项中哪种方法可以鉴别 溶液和
溶液和 溶液___________。
溶液___________。
(6)下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。

(1)向饱和NaCl溶液中通入
 和氨气时,应先通入
和氨气时,应先通入(2)写出反应①的化学方程式:
(3)该流程中可循环利用的物质是
(4)现将
 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(5)下列选项中哪种方法可以鉴别
 溶液和
溶液和 溶液___________。
溶液___________。| A.加入澄清石灰水 | B.加入氢氧化钠溶液 |
| C.加热 | D.逐滴加入稀盐酸 |
(6)下列实验方案中,不能测定出
 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。
| A.Li、Na、K的原子半径和密度都随原子序数的增加而增大 |
B.碱性: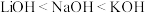 |
C.还原性: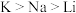 ,故K可以从NaCl溶液中置换出金属钠 ,故K可以从NaCl溶液中置换出金属钠 |
D.熔、沸点: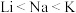 |
您最近一年使用:0次
2023-12-23更新
|
145次组卷
|
3卷引用:安徽省阜阳市第三中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
6 . 化学计量在生产和科研中应用广泛。回答下列问题:
(1) 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为___________ ,其质子的物质的量为___________ 。
(2)某气态氧化物的化学式为 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)若 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为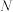 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为___________ (用含字母的代数式表示)。
(4)标准状况下将a LX气体(摩尔质量为 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________ 。
(5)将 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为___________ (忽略混合前后溶液体积的变化)。
(6)某混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
___________ 。
(1)
 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为(2)某气态氧化物的化学式为
 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为(3)若
 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为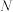 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为(4)标准状况下将a LX气体(摩尔质量为
 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)将
 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为(6)某混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
您最近一年使用:0次
2023-09-21更新
|
234次组卷
|
2卷引用:安徽省合肥六校联考2023-2024学年高三上学期期中联考化学试题
解题方法
7 . 100mL6.0mol•L-1稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。请回答以下问题:
(1)铜和稀硝酸反应的化学方程式_______ ,该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)原混合物中铜的物质的量为多少_______ ?氧化铜的质量为多少_______ ?(写出计算过程)
(1)铜和稀硝酸反应的化学方程式
(2)原混合物中铜的物质的量为多少
您最近一年使用:0次
名校
解题方法
8 . 雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为___________ 。
(2)上述反应中的氧化剂是___________ ,反应产生的气体可用___________ 吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO =2H3AsO4+3S↓+10NO2↑+2H2O。若生成2 mol H3AsO4,则反应中被S元素还原的NO
=2H3AsO4+3S↓+10NO2↑+2H2O。若生成2 mol H3AsO4,则反应中被S元素还原的NO 的物质的量为
的物质的量为___________
(4)若反应产物NO2与11.2 L O2(标准状况)混合后用水吸收全部转化成浓硝酸,然后与过量的碳反应所产生的CO2的物质的量___________ (选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5 mol d.无法确定
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为
(2)上述反应中的氧化剂是
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO
 =2H3AsO4+3S↓+10NO2↑+2H2O。若生成2 mol H3AsO4,则反应中被S元素还原的NO
=2H3AsO4+3S↓+10NO2↑+2H2O。若生成2 mol H3AsO4,则反应中被S元素还原的NO 的物质的量为
的物质的量为(4)若反应产物NO2与11.2 L O2(标准状况)混合后用水吸收全部转化成浓硝酸,然后与过量的碳反应所产生的CO2的物质的量
a.小于0.5 mol b.等于0.5 mol c.大于0.5 mol d.无法确定
您最近一年使用:0次
名校
解题方法
9 . 化学计量在化学中占有重要地位。请回答下列问题:
(1)长征系列运载火箭的燃料之一是肼( )。回答下列问题:肼的摩尔质量是
)。回答下列问题:肼的摩尔质量是____________ ,16g肼中含有氮原子的数目为________ 。
(2)22.2g某二价金属氯化物( )中含有0.4mol
)中含有0.4mol  ,则
,则 的物质的量是
的物质的量是____________ ;A的相对原子质量是____________ 。
(3)现有0.4mol的CO和 的混合气体,质量共12.8g,则
的混合气体,质量共12.8g,则 的质量为
的质量为____________ 。
(1)长征系列运载火箭的燃料之一是肼(
 )。回答下列问题:肼的摩尔质量是
)。回答下列问题:肼的摩尔质量是(2)22.2g某二价金属氯化物(
 )中含有0.4mol
)中含有0.4mol  ,则
,则 的物质的量是
的物质的量是(3)现有0.4mol的CO和
 的混合气体,质量共12.8g,则
的混合气体,质量共12.8g,则 的质量为
的质量为
您最近一年使用:0次
名校
10 . I.如图为10mL一定物质的量浓度的盐酸用一定浓度的NaOH溶液滴定的图示。
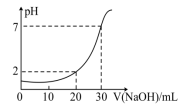
(1)盐酸的浓度为______ 。
(2)NaOH溶液的浓度为______ 。
(3)当滴加NaOH溶液至26mL时,溶液的pH为______ 。
Ⅱ.已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,Ksp[Mg(OH)2]=4.0×10-12,lg5=0.7。请回答下列问题:
(4)25℃时,若向50mL0.018mol•L-1的AgNO3溶液中加入50mL0.020mol•L-1的盐酸,混合后溶液中的c(Ag+)为______ mol•L-1,pH为______ 。
(5)25℃时,Mg(OH)2饱和溶液______ (填“能”或“不能”)使石蕊溶液变蓝色。

(1)盐酸的浓度为
(2)NaOH溶液的浓度为
(3)当滴加NaOH溶液至26mL时,溶液的pH为
Ⅱ.已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,Ksp[Mg(OH)2]=4.0×10-12,lg5=0.7。请回答下列问题:
(4)25℃时,若向50mL0.018mol•L-1的AgNO3溶液中加入50mL0.020mol•L-1的盐酸,混合后溶液中的c(Ag+)为
(5)25℃时,Mg(OH)2饱和溶液
您最近一年使用:0次



