1 . 常温时,用石墨电极电解500mLNaCl和CuSO4混合溶液,当电路中通过2mol电子时,两极均产生标准状况下16.8L气体,其中阳极产生的O2在标准状况下是5.6L(假定产生的气体全部放出,电解前后溶液体积变化忽略不计),求:
(1)原溶液中c(NaCl)=___________ ,c(CuSO4)=___________ 。
(2)电解后溶液的c(OH-)=___________ 。
(1)原溶液中c(NaCl)=
(2)电解后溶液的c(OH-)=
您最近一年使用:0次
2 . 用铂作电极电解1000mL 0.1mol/L AgNO3溶液,通电一段时间后关闭电源,测得溶液的质量减少了13.4g。请回答:
(1)写现电解过程中阴极反应的电极反应式___________ 。
(2)电解过程中流经外电路的电子数目为___________ 。
(3)加入___________ 使电解液彻底复原(填具体物质及其物质的量)。
(1)写现电解过程中阴极反应的电极反应式
(2)电解过程中流经外电路的电子数目为
(3)加入
您最近一年使用:0次
解题方法
3 . 0.16gNaOH恰好与20mL的盐酸完全反应,求盐酸中 的物质的量浓度
的物质的量浓度________ 。
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
名校
4 . 已知水在100℃时,Kw=10-12。
(1)在100℃下,某溶液中由水电离产生的c(H+)=1×10-9,则该溶液的pH=_______ 。
(2)100℃时,某BaCl2溶液中c(Cl-)=2×10-2 mol·L-1,取该溶液1mL加水稀释至100mL,则稀释后溶液中c(Ba2+)∶c(H+)=____ 。
(3)100℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是_____ 。
(4)100℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为_____ 。
(5)常温下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=_____ 。
(6)已知HA的Ka=1×10-5,常温下,取V1 L pH=3的HA溶液与V2 L pH=11的NaOH溶液混合,若混合后溶液pH=7,则大小关系:V1____ V2(填“大于”“小于”或“等于”)。
(7)常温下,将a mol·L-1NaOH溶液和b mol·L-1醋酸溶液等体积混合,反应后溶液恰好显中性,醋酸的电离平衡常数为______ (用a、b表示)。
(8)常温下,甲、乙两烧杯中分别有等体积pH=2和pH=3的HA溶液,加入等浓度的NaOH溶液,恰好完全反应时,消耗的NaOH溶液的体积:V甲____ 10V乙(填“大于”“小于”或“等于”)。
(1)在100℃下,某溶液中由水电离产生的c(H+)=1×10-9,则该溶液的pH=
(2)100℃时,某BaCl2溶液中c(Cl-)=2×10-2 mol·L-1,取该溶液1mL加水稀释至100mL,则稀释后溶液中c(Ba2+)∶c(H+)=
(3)100℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(4)100℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为
(5)常温下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=
(6)已知HA的Ka=1×10-5,常温下,取V1 L pH=3的HA溶液与V2 L pH=11的NaOH溶液混合,若混合后溶液pH=7,则大小关系:V1
(7)常温下,将a mol·L-1NaOH溶液和b mol·L-1醋酸溶液等体积混合,反应后溶液恰好显中性,醋酸的电离平衡常数为
(8)常温下,甲、乙两烧杯中分别有等体积pH=2和pH=3的HA溶液,加入等浓度的NaOH溶液,恰好完全反应时,消耗的NaOH溶液的体积:V甲
您最近一年使用:0次
5 . 分类法是进行化学研究的重要方法。不同的标准可以把物质和反应分为不同的类别。回答下列问题:
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是___________ (填序号);属于非电解质的是___________ (填序号);③在水中的电离方程式为___________ 。
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是___________ (填标号)。

A. B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg
(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式___________ 。
②完善下面的化学方程式,并配平___________ 。

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素( )。写出发生反应的离子方程式
)。写出发生反应的离子方程式___________ 。
(4)在20.00ml 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用
 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式②完善下面的化学方程式,并配平

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素(
 )。写出发生反应的离子方程式
)。写出发生反应的离子方程式(4)在20.00ml
 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________A. | B. | C. | D.V |
您最近一年使用:0次
名校
6 . 根据要求,完成下列各题:
(1)把含有 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为___________ 。
(2)某气态氧化物化学式为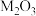 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为___________ 。
(3)标准状况下,把11.2L 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是___________ g。
(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有___________ ,属于非电解质的有___________ ,能导电的有___________ 。(填序号)
(1)把含有
 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为(2)某气态氧化物化学式为
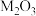 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为(3)标准状况下,把11.2L
 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤
 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
您最近一年使用:0次
2023-12-23更新
|
171次组卷
|
2卷引用:2024届河南省焦作市博爱县第一中学高三一模化学试题
名校
7 . 已知几种含碳物质间的转化及能量变化关系如图所示。
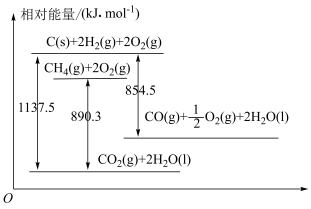
(1)写出表示CO燃烧热的热化学方程式:___________ 。
(2)反应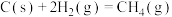

___________  ,该反应中反应物的总键能
,该反应中反应物的总键能___________ (填“大于”、“小于”或“等于”)生成物的总键能。若18gC(s)与 反应,完全转化成
反应,完全转化成 ,需要
,需要___________ (填“吸收”或“放出”)___________ kJ能量。
(3)在25℃、101kPa下,30g由 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为___________ mol、___________ mol。

(1)写出表示CO燃烧热的热化学方程式:
(2)反应
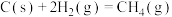

 ,该反应中反应物的总键能
,该反应中反应物的总键能 反应,完全转化成
反应,完全转化成 ,需要
,需要(3)在25℃、101kPa下,30g由
 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为
您最近一年使用:0次
2023-11-21更新
|
141次组卷
|
2卷引用:河南省新乡市2023-2024学年高二上学期期中考试化学试题
解题方法
8 . 已知几种含碳物质间的转化及能量变化关系如图所示。

(1)写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:___________ ,若有672mL(标准状况下) 完全燃烧,会放出
完全燃烧,会放出___________ kJ能量。
(2)反应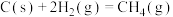
 =
=___________ kJ⋅mol-1,该反应中反应物的总键能___________ (填“大于”、“小于”或“等于”)生成物的总键能;若18gC(s)与 反应,完全转化成
反应,完全转化成 ,需要
,需要___________ (填“吸收”或“放出”)___________ kJ能量。
(3)在25℃、101kPa下,30g由 和
和 组成的混合气体完全燃烧生成
组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ,则混合气体中
和液态水,放出热量1031.8kJ,则混合气体中 和
和 的物质的量分别为
的物质的量分别为___________ mol、___________ mol。

(1)写出表示
 燃烧热的热化学方程式:
燃烧热的热化学方程式: 完全燃烧,会放出
完全燃烧,会放出(2)反应
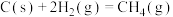
 =
= 反应,完全转化成
反应,完全转化成 ,需要
,需要(3)在25℃、101kPa下,30g由
 和
和 组成的混合气体完全燃烧生成
组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ,则混合气体中
和液态水,放出热量1031.8kJ,则混合气体中 和
和 的物质的量分别为
的物质的量分别为
您最近一年使用:0次
解题方法
9 . 回答下列问题:
(1)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和相应的能量图如图。
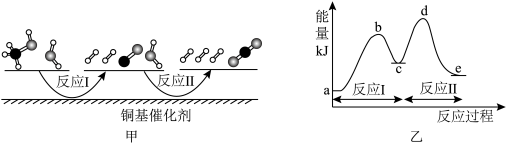
已知:a,b,c,d,e均表示能量值。
①选择优良的催化剂降低反应I和Ⅱ的活化能,有利于_____ (填“增加”或“减少”)过程中的能耗,反应Ⅱ的热化学方程式为_____ 。
②该反应属于_____ (填“放热”或“吸热”)反应,请写出总反应的热化学方程式:_____ 。
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合并在高温下煅烧,所得物质可作耐高温材料:
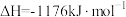 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为_____ 。
(3)氮气与氢气反应合成氨的能量变化如图所示,则热化学方程式为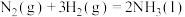

_____ 。
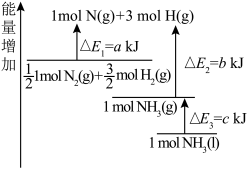
(4)下表是部分化学键的键能数据。
①已知1mol白磷完全燃烧生成固态 的反应热
的反应热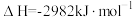 ,白磷(P4)、P4O6、P4O10结构如图所示,则上表中
,白磷(P4)、P4O6、P4O10结构如图所示,则上表中
_____ 。
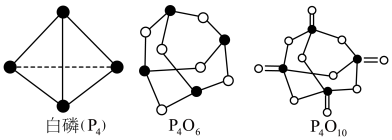
②0.5mol白磷(P4)与O2完全反应生成固态P4O6,放出的热量为_____ kJ。
(1)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和相应的能量图如图。

已知:a,b,c,d,e均表示能量值。
①选择优良的催化剂降低反应I和Ⅱ的活化能,有利于
②该反应属于
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合并在高温下煅烧,所得物质可作耐高温材料:

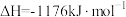 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(3)氮气与氢气反应合成氨的能量变化如图所示,则热化学方程式为
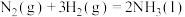


(4)下表是部分化学键的键能数据。
| 化学键 |  |  |  | 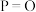 |
| 键能/(kJ·mol-1) | 198 | 360 | 498 |  |
 的反应热
的反应热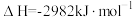 ,白磷(P4)、P4O6、P4O10结构如图所示,则上表中
,白磷(P4)、P4O6、P4O10结构如图所示,则上表中

②0.5mol白磷(P4)与O2完全反应生成固态P4O6,放出的热量为
您最近一年使用:0次
2023-10-27更新
|
262次组卷
|
3卷引用:河南省濮阳市2023-2024学年高二上学期9月月考化学试题
10 . 根据所学知识填写下列空白。
(1)在标准状况下,1.7g氨气与同条件下______ molH2S含有相同的氢原子数。
(2)在标准状况下,某气体的密度为2.86g•L-1,则其相对分子质量为______ (取整数值)。
(3)某气态氧化物化学式为R2O3,在标准状况下,1.52g该氧化物的体积是448mL,则R的摩尔质量为______ g•mol-1。
(4)将18.7gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体2.24L,所得溶液的体积为500mL,试计算:原混合物中Na2O的物质的量为______ mol。所得溶液中溶质的物质的量浓度为______ mol•L-1。
(5)现有含Na2SO4、MgSO4和NaNO3的混合溶液1L,已知其中c(Mg2+)=0.4mol•L-1,c(SO )=0.7mol•L-1, c(NO
)=0.7mol•L-1, c(NO )=0.2mol•L-1,则此溶液中c(Na+)为
)=0.2mol•L-1,则此溶液中c(Na+)为______ mol•L-1。
(1)在标准状况下,1.7g氨气与同条件下
(2)在标准状况下,某气体的密度为2.86g•L-1,则其相对分子质量为
(3)某气态氧化物化学式为R2O3,在标准状况下,1.52g该氧化物的体积是448mL,则R的摩尔质量为
(4)将18.7gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体2.24L,所得溶液的体积为500mL,试计算:原混合物中Na2O的物质的量为
(5)现有含Na2SO4、MgSO4和NaNO3的混合溶液1L,已知其中c(Mg2+)=0.4mol•L-1,c(SO
 )=0.7mol•L-1, c(NO
)=0.7mol•L-1, c(NO )=0.2mol•L-1,则此溶液中c(Na+)为
)=0.2mol•L-1,则此溶液中c(Na+)为
您最近一年使用:0次



