名校
1 . 请根据相关要求回答下列问题。
(1)标准状况下,2.4 g CH4分子与___________ L NH3气体含有的氢原子个数相同。
(2)等质量的O3和O2所含原子个数比为___________ 。
(3)等温等压下,等体积的O2和O3质量比为___________ 。
(4)0.9g水中含有的电子数为___________ NA。
(5)12.4g Na2R含0.4mol Na+,则Na2R的摩尔质量为___________ g·mol-1,R的相对原子质量为___________ 。
(6)100mL 0.2 mol·L-1 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为________ mol·L-1。
(1)标准状况下,2.4 g CH4分子与
(2)等质量的O3和O2所含原子个数比为
(3)等温等压下,等体积的O2和O3质量比为
(4)0.9g水中含有的电子数为
(5)12.4g Na2R含0.4mol Na+,则Na2R的摩尔质量为
(6)100mL 0.2 mol·L-1
 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解题方法
2 . 计算题(写计算过程)
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量______ ?(写出计算过程,下同)
(2)反应后ZnCl2的物质的量浓度______ ?
(3)生成H2的体积(标准状况)_______ ?
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为_______ ?
(5)用该浓盐酸配制250mL1.0mol L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是________ ?
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量
(2)反应后ZnCl2的物质的量浓度
(3)生成H2的体积(标准状况)
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为
(5)用该浓盐酸配制250mL1.0mol
 L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是
您最近一年使用:0次
3 . 化学计量在化学中占有重要地位,回答下列问题:
(1)0.2 molSO2的质量是______________ g,在标准状况下的体积约为_______________ L。
(2)将4.0 gNaOH固体溶于水配成100mL溶液,
①该溶液中NaOH的物质的量浓度为_________________ 。
②从该溶液中取出10mL,其中NaOH的物质的量浓度为________________ ,含NaOH的质量为________________ 。
(3)配制100mL0.5mol L-1氯化钠溶液,需要2.0mol
L-1氯化钠溶液,需要2.0mol L-1的氯化钠溶液的体积是
L-1的氯化钠溶液的体积是________________ mL。
(4)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是________________ 。
(5)含0.4 molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是________________ 。
(6)0.2 molNH3与________________ gH2O具有相同的氢原子数。
(1)0.2 molSO2的质量是
(2)将4.0 gNaOH固体溶于水配成100mL溶液,
①该溶液中NaOH的物质的量浓度为
②从该溶液中取出10mL,其中NaOH的物质的量浓度为
(3)配制100mL0.5mol
 L-1氯化钠溶液,需要2.0mol
L-1氯化钠溶液,需要2.0mol L-1的氯化钠溶液的体积是
L-1的氯化钠溶液的体积是(4)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是
(5)含0.4 molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(6)0.2 molNH3与
您最近一年使用:0次
2023-12-12更新
|
138次组卷
|
2卷引用:宁夏吴忠市青铜峡市2023-2024学年高一上学期12月月考化学试题
4 . 填空:
(1)2molSO3和3molSO2的分子数之比为___________ ,原子数之比___________ ;某氯化物(MC12)的质量为19g,含有0.4molCl-,则M的摩尔质量为___________ 。
(2)标准状况下,N2和O2组成的混合气体0.5mol,其体积为___________ ;常温常压下,相同体积的CH4和NH3质量之比为___________ ,质子数之比为___________ 。
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的分子数之比是___________ 。
(1)2molSO3和3molSO2的分子数之比为
(2)标准状况下,N2和O2组成的混合气体0.5mol,其体积为
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的分子数之比是
您最近一年使用:0次
名校
5 . 按要求解答问题。
(1)已知标准状况下,气体A的密度为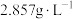 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为___________ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为___________ 。
(3)相同条件下,体积比为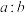 和质量比为
和质量比为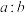 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是___________ 和___________ 。
(4)在标准状况下,将
 气体溶于
气体溶于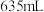 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:
①所得盐酸的质量分数和物质的量浓度分别是___________ 、___________ 。
②取这种盐酸 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度___________ 。
③在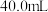

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过___________ mL。
(1)已知标准状况下,气体A的密度为
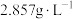 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入
 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为(3)相同条件下,体积比为
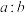 和质量比为
和质量比为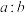 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是(4)在标准状况下,将

 气体溶于
气体溶于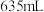 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:①所得盐酸的质量分数和物质的量浓度分别是
②取这种盐酸
 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度③在
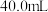

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过
您最近一年使用:0次
名校
解题方法
6 . 按要求回答问题。
(1)NaH能与水剧烈反应生成氢气,生成的 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目___________ 。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为___________  ,该样品中含杂质碳
,该样品中含杂质碳___________ g。
(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于___________ g,消耗NaOH溶液的体积是___________ mL。
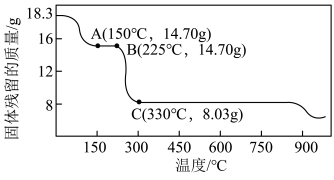
(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴( )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为___________ (填化学式),取C点固体用足量的浓盐酸完全溶解可得到黄绿色气体,写出以上反应的离子反应方程式___________ 。
(1)NaH能与水剧烈反应生成氢气,生成的
 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的
 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为 ,该样品中含杂质碳
,该样品中含杂质碳(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的
 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴(
 )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
您最近一年使用:0次
名校
解题方法
7 . 按照要求填空:
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是___________ ,属于强电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为___________ ;它与盐酸反应的化学方程式为___________ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是___________ 。
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)19.6克硫酸中含有___________ 个原子,将其溶于水配成500mL溶液则溶液的物质的量浓度为___________ ,从中取出100mL可以消耗1mol/L的NaOH溶液___________ mL。
(6)物质的量相等的SO2和SO3,其质量之比为________ ,所含原子数之比为________ ,所含质子数之比为________ ,质量相等的SO2和SO3,所含氧原子数之比为___________ 。
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为___________ 。36g 中质子数为
中质子数为___________ ,电子数为___________ (用NA表示)。
(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是___________ ,混合气体的平均摩尔质量为___________ ,混合气体中CO2在标准状况下的体积是___________ ,混合气体在标准状况下的密度是___________ ,该混合气体对氢气的相对密度为___________ 。
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)19.6克硫酸中含有
(6)物质的量相等的SO2和SO3,其质量之比为
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为
 中质子数为
中质子数为(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是
您最近一年使用:0次
名校
解题方法
8 . 计算:
(1)实验室欲配制0.1mol·L-1CuSO4溶液500mL,应用托盘天平称取CuSO4的质量是_______ 克。
(2)取200mL上述溶液加入铁粉,若恰好完全反应,则需要铁粉的质量为_______ 。
(1)实验室欲配制0.1mol·L-1CuSO4溶液500mL,应用托盘天平称取CuSO4的质量是
(2)取200mL上述溶液加入铁粉,若恰好完全反应,则需要铁粉的质量为
您最近一年使用:0次
名校
解题方法
9 . 按要求进行计算。
(1)0.5mol C2H6O的质量是_______ 克,与_______ g H2O分子中的氢的原子数目相同。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量_______ 。
(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为_______ L。
(4)某溶液中仅含有H+、Al3+、Cl-、 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是_______ mol·L-1。
(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为_______ 。
(1)0.5mol C2H6O的质量是
(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为
(4)某溶液中仅含有H+、Al3+、Cl-、
 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为
您最近一年使用:0次
名校
解题方法
10 . 回答下列小题
(1)25℃时,amol·L-1CH3COOH溶液中c(H+)=10-bmol·L-1,用含a和b的代数式表示CH3COOH的电离常数K=___________ 。
(2)已知25℃时,K(CH3COOH)=1.8×10-5,K(HSCN)=0.13。在该温度下将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如下,则反应前醋酸溶液中由水产生的氢离子浓度为:___________ ,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是___________ 。

(3)下表是几种弱酸常温下的电离常数:
①CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为___________ 。
②多元弱酸的二级电离程度远小于一级电离的主要原因是___________ (从电离平衡角度考虑)。
③同浓度的CH3COO-、 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为___________ 。
(1)25℃时,amol·L-1CH3COOH溶液中c(H+)=10-bmol·L-1,用含a和b的代数式表示CH3COOH的电离常数K=
(2)已知25℃时,K(CH3COOH)=1.8×10-5,K(HSCN)=0.13。在该温度下将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如下,则反应前醋酸溶液中由水产生的氢离子浓度为:

(3)下表是几种弱酸常温下的电离常数:
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
①CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为
②多元弱酸的二级电离程度远小于一级电离的主要原因是
③同浓度的CH3COO-、
 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为
您最近一年使用:0次



