解题方法
1 . 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:
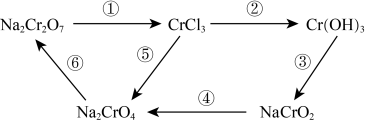
(1)Na2Cr2O7属于___________ (填序号)。
①酸 ②碱 ③盐 ④氧化物
(2)上述转化中,Cr元素化合价不变的步骤是___________ (填序号)。
(3)反应①为:Na2Cr2O7+HCl—NaCl+CrCl3+Cl2↑+H2O (未配平)。其中还原产物为___________ ,Na2Cr2O7与Cl2的计量系数比为___________ 。

(1)Na2Cr2O7属于
①酸 ②碱 ③盐 ④氧化物
(2)上述转化中,Cr元素化合价不变的步骤是
(3)反应①为:Na2Cr2O7+HCl—NaCl+CrCl3+Cl2↑+H2O (未配平)。其中还原产物为
您最近一年使用:0次
解题方法
2 . 生活离不开化学,家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①漂白粉;②NaClO;③Cl2;④Na2CO3;⑤小苏打(NaHCO3);⑥生铁;⑦甲烷。回答下列问题:
(1)漂白液的有效成分NaClO在水溶液的电离方程式:___________ 。
(2)厨卫用品的主要成分(括号内的物质):是电解质的有___________ (填序号,下同),是非电解质的有___________ 。
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为___________ g。
(4)实验室制Cl2的化学方程式___________ ,收集到33.6L(折算到标准状态)氯气时该反应总共转移的电子数___________ 。
(1)漂白液的有效成分NaClO在水溶液的电离方程式:
(2)厨卫用品的主要成分(括号内的物质):是电解质的有
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为
(4)实验室制Cl2的化学方程式
您最近一年使用:0次
3 . 回答下列问题。
(1)等质量的CO和 ,物质的量之比为
,物质的量之比为___________ ;氧原子个数之比为___________ ;
(2) 个氨分子含
个氨分子含___________ 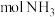 ,
,___________ g氮原子,___________ mol电子。
(3)含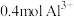 的
的 中所含的
中所含的 的质量是
的质量是___________ 。
(4)已知16g A和20g B恰好完全反应,生成0.04mol C和31.76g D,则C的摩尔质量为___________ 。
(1)等质量的CO和
 ,物质的量之比为
,物质的量之比为(2)
 个氨分子含
个氨分子含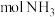 ,
,(3)含
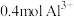 的
的 中所含的
中所含的 的质量是
的质量是(4)已知16g A和20g B恰好完全反应,生成0.04mol C和31.76g D,则C的摩尔质量为
您最近一年使用:0次
4 . CO和 是碳的两种重要氧化物。
是碳的两种重要氧化物。
(1)在标准状况下,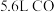 的物质的量是
的物质的量是______________ 。
(2)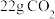 的体积是
的体积是___________ (标准状况)。
(3)相同物质的量的CO和 所含的原子个数比是
所含的原子个数比是___________ 。
(4)现有物质的量浓度为 的
的 溶液
溶液 ,求该溶液中
,求该溶液中 的物质的量为
的物质的量为__________ 。
 是碳的两种重要氧化物。
是碳的两种重要氧化物。(1)在标准状况下,
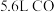 的物质的量是
的物质的量是(2)
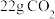 的体积是
的体积是(3)相同物质的量的CO和
 所含的原子个数比是
所含的原子个数比是(4)现有物质的量浓度为
 的
的 溶液
溶液 ,求该溶液中
,求该溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
5 . 按要求填空:
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与水反应的化学方程式___________ ,1molNa2O2参与反应,转移电子数为___________ (用NA表示阿伏加德罗常数)。
(2)氧化铝是两性氧化物,写出铝与氢氧化钠溶液反应的化学方程式___________ 。
(3)NaHCO3与NaOH反应的离子方程式为___________ 。
(4)在钢铁厂生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,否则会发生爆炸事故,用化学方程式解释其中的原因___________ 。
(5)向KI溶液中,滴加FeCl3溶液,溶液变棕黄色,写出反应的离子方程式___________ 。
(6)实验室配制FeSO4溶液时根据需要加入一定量H2SO4,久置的FeSO4溶液发黄,原因是酸性条件下被空气氧化,离子方程式为___________ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与水反应的化学方程式
(2)氧化铝是两性氧化物,写出铝与氢氧化钠溶液反应的化学方程式
(3)NaHCO3与NaOH反应的离子方程式为
(4)在钢铁厂生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,否则会发生爆炸事故,用化学方程式解释其中的原因
(5)向KI溶液中,滴加FeCl3溶液,溶液变棕黄色,写出反应的离子方程式
(6)实验室配制FeSO4溶液时根据需要加入一定量H2SO4,久置的FeSO4溶液发黄,原因是酸性条件下被空气氧化,离子方程式为
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①NO是___________ 产物(填“氧化”或“还原”)
②若反应中有64g铜溶解,则被还原的HNO3的质量为___________ 。
(2)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①氧化剂是___________ 。
②用单线桥标出电子转移方向和数目:_________
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(3)已知:2H2S+SO2=3S+2H2O
①若有4个H2S分子参加反应,电子转移的数目为___________ 。
②氧化产物与还原产物的质量比为___________ 。
(1)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①NO是
②若反应中有64g铜溶解,则被还原的HNO3的质量为
(2)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①氧化剂是
②用单线桥标出电子转移方向和数目:
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(3)已知:2H2S+SO2=3S+2H2O
①若有4个H2S分子参加反应,电子转移的数目为
②氧化产物与还原产物的质量比为
您最近一年使用:0次
名校
解题方法
7 . 某兴趣小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

(1)向饱和NaCl溶液中通入 和氨气时,应先通入
和氨气时,应先通入___________ (填化学式)。操作①的名称为___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)该流程中可循环利用的物质是___________ (填化学式)。
(4)现将 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)下列选项中哪种方法可以鉴别 溶液和
溶液和 溶液___________。
溶液___________。
(6)下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。

(1)向饱和NaCl溶液中通入
 和氨气时,应先通入
和氨气时,应先通入(2)写出反应①的化学方程式:
(3)该流程中可循环利用的物质是
(4)现将
 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(5)下列选项中哪种方法可以鉴别
 溶液和
溶液和 溶液___________。
溶液___________。| A.加入澄清石灰水 | B.加入氢氧化钠溶液 |
| C.加热 | D.逐滴加入稀盐酸 |
(6)下列实验方案中,不能测定出
 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。
| A.Li、Na、K的原子半径和密度都随原子序数的增加而增大 |
B.碱性: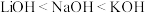 |
C.还原性: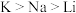 ,故K可以从NaCl溶液中置换出金属钠 ,故K可以从NaCl溶液中置换出金属钠 |
D.熔、沸点: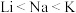 |
您最近一年使用:0次
2023-12-23更新
|
145次组卷
|
3卷引用:湖南省长沙市南雅中学2023-2024学年高一上学期第三次12月月考化学试卷
解题方法
8 . NA为阿伏加德罗常数,如需要用NA表示:
(1)1.204×1024个 的物质的量为
的物质的量为___________ ,含有的电子数为___________ ;
(2)同温同压下,体积相同的HCl、NH3、CO2气体中,质量最大的是___________ 。
(1)1.204×1024个
 的物质的量为
的物质的量为(2)同温同压下,体积相同的HCl、NH3、CO2气体中,质量最大的是
您最近一年使用:0次
解题方法
9 . 建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
(1)配平该方程式______ 。
NaNO2+HI=NO↑+I2+NaI+H2O
(2)配平该方程式______ 。
ClO-+Fe3++OH-=FeO +Cl-+H2O。
+Cl-+H2O。
(1)配平该方程式
NaNO2+HI=NO↑+I2+NaI+H2O
(2)配平该方程式
ClO-+Fe3++OH-=FeO
 +Cl-+H2O。
+Cl-+H2O。
您最近一年使用:0次
名校
解题方法
10 . 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。_______ 。硝酸所表现出的化学性质主要有_______
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是_______ g。
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则
①反应结束后的溶液中 、
、 的物质的量之比
的物质的量之比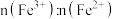 为
为_______ 。
②标准状况下,计算生成NO气体的体积_______ 。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。
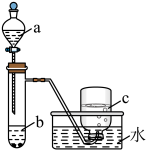
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol
 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则①反应结束后的溶液中
 、
、 的物质的量之比
的物质的量之比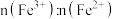 为
为②标准状况下,计算生成NO气体的体积
您最近一年使用:0次
2023-04-19更新
|
169次组卷
|
2卷引用:湖南省岳阳市岳汨联考2023-2024学年高二下学期5月月考化学试题



