名校
解题方法
1 . 请回答:
(1)①硫酸铁的化学式是___________ ;②水的电子式是___________ 。
(2)纯净的H2在Cl2中燃烧时,火焰呈___________ 色,并伴有白雾生成。
(3)金属Na与水反应的离子方程式___________ 。
(1)①硫酸铁的化学式是
(2)纯净的H2在Cl2中燃烧时,火焰呈
(3)金属Na与水反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题
(1)甲醇与氧气在氢氧化钾溶液中形成燃料电池,写出负极方程式_______ 。
(2)已知20℃下,饱和食盐水的质量分数为26.5%,密度为1.17 g/mL,则该饱和食盐水的物质的量浓度为_______ mol/L。
(3)向27.2 g由Fe和Fe2O3组成的固体混合物加入2L一定浓度的稀硫酸后固体恰好溶解,可收集到标准状况下气体2.24 L,再向反应后的溶液中滴入KSCN溶液,无明显现象。(忽略反应前后溶液的体积变化),反应后溶液中FeSO4的物质的量浓度为_______ 。
(4) 溶液与1.95g锌粉在量热计中充分反应。已知:反应
溶液与1.95g锌粉在量热计中充分反应。已知:反应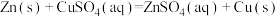 的
的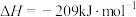 ,反应前后,溶液的比热容均近似为
,反应前后,溶液的比热容均近似为 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。实验测得反应前温度为20.1℃,请计算反应后测得的最高温度为
,忽略溶液体积、质量变化和金属吸收的热量。实验测得反应前温度为20.1℃,请计算反应后测得的最高温度为_______ ℃。
(1)甲醇与氧气在氢氧化钾溶液中形成燃料电池,写出负极方程式
(2)已知20℃下,饱和食盐水的质量分数为26.5%,密度为1.17 g/mL,则该饱和食盐水的物质的量浓度为
(3)向27.2 g由Fe和Fe2O3组成的固体混合物加入2L一定浓度的稀硫酸后固体恰好溶解,可收集到标准状况下气体2.24 L,再向反应后的溶液中滴入KSCN溶液,无明显现象。(忽略反应前后溶液的体积变化),反应后溶液中FeSO4的物质的量浓度为
(4)
 溶液与1.95g锌粉在量热计中充分反应。已知:反应
溶液与1.95g锌粉在量热计中充分反应。已知:反应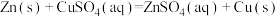 的
的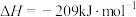 ,反应前后,溶液的比热容均近似为
,反应前后,溶液的比热容均近似为 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。实验测得反应前温度为20.1℃,请计算反应后测得的最高温度为
,忽略溶液体积、质量变化和金属吸收的热量。实验测得反应前温度为20.1℃,请计算反应后测得的最高温度为
您最近一年使用:0次
3 . 工业上用 为原料制
为原料制 可简化为如下两步反应:
可简化为如下两步反应:
第一步: (条件略);第二步:
(条件略);第二步: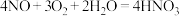 。
。
某同学用 与足量
与足量 和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气
和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气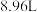 。请计算:
。请计算:
(1)消耗的 的物质的量为
的物质的量为___________  。
。
(2)整个过程转移电子的物质的量为___________  。
。
(3)理论上可获得质量分数为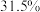 的硝酸(假设溶质不挥发)质量为
的硝酸(假设溶质不挥发)质量为___________  。
。
 为原料制
为原料制 可简化为如下两步反应:
可简化为如下两步反应:第一步:
 (条件略);第二步:
(条件略);第二步: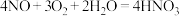 。
。某同学用
 与足量
与足量 和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气
和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气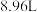 。请计算:
。请计算:(1)消耗的
 的物质的量为
的物质的量为 。
。(2)整个过程转移电子的物质的量为
 。
。(3)理论上可获得质量分数为
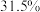 的硝酸(假设溶质不挥发)质量为
的硝酸(假设溶质不挥发)质量为 。
。
您最近一年使用:0次
4 . 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列转化制得。
(1)X的分子式是_______ 。
(2)Y中含氧官能团的名称是羟基和_______ 。
(3)Y→Z反应的反应类型是_______ 。
(4)乙醛与 反应的化学方程式是
反应的化学方程式是_______ 。

(1)X的分子式是
(2)Y中含氧官能团的名称是羟基和
(3)Y→Z反应的反应类型是
(4)乙醛与
 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
5 . 回答下列问题:
(1)① 的电子式是
的电子式是_______ ;②乙炔的结构简式是_______ 。
(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是_______ 。
(3) 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是_______ 。
(1)①
 的电子式是
的电子式是(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是
(3)
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是
您最近一年使用:0次
名校
6 . 按要求完成下列填空:
(1)漂白液有效成分的化学式______ ;Fe2O3的俗称为_______ 。
(2)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______ 。
(3)用FeCl3溶液可以制作铜制的印刷电路板,写出该反应的离子方程式______ 。
(1)漂白液有效成分的化学式
(2)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为
(3)用FeCl3溶液可以制作铜制的印刷电路板,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
7 . 化学反应中的能量变化通常表现为热量的变化,研究反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是______ (填序号)。
①液态水气化
②胆矾加热变成白色粉末
③灼热的木炭与CO2的反应
④甲烷在空气中燃烧的反应
⑤盐酸和碳酸氢钠反应
⑥氢氧化钾和稀硫酸反应
(2)已知:C(s)+ O2(g)=CO(g) ΔH1,C(s)+O2(g)=CO2(g) ΔH2,则ΔH1
O2(g)=CO(g) ΔH1,C(s)+O2(g)=CO2(g) ΔH2,则ΔH1______ ΔH2(填“>”、“<”或“=”)。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ•mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量
2SO3(g)ΔH=-196.6kJ•mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_______ (填字母)。
(4)在25℃、101kPa下,23g乙醇CH3CH2OH(l)完全燃烧生成CO2和液态水时放热638.4kJ。则表示乙醇燃烧的热化学方程式为_______ 。
(1)下列变化属于吸热反应的是
①液态水气化
②胆矾加热变成白色粉末
③灼热的木炭与CO2的反应
④甲烷在空气中燃烧的反应
⑤盐酸和碳酸氢钠反应
⑥氢氧化钾和稀硫酸反应
(2)已知:C(s)+
 O2(g)=CO(g) ΔH1,C(s)+O2(g)=CO2(g) ΔH2,则ΔH1
O2(g)=CO(g) ΔH1,C(s)+O2(g)=CO2(g) ΔH2,则ΔH1(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ•mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量
2SO3(g)ΔH=-196.6kJ•mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量| A.等于196.6kJ | B.98.3kJ~196.6kJ | C.等于98.3kJ | D.小于98.3kJ |
您最近一年使用:0次
解题方法
8 . 电子工业常用覆铜板为基础材料制作印刷电路板。现取一定质量的覆铜板,用油性笔画上设计好的图案,浸入盛有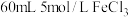 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:
(1) 的物质的量是
的物质的量是_______ mol。
(2)反应过程中,转移电子总数为_______  。
。
(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为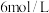 的
的 溶液
溶液_______ mL。
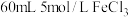 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:(1)
 的物质的量是
的物质的量是(2)反应过程中,转移电子总数为
 。
。(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为
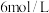 的
的 溶液
溶液
您最近一年使用:0次
解题方法
9 . 化学用语是化学专业语言,是学习化学的工具。请回答:
(1)H2S的电子式为___________ ;生产光导纤维的主要原料是为___________ 。
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为___________ 。
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①___________ ;②___________ 。
(1)H2S的电子式为
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①
您最近一年使用:0次
10 . 请回答:
(1)①氧化亚铜的化学式为___________ 。②水分子的电子式为___________ 。
(2)在坩埚中加热氢氧化铁,观察到固体的颜色由___________ 色变为___________ 色。
(3)蔗糖在稀酸催化下发生水解反应的化学方程式为___________ 。
(1)①氧化亚铜的化学式为
(2)在坩埚中加热氢氧化铁,观察到固体的颜色由
(3)蔗糖在稀酸催化下发生水解反应的化学方程式为
您最近一年使用:0次



