解题方法
1 . 某温度时,在2L容器中发生A、B两种气体间的转化反应,A、B物质的量随时间变化的曲线如图所示,M点的坐标为(7,0.24)请分析图中数据,回答下列问题。
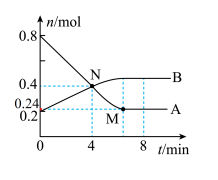
(1)该反应______ (填写“是”或“不是”)可逆反应。
(2)该化学方程式为______ 。
(3)反应从开始至4min时,用B的浓度变化来表示的反应速率为______ 。
(4)比较M、N两点该反应的正反应速率的相对大小v(M)正______ v(N)正(填写“>”、“<”或“=”)。
(5)运用图示数据计算该反应达到限度时A的转化率为______ %。

(1)该反应
(2)该化学方程式为
(3)反应从开始至4min时,用B的浓度变化来表示的反应速率为
(4)比较M、N两点该反应的正反应速率的相对大小v(M)正
(5)运用图示数据计算该反应达到限度时A的转化率为
您最近一年使用:0次
名校
2 . 计算
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为_______ 。
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为_______ 。
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为_______ 。
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为_______ 。
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
3 . 某食品膨松剂作用物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
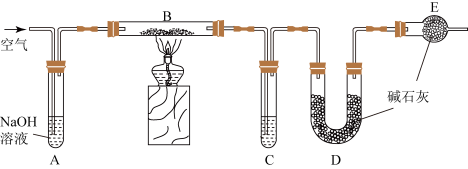
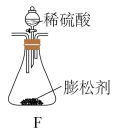
已知:碱石灰是固体氢氧化钠和氧化钙的混合物: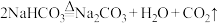 。
。
(1)A装置中 溶液的作用是除去空气中的
溶液的作用是除去空气中的________ ,C装置内所盛试剂是________ ,E装置的作用是________________________ ;
(2)若没有E装置,测定的结果________ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将________ (填“偏高”、“偏低”或“无影响”)。
(3)取a克 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是________ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。

已知:碱石灰是固体氢氧化钠和氧化钙的混合物:
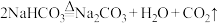 。
。(1)A装置中
 溶液的作用是除去空气中的
溶液的作用是除去空气中的(2)若没有E装置,测定的结果
(3)取a克
 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
您最近一年使用:0次
4 . 在密闭容器中,通入a mol N2和b mol H2,若在一定条件下反应达到平衡时,容器中剩余c mol N2。
(1)达到平衡时,生成NH3的物质的量为_______
(2)若把容器的容积减小到原来的一半,则正反应速率_______ (填“增大”“减小”或“不变”,下同),逆反应速率_______ ,N2的转化率_______ 。
(1)达到平衡时,生成NH3的物质的量为
(2)若把容器的容积减小到原来的一半,则正反应速率
您最近一年使用:0次
名校
5 . 完成下列问题
(1)常温下,某溶液由水电离出的c(H+)=10-12 mol·L-1,则该溶液的pH为_______ 。
(2)某温度下,纯水中c(H+)=5.0×10-7 mol·L-1,则该温度下的KW=_______ ,若温度不变,0.005 mol·L-1的H2SO4溶液中,由水电离出的c(H+)=_______ 。
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:该温度下水的Kw=_______ ;此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va:Vb=_______ 。
(4)25℃时,将0.1mol·L-1 NaOH溶液与0.06mol·L-1的H2SO4溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为_______ 。
(5)将pH=5的H2SO4稀释1000倍后,c(H+):c(SO )约为
)约为_______ 。
(1)常温下,某溶液由水电离出的c(H+)=10-12 mol·L-1,则该溶液的pH为
(2)某温度下,纯水中c(H+)=5.0×10-7 mol·L-1,则该温度下的KW=
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:该温度下水的Kw=
(4)25℃时,将0.1mol·L-1 NaOH溶液与0.06mol·L-1的H2SO4溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为
(5)将pH=5的H2SO4稀释1000倍后,c(H+):c(SO
 )约为
)约为
您最近一年使用:0次
2023-03-04更新
|
600次组卷
|
2卷引用:广东省湛江市第二十一中学2022-2023学年高二上学期期中考试化学试题
名校
6 . 完成下列问题
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积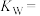
_______ ;该温度下, 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显_______ 性。

(2)已知室温下, 的电离常数
的电离常数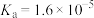 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为_______ 。向其中加入少量 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH_______ (填“增大”、“减小”或“不变”)。
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积
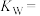
 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显
(2)已知室温下,
 的电离常数
的电离常数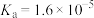 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH
您最近一年使用:0次
名校
解题方法
7 . 将某碳酸钠和碳酸氢钠混合物2.43g加热到质量不再变化时,剩余物质的质量为2.12g,求:
(1)写出加热过程中发生反应的化学方程式_______ 。
(2)碳酸氢钠的质量为_______ 克?
(3)碳酸钠的质量分数为_______ (保留三位有效数字)?
(1)写出加热过程中发生反应的化学方程式
(2)碳酸氢钠的质量为
(3)碳酸钠的质量分数为
您最近一年使用:0次
2022-11-19更新
|
292次组卷
|
3卷引用:广东省汕尾华大实验学校2022-2023学年高一上学期12月月考化学试题
解题方法
8 . 2020 年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式___________ ;
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8 g KMnO4能和_____ mol HCl发生上述反应、产生的Cl2在标准状况下的体积为___________ L;
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为___________ mol;
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:___________ ;
(1)①写出实验室中制取氯气的离子方程式
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8 g KMnO4能和
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:
您最近一年使用:0次
9 . 燃烧法是测定有机化合物分子式的一种方法,准确称取某有机物样品3.0g完全燃烧,产物依次通过浓硫酸、浓碱溶液,实验结束后,称得浓硫酸质量增加1.8g,浓碱溶液质量增加4.4g。
(1)求该有机物的实验式为_______ 。
(2)若有机物相对氢气的密度为30,该有机物的核磁共振氢谱如下图所示,且该有机物能与 溶液反应产生气体,则其结构简式为
溶液反应产生气体,则其结构简式为_______ ;

(3)若该有机物既能与Na反应产生气体,又能发生银镜反应,则结构简式为_______ 。
(1)求该有机物的实验式为
(2)若有机物相对氢气的密度为30,该有机物的核磁共振氢谱如下图所示,且该有机物能与
 溶液反应产生气体,则其结构简式为
溶液反应产生气体,则其结构简式为
(3)若该有机物既能与Na反应产生气体,又能发生银镜反应,则结构简式为
您最近一年使用:0次
2022-03-18更新
|
542次组卷
|
4卷引用:广东省茂名市电白区水东中学2021-2022学年高二下学期3月测试化学试题
10 . 回答下列问题:
(1)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为_______ mol,其中CO2为_______ mol,CO占总体积的_______ ,混合气体的摩尔质量为_______ 。
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,所含分子数之比为_______ ,物质的量之比为_______ ,原子数之比为_______ ,质量之比为_______ ,密度之比为_______ 。
(3)在标准状况下,4gH2、11.2LO2、1molH2O中,所含分子数最多的是_______ ,原子数最多的是_______ ,质量最大的是_______ ,体积最小的是_______ 。
(1)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,所含分子数之比为
(3)在标准状况下,4gH2、11.2LO2、1molH2O中,所含分子数最多的是
您最近一年使用:0次
2022-03-17更新
|
497次组卷
|
2卷引用:广东深圳市第二高级中学2022-2023学年高一上学期10月测试化学试题



