名校
解题方法
1 . 化学计量在化学中占有重要地位。请回答下列问题:
(1)长征系列运载火箭的燃料之一是肼( )。回答下列问题:肼的摩尔质量是
)。回答下列问题:肼的摩尔质量是____________ ,16g肼中含有氮原子的数目为________ 。
(2)22.2g某二价金属氯化物( )中含有0.4mol
)中含有0.4mol  ,则
,则 的物质的量是
的物质的量是____________ ;A的相对原子质量是____________ 。
(3)现有0.4mol的CO和 的混合气体,质量共12.8g,则
的混合气体,质量共12.8g,则 的质量为
的质量为____________ 。
(1)长征系列运载火箭的燃料之一是肼(
 )。回答下列问题:肼的摩尔质量是
)。回答下列问题:肼的摩尔质量是(2)22.2g某二价金属氯化物(
 )中含有0.4mol
)中含有0.4mol  ,则
,则 的物质的量是
的物质的量是(3)现有0.4mol的CO和
 的混合气体,质量共12.8g,则
的混合气体,质量共12.8g,则 的质量为
的质量为
您最近一年使用:0次
2 . 一氧化氮可用作人造丝的漂白剂及丙烯和二甲醚的安定剂。一定温度下,在2L恒容密闭容器中充入1molNO、1mol ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。
(1)平衡时,体系压强p=___________ MPa。
(2)平衡时,
___________ 。
(3)该反应平衡常数表达式为___________ ,该温度下时,平衡常数K=___________ 。
 ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。(1)平衡时,体系压强p=
(2)平衡时,

(3)该反应平衡常数表达式为
您最近一年使用:0次
名校
3 . 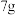 粗锌放在烧杯中,加入
粗锌放在烧杯中,加入 稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为
稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为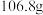 ,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)___________ 。
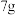 粗锌放在烧杯中,加入
粗锌放在烧杯中,加入 稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为
稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为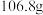 ,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
您最近一年使用:0次
解题方法
4 . I.某双原子分子构成的气体,其摩尔质量为Mg/mol,该气体的质量为mg。设阿伏加德罗常数的值为 ,则:
,则:
(1)该气体在标准状况下的体积为_______ L;
(2)该气体在标准状况下的密度为_______ g/L;
(3)该气体所含的原子总数为_______ ;
(4)一个该气体分子的质量为_______ g;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_______  。
。
II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是_______ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______ 。
A. B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
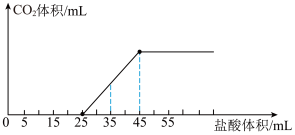
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为_______ 。
 ,则:
,则:(1)该气体在标准状况下的体积为
(2)该气体在标准状况下的密度为
(3)该气体所含的原子总数为
(4)一个该气体分子的质量为
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
 。
。II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是
A.
 B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的
 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
您最近一年使用:0次
解题方法
5 . (Ⅰ)把15.6gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2在标准状况的体积___________ mL;
(2)反应后所得NaOH的物质的量浓度___________ 。(反应前后溶液体积变化忽略不计)。
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象____________ 。
(4)则原混合物中Fe2O3与Fe的物质的量之比为___________ 。
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为_______ L(标准状况)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象
(4)则原混合物中Fe2O3与Fe的物质的量之比为
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为
您最近一年使用:0次
名校
解题方法
6 . 填空。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①
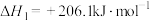
②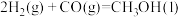
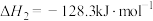
③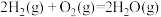
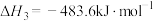
写出由甲烷和氧气合成液态甲醇的热化学方程式:_______ 。
(2)已知: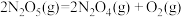
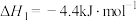
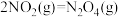
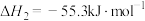
则反应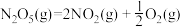 的△H=
的△H=_______ kJ∙mol-1。
(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是_______ 。
(4)实验室现欲用质量分数为98%,密度为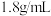 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为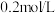 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是_______ mL。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①

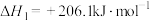
②
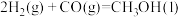
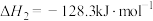
③
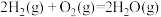
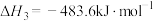
写出由甲烷和氧气合成液态甲醇的热化学方程式:
(2)已知:
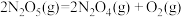
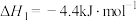
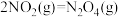
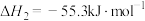
则反应
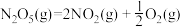 的△H=
的△H=(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是
(4)实验室现欲用质量分数为98%,密度为
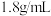 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为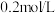 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是_______ 。
(2)下列所给出的几组物质中:标准状况下体积最大的是_______ ;质量最大的是_______ 。(填序号)
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______ mol,具有相同氧原子数的硫酸分子有_______ 个。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)已知一混合溶液中有Na+、Cl-、SO 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为 _______ 。
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是
(2)下列所给出的几组物质中:标准状况下体积最大的是
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)已知一混合溶液中有Na+、Cl-、SO
 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
您最近一年使用:0次
2022-10-30更新
|
275次组卷
|
2卷引用:安徽省淮北市第一中学2022-2023学年高一上学期期中考试化学试题
名校
8 . 完成下列问题
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)_______ 25℃,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
①若所得混合溶液为中性,则a:b=_______ ;
②若所得混合溶液pH=2, 则 a:b=_______ 。
(2)在一定温度下,有a.醋酸 b.盐酸 c.硫酸 三种酸:
①同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小 的顺序是_______ ;(用a、b、c表示,下同)
②若三者c(H+)相同时,酸的物质的量浓度由大到小 的顺序为_______ ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小 的顺序是_______ 。
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)
①若所得混合溶液为中性,则a:b=
②若所得混合溶液pH=2, 则 a:b=
(2)在一定温度下,有a.醋酸 b.盐酸 c.硫酸 三种酸:
①同体积、同物质的量浓度的三种酸,中和NaOH的能力
②若三者c(H+)相同时,酸的物质的量浓度
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)
您最近一年使用:0次
2022-10-28更新
|
575次组卷
|
3卷引用:安徽省合肥庐巢八校2022-2023学年高二上学期12月联考化学试题
9 . 化学计量是研究化学的重要工具。回答下列有关问题:
(1)28g氮气中含有的原子数约为_______ 个,标准状况下的体积为_______ L。
(2)7.8g 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为_______ mol。
(3)在含有 、
、 、
、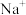 、
、 、
、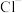 的溶液中,
的溶液中, ,若
,若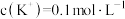 ,则
,则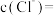
_______  。
。
(4)某气体纯净物在标准状况下的密度为1.25 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是_______ 。
(5)27g某二价金属氯化物中含有0.4mol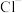 ,则该物质的化学式为
,则该物质的化学式为_______ 。
(6)标准状况下,由CO与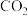 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中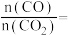
_______ (用含 的分式表示,不需要化简)。
的分式表示,不需要化简)。
(1)28g氮气中含有的原子数约为
(2)7.8g
 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为(3)在含有
 、
、 、
、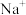 、
、 、
、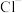 的溶液中,
的溶液中, ,若
,若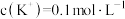 ,则
,则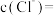
 。
。(4)某气体纯净物在标准状况下的密度为1.25
 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是(5)27g某二价金属氯化物中含有0.4mol
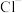 ,则该物质的化学式为
,则该物质的化学式为(6)标准状况下,由CO与
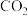 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中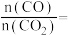
 的分式表示,不需要化简)。
的分式表示,不需要化简)。
您最近一年使用:0次
10 . 把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:_______ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次



