名校
解题方法
1 . 某稀硫酸和稀硝酸混合溶液100 mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示,求原混合溶液 和
和 的浓度
的浓度___________ 。(需在答题纸上写出计算过程)

 和
和 的浓度
的浓度
您最近一年使用:0次
21-22高一下·上海浦东新·期中
名校
解题方法
2 . Ⅰ.钠和铝是两种重要的金属,请回答下列问题:
(1)钠在空气中燃烧现象为___________ ,产物的电子式为___________ 。
(2)将一小块钠投入到下列溶液中,既能产生气体又会出现白色沉淀的是___________ (填字母)。
a.稀硫酸 b.硫酸铜溶液 c.饱和氯化钠溶液 d.氯化镁溶液
(3)将 的
的 与
与 的
的 同时投入到水中,充分反应,是否有金属剩余?
同时投入到水中,充分反应,是否有金属剩余?___________ ,得到的气体质量为___________ g。
Ⅱ.为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为 ,将质量为
,将质量为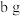 的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为
的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为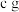 。
。
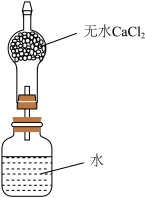
(4)列出计算钠相对原子质量的数学表达式___________ (用含有a、b、c的算式表示)。
(5)无水氯化钙的作用是___________ 。
(1)钠在空气中燃烧现象为
(2)将一小块钠投入到下列溶液中,既能产生气体又会出现白色沉淀的是
a.稀硫酸 b.硫酸铜溶液 c.饱和氯化钠溶液 d.氯化镁溶液
(3)将
 的
的 与
与 的
的 同时投入到水中,充分反应,是否有金属剩余?
同时投入到水中,充分反应,是否有金属剩余?Ⅱ.为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为
 ,将质量为
,将质量为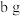 的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为
的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为 。
。
(4)列出计算钠相对原子质量的数学表达式
(5)无水氯化钙的作用是
您最近一年使用:0次
名校
3 . 在容器体积可变的密闭容器中,反应N2(g)+3H2(g)  2NH3(g)在一定条件下达到平衡。完成下列填空:
2NH3(g)在一定条件下达到平衡。完成下列填空:
(1)若该反应经过2秒钟后达到平衡,NH3的浓度增加了0.6mol/L,在此期间,正反应速率v(H2)=的值为_______。
(2)在其他条件不变的情况下,缩小容器体积以增大反应体系的压强,v正_______ (选填“增大”、“减小”,下同),v逆_______ ,平衡向_______ 方向移动(选填“正反应”、“逆反应”)。
(3)在其他条件不变的情况下,降低温度平衡向正反应方向移动,则正反应为_______ 反应(选填“吸热”、“放热”)。
(4)如图为反应速率(v)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是_______ (填写编号)。
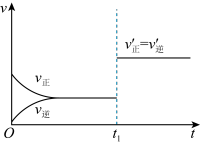
a. 增大N2的浓度 b. 扩大容器体积
c. 加入催化剂 d. 升高温度
改变条件后,平衡混合物中NH3的百分含量_______ (选填“增大”、“减小”、“不变”)。
(5)若达到平衡时,n(N2):n(H2):n(NH3)=2:2:1,保持温度不变,以2:2:1的物质的量之比再充入N2、H2、NH3,则_______。
 2NH3(g)在一定条件下达到平衡。完成下列填空:
2NH3(g)在一定条件下达到平衡。完成下列填空:(1)若该反应经过2秒钟后达到平衡,NH3的浓度增加了0.6mol/L,在此期间,正反应速率v(H2)=的值为_______。
| A.0.6mol/(L·s) | B.0.45mol/(L·s) | C.0.3mol/(L·s) | D.0.2mol/(L·s) |
(3)在其他条件不变的情况下,降低温度平衡向正反应方向移动,则正反应为
(4)如图为反应速率(v)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是

a. 增大N2的浓度 b. 扩大容器体积
c. 加入催化剂 d. 升高温度
改变条件后,平衡混合物中NH3的百分含量
(5)若达到平衡时,n(N2):n(H2):n(NH3)=2:2:1,保持温度不变,以2:2:1的物质的量之比再充入N2、H2、NH3,则_______。
| A.平衡向正反应方向移动 | B.平衡不移动 |
| C.平衡时,NH3的体积分数增大 | D.平衡时,NH3的体积分数可能减小 |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
4 . 某工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品。已知黄铁矿与氧气反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸_______ 吨(设生产过程中硫损失2%)。(提示:用关系式法或原子守恒法进行计算)
 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
名校
解题方法
5 . 向碘酸铜和碘化钾的混合溶液中加入硫酸酸化,也可以得到单质碘,其化学方程式为: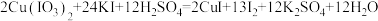
(1)该反应被氧化得到的碘与被还原得到的碘的质量之比为_____
(2)该反应中若有0.65mol单质碘生成,发生转移的电子数目为_______ 。
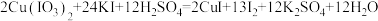
(1)该反应被氧化得到的碘与被还原得到的碘的质量之比为_____
| A.11:2 | B.2:11 | C.1:6 | D.6:1 |
您最近一年使用:0次
名校
6 . 完成下列问题
(1)质量为36g水所含质子的物质的量为_______ 。
(2)NA为阿伏加德罗常数,某气体中含分子数为b,则该气体在标准状况下的体积是_______ 。
(3)NA为阿伏加德罗常数,一个铝原子的质量约为_______ 克。
(1)质量为36g水所含质子的物质的量为
(2)NA为阿伏加德罗常数,某气体中含分子数为b,则该气体在标准状况下的体积是
(3)NA为阿伏加德罗常数,一个铝原子的质量约为
您最近一年使用:0次
7 . 回答下列问题
(1)在标准状况下2.24LCO与CO2混合气的总质量为3.7g,则混合气体中CO与CO2的分子数之比为_______
(2)甲烷(CH4)与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积之比为_______ 。
(3)某人的血糖化验单显示血液中葡萄糖(C6H12O6,M=180g/mol)为 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖_______ mg。
(1)在标准状况下2.24LCO与CO2混合气的总质量为3.7g,则混合气体中CO与CO2的分子数之比为
(2)甲烷(CH4)与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积之比为
(3)某人的血糖化验单显示血液中葡萄糖(C6H12O6,M=180g/mol)为
 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖
您最近一年使用:0次
名校
解题方法
8 . 2021年5月15日,“天问一号”携“祝融号”成功着陆火星,这是我国深空探测迈出的重要一步。回答以下问题:
(1)“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。工业上制取碳化硅的化学反应方程式为: ,请写出X的化学式
,请写出X的化学式___________ 。若生成4 g碳化硅,则其中含有___________ 个碳原子;生成4g碳化硅的同时,生成X气体的体积在标准状况下为___________ L。
(2)①火星大气主要成分是CO2。碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为___________ 。
②碳在自然界有两种稳定的同位素,有关数据如下表:
请列出碳元素近似相对原子质量的计算式___________ 。
(3)此次探测任务中,“祝融”号火星车利用了正十一烷(C11H24)储存能量。其原理是:白天火星温度___________ (选填“升高”或“降低),正十一烷吸热融化,储存能量;到了晚上反之释放能量。正十一烷在氧气中完全燃烧会生成两种氧化物,写出该燃烧反应的化学方程式___________ 。78 g正十一烷(C11H24)完全燃烧,需要氧气___________ mol。
(1)“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。工业上制取碳化硅的化学反应方程式为:
 ,请写出X的化学式
,请写出X的化学式(2)①火星大气主要成分是CO2。碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为
②碳在自然界有两种稳定的同位素,有关数据如下表:
| 同位素 | 相对原子质量 | 丰度(原子分数) |
| 2C | 12(整数,相对原子质量的基准) | 0.9893 |
| 13C | 13.003354826 | 0.0107 |
请列出碳元素近似相对原子质量的计算式
(3)此次探测任务中,“祝融”号火星车利用了正十一烷(C11H24)储存能量。其原理是:白天火星温度
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
9 . 298K时,向V升真空容器中通入n摩SO2和m摩H2S。
(1)若n=2,则当m=_______ 时,反应后容器内气体的密度最小。
(2)若2n>m,则反应后氧化产物与还原产物的质量差为_______ 克。
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=_______ 。
(1)若n=2,则当m=
(2)若2n>m,则反应后氧化产物与还原产物的质量差为
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=
您最近一年使用:0次
名校
10 . 某 无土栽培用的营养液中含有
无土栽培用的营养液中含有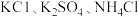 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:

(1)该营养液中 的物质的量浓度为
的物质的量浓度为________  ,含
,含 的质量为
的质量为______________ 。
(2)该营养液中 的物质的量为
的物质的量为__________________ 。
(3)将该营养液加水稀释,稀释过程中 的浓度
的浓度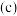 随溶液体积
随溶液体积 变化的曲线如图乙所示,则
变化的曲线如图乙所示,则
________________ 。
 无土栽培用的营养液中含有
无土栽培用的营养液中含有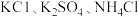 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
(1)该营养液中
 的物质的量浓度为
的物质的量浓度为 ,含
,含 的质量为
的质量为(2)该营养液中
 的物质的量为
的物质的量为(3)将该营养液加水稀释,稀释过程中
 的浓度
的浓度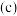 随溶液体积
随溶液体积 变化的曲线如图乙所示,则
变化的曲线如图乙所示,则
您最近一年使用:0次



