某工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品。已知黄铁矿与氧气反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸_______ 吨(设生产过程中硫损失2%)。(提示:用关系式法或原子守恒法进行计算)
 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2022高一·上海·专题练习 查看更多[1]
(已下线)3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
更新时间:2022-12-19 17:49:39
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】500mL某浓度的NaOH溶液恰好与标准状况下11.2LCO2完全反应生成正盐,则
①原溶液中NaOH的物质的量浓度为___________ ,
②若在原溶液中通入16.8L(标准状况下)CO2则生成的产物是__________________ 。
③若在②中的产物中加足量的盐酸,则需要盐酸的物质的量为_______________ 。
①原溶液中NaOH的物质的量浓度为
②若在原溶液中通入16.8L(标准状况下)CO2则生成的产物是
③若在②中的产物中加足量的盐酸,则需要盐酸的物质的量为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】汽车受到猛烈撞击时,气囊内的 会发生分解反应生成Na和
会发生分解反应生成Na和 ;
;
(1)写出上述气囊内的 发生反应的化学反应方程式:
发生反应的化学反应方程式:______ .
(2)能保护司机不受伤害的某气囊需要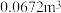 (已折算到标准状况下)的
(已折算到标准状况下)的 ,列式计算该气囊中需要装入
,列式计算该气囊中需要装入 的质量
的质量____ (写出计算过程)
 会发生分解反应生成Na和
会发生分解反应生成Na和 ;
;(1)写出上述气囊内的
 发生反应的化学反应方程式:
发生反应的化学反应方程式:(2)能保护司机不受伤害的某气囊需要
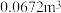 (已折算到标准状况下)的
(已折算到标准状况下)的 ,列式计算该气囊中需要装入
,列式计算该气囊中需要装入 的质量
的质量
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】把1L 1.0mol/L 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
(1)溶液混合前 的物质的量是
的物质的量是___________ mol。
(2)反应后 的物质的量浓度是
的物质的量浓度是___________ mol/L。
(3)反应中消耗铁粉的质量是___________ g。
 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:(1)溶液混合前
 的物质的量是
的物质的量是(2)反应后
 的物质的量浓度是
的物质的量浓度是(3)反应中消耗铁粉的质量是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】取1.06gNa2CO3溶于水配成100mL溶液,求:
(1)Na2CO3溶液的物质的量浓度_________ 。
(2)取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求稀释后溶液的体积______ 。
(3)取出20.0mL该溶液,向其中滴加足量1mol/L的稀硫酸,计算产生的CO2在标准状况下的体积__ 。
(1)Na2CO3溶液的物质的量浓度
(2)取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求稀释后溶液的体积
(3)取出20.0mL该溶液,向其中滴加足量1mol/L的稀硫酸,计算产生的CO2在标准状况下的体积
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】长征系列运载火箭的燃料之一是某液体化合物X2Y4。16gX2Y4在一定量的O2中恰好完全燃烧,反应的化学方程式为X2Y4(l)+O2(g)=X2(g)+2Y2O(l)。冷却后标准状况下测得生成物X2的体积为11.2L,其密度为1.25g·L-1,则:
(1)反应前O2的体积(标准状况下)为__ ,其物质的量为__ mol。
(2)X2的摩尔质量为__ ,Y元素的名称是__ 。
(3)若反应生成0.1molX2,则转移电子的物质的量为__ mol。
(1)反应前O2的体积(标准状况下)为
(2)X2的摩尔质量为
(3)若反应生成0.1molX2,则转移电子的物质的量为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】已知:2Fe3++2I-=2Fe2++I2、2Fe2++Br2=2Fe3++2Br-、2Br-+Cl2=Br2+2Cl-。
(1)含有1.5 mol FeI2和2 mol FeBr2的溶液中通入3 mol Cl2,此时被氧化的离子及其物质的量分别是__________________ 。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为________ (用含a、b的代数式表示)。
(1)含有1.5 mol FeI2和2 mol FeBr2的溶液中通入3 mol Cl2,此时被氧化的离子及其物质的量分别是
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】在加热条件下,6.4g铜与20mL 18mol/L硫酸(足量)反应,反应后稀释溶液至200mL。计算:
(1)生成气体的体积为_____ (标准状况下)
(2)被还原的硫酸的物质的量为_____
(3)反应后溶液中硫酸根离子的物质的量浓度为_____
(1)生成气体的体积为
(2)被还原的硫酸的物质的量为
(3)反应后溶液中硫酸根离子的物质的量浓度为
您最近一年使用:0次
【推荐2】已知锌跟浓硫酸反应生成SO2,跟稀硫酸反应生成H2。使一定量的锌与100mL18.5mol·L-1浓硫酸充分反应,锌完全溶解,同时收集到标准状况下的气体A33.6L。将反应后的溶液稀释到1L,测得溶液中氢离子的浓度为0.1mol·L-1。
(1)写出锌跟浓硫酸反应的化学方程式:____ 。
(2)反应过程中消耗的H2SO4的物质的量是____ 。
(3)气体A的成分是____ ,各成分的体积比是____ 。
(4)反应过程中消耗的锌的质量是____ 。
(1)写出锌跟浓硫酸反应的化学方程式:
(2)反应过程中消耗的H2SO4的物质的量是
(3)气体A的成分是
(4)反应过程中消耗的锌的质量是
您最近一年使用:0次