回收得到的SeO2的含量,可以通过下面的方法测定:①SeO2+KI+HNO3→Se+I2+KNO3+H2O(未配平)②I2+Na2S2O3→Na2S4O6+NaI(未配平)实验中,准确称量SeO2样品0.1500g,消耗0.2000mol·L-1的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为____ 。
21-22高一·全国·假期作业 查看更多[1]
(已下线)第11讲 氧化还原反应的应用和配平-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
更新时间:2022-06-25 22:42:56
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】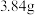 铜溶于
铜溶于 的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变)反应方程式为
的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变)反应方程式为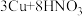 (稀)
(稀) 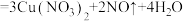 。计算下列问题:
。计算下列问题:
(1)产生气体的体积(标准状况下)______ ;
(2)生成的硝酸铜的物质的量浓度______ 。
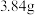 铜溶于
铜溶于 的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变)反应方程式为
的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变)反应方程式为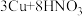 (稀)
(稀) 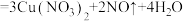 。计算下列问题:
。计算下列问题:(1)产生气体的体积(标准状况下)
(2)生成的硝酸铜的物质的量浓度
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】将5.6g铁粉与足量的稀盐酸充分反应,所得溶液的体积为10mL。试计算:
(1)生成氢气的体积______ (标准状况)。
(2)所得溶液中金属阳离子的物质的量浓度_______ 。(上述计算均要求写出计算过程)
(1)生成氢气的体积
(2)所得溶液中金属阳离子的物质的量浓度
您最近一年使用:0次
【推荐1】磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO 3Fe+4CO2,若有1.5molFe3O4参加反应,转移电子的物质的量是
3Fe+4CO2,若有1.5molFe3O4参加反应,转移电子的物质的量是_______ 。
 3Fe+4CO2,若有1.5molFe3O4参加反应,转移电子的物质的量是
3Fe+4CO2,若有1.5molFe3O4参加反应,转移电子的物质的量是
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】 铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为
铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为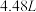 . 铜和硝酸反应的化学方程式为:
. 铜和硝酸反应的化学方程式为:
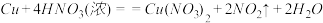
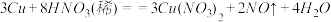
试计算:
(1)被还原的硝酸的物质的量
(2)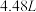 气体中各成分的物质的量
气体中各成分的物质的量
 铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为
铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为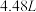 . 铜和硝酸反应的化学方程式为:
. 铜和硝酸反应的化学方程式为: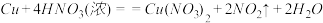
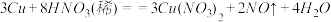
试计算:
(1)被还原的硝酸的物质的量
(2)
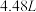 气体中各成分的物质的量
气体中各成分的物质的量
您最近一年使用:0次



