(Ⅰ)把15.6gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2在标准状况的体积___________ mL;
(2)反应后所得NaOH的物质的量浓度___________ 。(反应前后溶液体积变化忽略不计)。
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象____________ 。
(4)则原混合物中Fe2O3与Fe的物质的量之比为___________ 。
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为_______ L(标准状况)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象
(4)则原混合物中Fe2O3与Fe的物质的量之比为
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为
更新时间:2022-12-13 20:32:40
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将6.5g锌放入一定量稀硫酸中恰好完全反应,得到80mL密度为1.25g/mL的溶液。
试计算:
(1)生成标准状况下的H2的体积_______ ;
(2)所得溶液中硫酸锌的物质的量浓度_______ ;
(3)所用稀硫酸的质量分数_______ 。
试计算:
(1)生成标准状况下的H2的体积
(2)所得溶液中硫酸锌的物质的量浓度
(3)所用稀硫酸的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
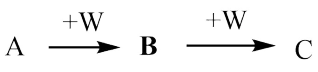
(1)若A为有刺激性气味的气体,其水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①实验室制取气体A的化学方程式_______ ;
②写出A→B的化学方程式为_______ ;
③将3.2g铜与60.0mL一定浓度D的溶液发生反应,铜完全溶解,产生B和C混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入100mL2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原D溶液的物质的量浓度为_______ mol/L。
(2)若A、B、C的溶液均显碱性,焰色试验均呈黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
①写出A溶液与C溶液反应的离子方程式_______ ;
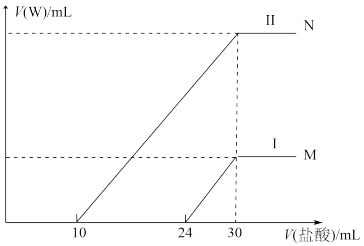
②向两份60mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25mol/L盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。则A溶液的物质的量浓度为_______ ,M、N两溶液中相同溶质的物质的量之比为_______ 。
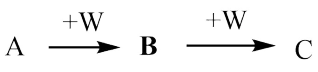
(1)若A为有刺激性气味的气体,其水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①实验室制取气体A的化学方程式
②写出A→B的化学方程式为
③将3.2g铜与60.0mL一定浓度D的溶液发生反应,铜完全溶解,产生B和C混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入100mL2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原D溶液的物质的量浓度为
(2)若A、B、C的溶液均显碱性,焰色试验均呈黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
①写出A溶液与C溶液反应的离子方程式

②向两份60mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25mol/L盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。则A溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)8gCH4中含___________ mol分子,含___________ 个原子。
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2物质的量之比是___________ 混合气体的平均相对分子质量为___________
(3) ,其中还原产物是
,其中还原产物是___________ (填化学式)
(4)用1000g溶剂中所含溶质的物质的量来表示的溶液浓度叫质量物质的量浓度,其单位是mol/kg.5mol/kg的硫酸的密度是1.29g/cm3,则其物质的量浓度是___________ (填序号)
A.3.56mol/L B.4.33mol/L C.5.00mol/L D.5.23mol/L
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2物质的量之比是
(3)
 ,其中还原产物是
,其中还原产物是(4)用1000g溶剂中所含溶质的物质的量来表示的溶液浓度叫质量物质的量浓度,其单位是mol/kg.5mol/kg的硫酸的密度是1.29g/cm3,则其物质的量浓度是
A.3.56mol/L B.4.33mol/L C.5.00mol/L D.5.23mol/L
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】硫酸和盐酸组成的混合液100 mL,与3.42g氢氧化钡粉末恰好完全反应后溶液呈中性。反应后经过滤、洗涤、干燥,得到沉淀2.33g。则分别计算原混合液中硫酸的物质的量的浓度_____________ 和盐酸的物质的量的浓度_____________ 。(设溶液总体积始终不变)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
(1)该盐酸的物质的量浓度____________ ;
(2)合金中Mg、Al的物质的量之比为___________ ;
(3)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为AlO2-,并使Mg2+刚好沉淀完全,则溶液中AlO2-的物质的量为__________ mol;溶液中Na+的物质的量为_________ mol;所加NaOH溶液的体积为_________ mL。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 0.255 | 0.385 | 0.459 |
| 生成气体/ml | 280 | 336 | 336 |
(1)该盐酸的物质的量浓度
(2)合金中Mg、Al的物质的量之比为
(3)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为AlO2-,并使Mg2+刚好沉淀完全,则溶液中AlO2-的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】钠及其化合物有非常重要的用途。
(1)钠的化学性质非常活泼。画出钠的原子结构示意图________ 。
钠与水反应的实验过程如图①、②、③所示。
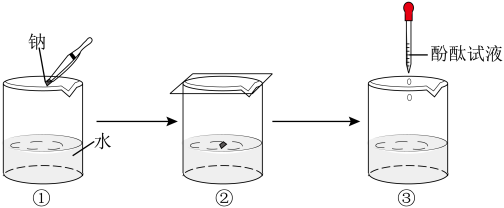
①将图②中的现象与解释用直线连接起来。_________
实验现象 解释
钠熔成小球 产生了气体
钠四处游动,嘶嘶作响 钠的密度比水小
钠浮在水面上 钠与水反应放热且钠的熔点低
②在③中酚酞变红,说明溶液呈_______ (填“酸”或“碱”或“中”)性。
③钠与水反应的化学方程式是_________ 。
(2)过氧化钠可在潜水艇中作为氧气的来源。写出过氧化钠与水反应的化学方程式___ ,与二氧化碳反应的化学方程式___ 。
(3)为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验:
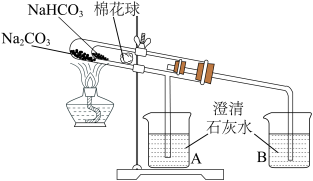
加热一段时间后,________ (填“A”或“B”)中澄清石灰水变浑浊,写出澄清石灰水变浑浊的离子方程式:________ 。写出试管中发生反应的化学方程式________ 。
(4)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。含有氮元素、钾元素、磷元素的某些盐可以作为化肥。
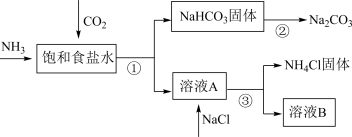
①联合制碱法所制得的“碱”是指_______ (填化学式)。
②在①-③所涉及的操作方法中,包含过滤的是_______ (填序号)。
③根据图,将化学方程式补充完整:NH3+CO2+___ +___ =NaHCO3↓+NH4Cl
④NaHCO3溶于水电离的方程式___ 。
⑤下列说法中,正确的是___ (填字母)
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH4+、Cl-
(1)钠的化学性质非常活泼。画出钠的原子结构示意图
钠与水反应的实验过程如图①、②、③所示。

①将图②中的现象与解释用直线连接起来。
实验现象 解释
钠熔成小球 产生了气体
钠四处游动,嘶嘶作响 钠的密度比水小
钠浮在水面上 钠与水反应放热且钠的熔点低
②在③中酚酞变红,说明溶液呈
③钠与水反应的化学方程式是
(2)过氧化钠可在潜水艇中作为氧气的来源。写出过氧化钠与水反应的化学方程式
(3)为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验:

加热一段时间后,
(4)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。含有氮元素、钾元素、磷元素的某些盐可以作为化肥。

①联合制碱法所制得的“碱”是指
②在①-③所涉及的操作方法中,包含过滤的是
③根据图,将化学方程式补充完整:NH3+CO2+
④NaHCO3溶于水电离的方程式
⑤下列说法中,正确的是
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH4+、Cl-
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列空格:
(1)4.9 g硫酸的物质的量___________ mol;标准状况下,3.612×1023个氯气分子的物质的量为___________ mol。
(2)一定量的铜片与200 mL18 mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为___________ mol。
(3)7.8 g Na2O2投入200 mL水中,充分反应。
①该反应的化学方程式为___________ 。
②反应后溶液中溶质的物质的量浓度为___________ mol/L。(忽略反应前后溶液体积变化)
(1)4.9 g硫酸的物质的量
(2)一定量的铜片与200 mL18 mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为
(3)7.8 g Na2O2投入200 mL水中,充分反应。
①该反应的化学方程式为
②反应后溶液中溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将2.88gCu与Fe2O3的混合物加入40.0 mL2.00 mol/L的稀硫酸中,充分反应后剩余固体的质量为0.640 g。继续往溶液中加入一定质量的铁粉,溶液质量增加了1.54 g,请计算:
(1)混合物中Cu与Fe2O3物质的量之比为_______ 。
(2)继续加入铁粉的质量为_______ 。
(1)混合物中Cu与Fe2O3物质的量之比为
(2)继续加入铁粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】向铁和氧化铁的固体混合物中加入500mL0.30mol·L-1稀盐酸后固体完全溶解,盐酸恰好完全反应,得到浅绿色溶液(只含一种金属阳离子),并收集到气体672mL(标准状况下测定),回答下列问题:
(1)实验室欲用浓度为10.0mol·L-1的浓盐酸配制500mL0.30mol·L-1的稀盐酸,则需要量取上述浓盐酸_______ mL。
(2)原混合物中氧化铁的质量为______ g。
(1)实验室欲用浓度为10.0mol·L-1的浓盐酸配制500mL0.30mol·L-1的稀盐酸,则需要量取上述浓盐酸
(2)原混合物中氧化铁的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】“孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近一年使用:0次

 )和浓盐酸混合加热能制取氯气:
)和浓盐酸混合加热能制取氯气: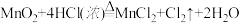 。现将
。现将 含
含 浓盐酸完全反应(杂质不参加反应)。
浓盐酸完全反应(杂质不参加反应)。
 的体积(标准状况)
的体积(标准状况)
 的物质的量
的物质的量



