9-10高一下·河北唐山·期中
名校
解题方法
1 . 在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A+2B=3C。反应经2min后,A的浓度从开始时的1.0mol·L-1降到0.8mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。
(1)2min末B、C的浓度____ 。
(2)用A表示该反应2min内的平均速率____ 。
(1)2min末B、C的浓度
(2)用A表示该反应2min内的平均速率
您最近一年使用:0次
2022-02-10更新
|
755次组卷
|
7卷引用:2011-2012学年广东省梅州市曾宪梓中学高一5月月考化学试卷
(已下线)2011-2012学年广东省梅州市曾宪梓中学高一5月月考化学试卷(已下线)2009---2010学年唐山二中高一第二学期期中化学试卷陕西省西安中学2019-2020学年高一下学期期中考试(平行班)化学试题(已下线)6.1.1 化学反应速率-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第二册)江苏省扬州市江都区邵伯高级中学2020-2021学年高一下学期期中考试化学试题苏教2020版化学必修第二册专题6第一单元 化学反应速率与反应限度课后习题福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷
解题方法
2 . 苯甲酸作为食品如香肠、蕃茄酱、芥末、其他调味剂,和黄油及其许多其他产品的防腐剂被广泛使用。苯甲酸能抑制霉菌、酵母和其他一些细菌的繁殖。苯甲酸对人体无害,其通过代谢为马尿酸被排出体外,因而不会在体内积累。越橘、野生黄莓等含有较多的苯甲酸。当pH低于5时,苯甲酸具有防腐效果。
(1)写出苯甲酸在水中的质子转移反应方程式_______ 。
(2)已知苯甲酸的Ka= 6.31 ×10-5。当苯甲酸的浓度c为0.012 mol·L-1时,计算该溶液的pH=_______ 。
(3)分别确定pH=4.00和pH=6.00的水果汁中苯甲酸离子与苯甲酸浓度的比值_______ 、_______ 。
(4)当pH=_______ 时苯甲酸溶液具有最佳的缓冲能力。
(5)将25 mL、浓度为0.0150 mol·L-1的苯甲酸溶液加到浓度为0.0120 mol·L-1的17 mL氢氧化钠溶液中,计算该混合溶液的pH=_______ 。
(1)写出苯甲酸在水中的质子转移反应方程式
(2)已知苯甲酸的Ka= 6.31 ×10-5。当苯甲酸的浓度c为0.012 mol·L-1时,计算该溶液的pH=
(3)分别确定pH=4.00和pH=6.00的水果汁中苯甲酸离子与苯甲酸浓度的比值
(4)当pH=
(5)将25 mL、浓度为0.0150 mol·L-1的苯甲酸溶液加到浓度为0.0120 mol·L-1的17 mL氢氧化钠溶液中,计算该混合溶液的pH=
您最近一年使用:0次
名校
解题方法
3 . (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H=___________ kJ·mol-1。
(2)已知H-H键键能(断裂时吸收或生成时释放的能量)为436kJ•mol﹣1,H-N键键能为391kJ•mol﹣1,根据热化学方程式:N2(g)+3H2(g) 2NH3(g) △H=﹣92.4kJ•mol﹣1.则N≡N键的键能是
2NH3(g) △H=﹣92.4kJ•mol﹣1.则N≡N键的键能是___________ kJ·mol-1。
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H=
(2)已知H-H键键能(断裂时吸收或生成时释放的能量)为436kJ•mol﹣1,H-N键键能为391kJ•mol﹣1,根据热化学方程式:N2(g)+3H2(g)
 2NH3(g) △H=﹣92.4kJ•mol﹣1.则N≡N键的键能是
2NH3(g) △H=﹣92.4kJ•mol﹣1.则N≡N键的键能是
您最近一年使用:0次
名校
解题方法
4 . 有氯化钠,碳酸钠,碳酸氢钠固体混合物共4克,加热到质量不再减少为止,此时剩余固体质量为3.38克,在残留的固体中加入足量盐酸,将产生的气体通过干燥管后,通入澄清石灰水中,生成2g固体。
(1)原混合物中碳酸氢钠的质量是多少?___
(2)标准状况下,加热时生成的气体的体积是多少?___
(3)原混合物中碳酸钠的质量是多少?___
(1)原混合物中碳酸氢钠的质量是多少?
(2)标准状况下,加热时生成的气体的体积是多少?
(3)原混合物中碳酸钠的质量是多少?
您最近一年使用:0次
名校
5 . 物质的量是高中化学中广泛应用的物理量,依据相关公式计算下列数值。
(1)含有6.02×1023个氧原子的H2SO4的物质的量是__ mol,质量是__ g。
(2)标准状况下11.2LCO2所含氧原子的数目是__ NA,与_ gH2O具有的氧原子数目相同。
(3)将5.4gAl放入氢氧化钠溶液中完全反应,生成气体体积__ L。
(1)含有6.02×1023个氧原子的H2SO4的物质的量是
(2)标准状况下11.2LCO2所含氧原子的数目是
(3)将5.4gAl放入氢氧化钠溶液中完全反应,生成气体体积
您最近一年使用:0次
解题方法
6 . 600mL 2mol/L的盐酸与足量的铝片完全反应。计算:
(1)参加反应的铝片的物质的量______
(2)生成H2的体积(标准状况)_______
(1)参加反应的铝片的物质的量
(2)生成H2的体积(标准状况)
您最近一年使用:0次
7 . 在一定温度下,将3molA和1molB两种气体相混合于1L的密闭容器中,发生以下反应: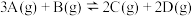 。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
(1)A的转化率为多少_______ ?
(2)求此温度下的平衡常数_______ ?
(3)求平衡时D的体积分数_______ (即物质的量分数)?
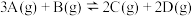 。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)(1)A的转化率为多少
(2)求此温度下的平衡常数
(3)求平衡时D的体积分数
您最近一年使用:0次
8 . 丙烷燃烧可以通过以下两种途径:
途径Ⅰ:
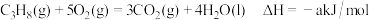
途径II:

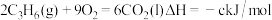
 (a、b、c、d均为正值)
(a、b、c、d均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量____________ 填“大于”、“等于”或“小于”)途径II放出的热量。
(2)在 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量___________ (填“大于”、“等于”或“小于”)生成物具有的总能量。
(3)b与a、c、d的数学关系式是_________
(4)已知25℃、101 kPa下,
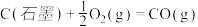 ;
; 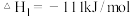
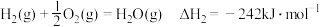
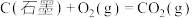
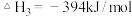
请写出一氧化碳与水蒸气作用生成氢气和二氧化碳的热化学方程式:__________
途径Ⅰ:
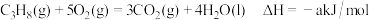
途径II:

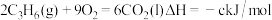
 (a、b、c、d均为正值)
(a、b、c、d均为正值)请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量
(2)在
 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量(3)b与a、c、d的数学关系式是
(4)已知25℃、101 kPa下,
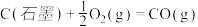 ;
; 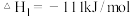
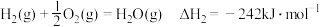
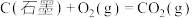
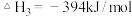
请写出一氧化碳与水蒸气作用生成氢气和二氧化碳的热化学方程式:
您最近一年使用:0次
9 . 在一定条件下,向容积为2 L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
(1)该条件下反应的化学平衡常数表达式为K=___________ 。
(2)平衡时升高温度,化学平衡常数的变化为___________ (填“变大”、“变小”或“不变”)。
(3)该条件下反应到达平衡时,CH3OH的转化率为___________ ,混合气体的压强是反应前的___________ 倍。
(4)该条件下判断该反应达平衡状态的依据是(填序号)___________ 。
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是( )
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
 CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则(1)该条件下反应的化学平衡常数表达式为K=
(2)平衡时升高温度,化学平衡常数的变化为
(3)该条件下反应到达平衡时,CH3OH的转化率为
(4)该条件下判断该反应达平衡状态的依据是(填序号)
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
您最近一年使用:0次
2021-01-13更新
|
308次组卷
|
2卷引用:海南省海口市琼山中学2019-2020学年度高二上学期第二次月考化学试题
10 . 回答下列问题:
消除含氮、硫等化合物对大气的污染,对建设美丽家乡、打造宜居环境具有重要意义。
(1)容积均恒定为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g) ⇌N2O4 ΔH<0,甲中NO2的相关量随时间变化如图所示。
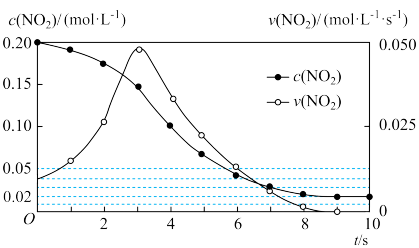
① 0~3 s内,甲容器中NO2的反应速率增大的原因是___________ 。
② 甲达到平衡时,温度若为T ℃,此温度下的平衡常数K=___________ 。(不用注明单位)
③ 平衡时,p甲___________ p乙(填“>”、“<”或“=”,下同),原因是:___________ 。
④平衡时,K甲___________ K乙
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) ΔH2<0.820℃ 时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0.
平衡时,甲容器中CO的转化率是___________ (填“>”、“=”、“<”或“无法判断”);丙容器中n(CO)为___________ mol。
消除含氮、硫等化合物对大气的污染,对建设美丽家乡、打造宜居环境具有重要意义。
(1)容积均恒定为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g) ⇌N2O4 ΔH<0,甲中NO2的相关量随时间变化如图所示。

① 0~3 s内,甲容器中NO2的反应速率增大的原因是
② 甲达到平衡时,温度若为T ℃,此温度下的平衡常数K=
③ 平衡时,p甲
④平衡时,K甲
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) ΔH2<0.820℃ 时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0.
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
您最近一年使用:0次



